(厦门大学化学化工学院,固体表面物理化学国家重点实验室,福建 厦门 361005)
(State Key Laboratory of Physical Chemistry of Solid Surfaces,College of Chemistry and Chemical Engineering,Xiamen University,Xiamen 361005,China)
high sensitivity-low energy ion scattering spectroscopy(HS-LEIS); low energy ion scattering spectroscopy(LEIS); X-ray photoemission spectroscopy(XPS); heterogeneous catalysis; surface composition; structure-activity relationshipdoi:10.6043/j.issn.0438-0479.202006022
DOI: 10.6043/j.issn.0438-0479.202006008
备注
多相催化反应大多在催化剂表层发生,研究催化剂的表面组成、结构、化学态和催化性能之间的关系对于设计、优化工业催化剂具有重要意义.高灵敏度低能离子散射谱(HS-LEIS)既可测定样品(包括粉末及块状样品、导体和半导体等)最外原子层的元素组成和相对含量,又可推断催化剂的表面结构,因此被广泛应用于各类催化反应研究中.本文介绍了HS-LEIS的基本原理,并概述了其在催化研究中的一些应用,包括催化剂表面组成、表面活性位、双金属催化剂表面偏析和表面结构、核壳结构等的研究.同时还对比分析了目前在表面研究中应用广泛的X-射线光电子能谱(XPS)和HS-LEIS表征结果的差异,进一步说明HS-LEIS能够更为准确地获得催化剂表面的真实情况.
Heterogeneous catalytic reactions always take place on the surfaces of catalysts.It is critical to understand the surface properties,such as elements on the outmost surface,local structures,electronic properties,etc.,as well as changes of the surfaces induced under reaction conditions.High sensitivity-low energy ion scattering spectroscopy(HS-LEIS)is a unique technology that can not only sensitively analyze the composition and relative content of elements in the outermost atomic layer of a sample(induding powder and bulk samples,conductors and semiconductors),but also infer the surface structure of catalysts.Therefore,HS-LEIS has been widely used in various catalytic reactions.In this overview,HS-LEIS is introduced.Catalysis studies using HS-LEIS in studying the surface composition,surface segregation,dispersion of the active component,supported bimetal system,active surface species,core-shell structure,strong metal-support interaction,and catalytic active centers are discussed.The currently widely used X-ray photoemission spectroscopy(XPS)in catalyst characterization is compared with HS-LEIS,and HS-LEIS can achieve a more reliable surface composition than XPS of heterogeneous catalysts.
引言
多相催化反应大多发生在催化剂表层,明确催化剂的表面组成、结构、化学态和催化性能之间的关系对于设计、优化工业催化剂具有重要意义.随着科学技术的发展,特别是各种基于超高真空表面科学表征手段的出现,如低能离子散射谱(LEIS)、X-射线衍射(XRD)、X-射线光电子能谱(XPS)、X-射线吸收能谱(XAS)、X-射线吸收精细结构谱(XAFS)、扩展XAFS(EXAFS)、 近边XAFS(NEXAFS)、红外光谱、拉曼光谱、扫描电镜(SEM)、透射电镜(TEM)等被广泛应用于催化剂的结构表征中[1-3],使得从原子、分子水平深入了解催化活性与表面组成、结构的关系变成可能.其中LEIS所获得的信息来自样品最表层,同时通过逐层溅射可获得一定深度的样品组成变化,因而成为研究表面组成、表面结构以及表面变化过程的有效手段.利用LEIS 可以鉴定吸附物种的几何结构,例如通过LEIS表征确定在Ru(0001)表面 13CO 在单原子的石墨表面发生插层反应,插入方式为O端朝上,但是随着温度升高插入的CO分子发生倾斜[4].LEIS可以很好地测定W表面水汽吸附厚度[5].利用LEIS可以测定CuAu(100)合金中Au的表面富集及其随处理温度的变化[6].通过LEIS测得真空退火状态下多晶Pt3Sc 表面被Pt覆盖,其电化学催化氧化还原反应活性完全不同于Pt(111)表面[7].LEIS可用于鉴定离子液体真空条件下的表面元素,并给出准确清晰的表面元素组成图[8].LEIS结果表明在电化学电池中杂质从氧化钇稳定氧化锆(YSZ)电解液中析出并迁移至镧锶钴铁氧(LSCF)阴极表面,这种电极组分和杂质之间的相互迁移对电池性能具有一定的影响[9].总之LEIS被广泛应用于各个领域.近年来随着高灵敏度LEIS(HS-LEIS)的出现使得表面粗糙、绝缘的粉末样品也可通过HS-LEIS表征获得其表面组成和结构信息,例如表面浸润、表面吸附、表面污染、薄膜生长、催化剂表面组成、合金/核壳结构以及表面活性位点和反应机理的研究[10-14].
1 LEIS介绍
LEIS使用较低能量(离子动能为0.5~10 keV)的惰性气体离子(He+、Ne+、Ar+、Kr+)入射到样品表面,与样品表面原子发生作用,实验证明低能离子与固体表面原子的碰撞主要为弹性碰撞,根据弹性散射理论,通过对散射离子能量进行分析可以得到表面元素组分及表面结构信息.如图1所示,已知质量m1能量E0的离子入射到样品表面(质量m2)通过θ角散射以后,根据能量守恒和动量守恒,剩余能量Ef由方程(1)获得[15-16],从而使能量标度变成样品上靶原子的质量标度,获得m2进而确定样品的表面元素组成.由于低能离子的散射截面和离子在表面内外的中和概率都很高,使得低能离子散射的信息深度仅仅是表面的最外一层或二层,成为名副其实的表面灵敏分析手段.LEIS上尖锐的特征峰代表了深度只有几百皮米处的散射,这种单原子层灵敏的检测方法,在诸如多相催化剂、原子扩散、合金表面偏析、半导体、陶瓷、腐蚀等研究中是非常重要的,使得LEIS成为最有效的表面分析手段之一.
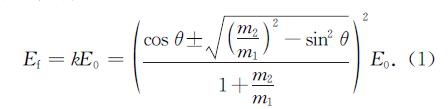
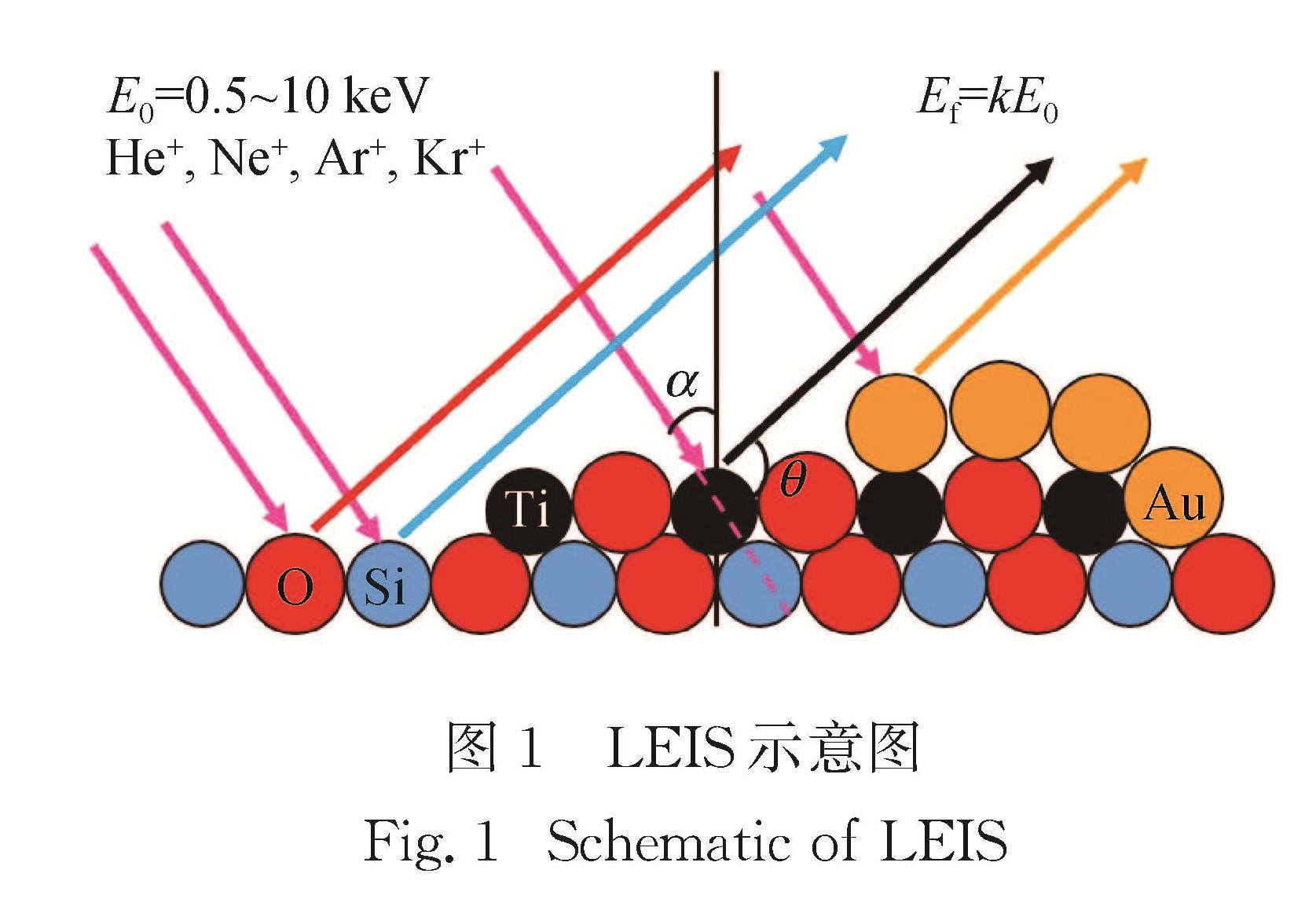
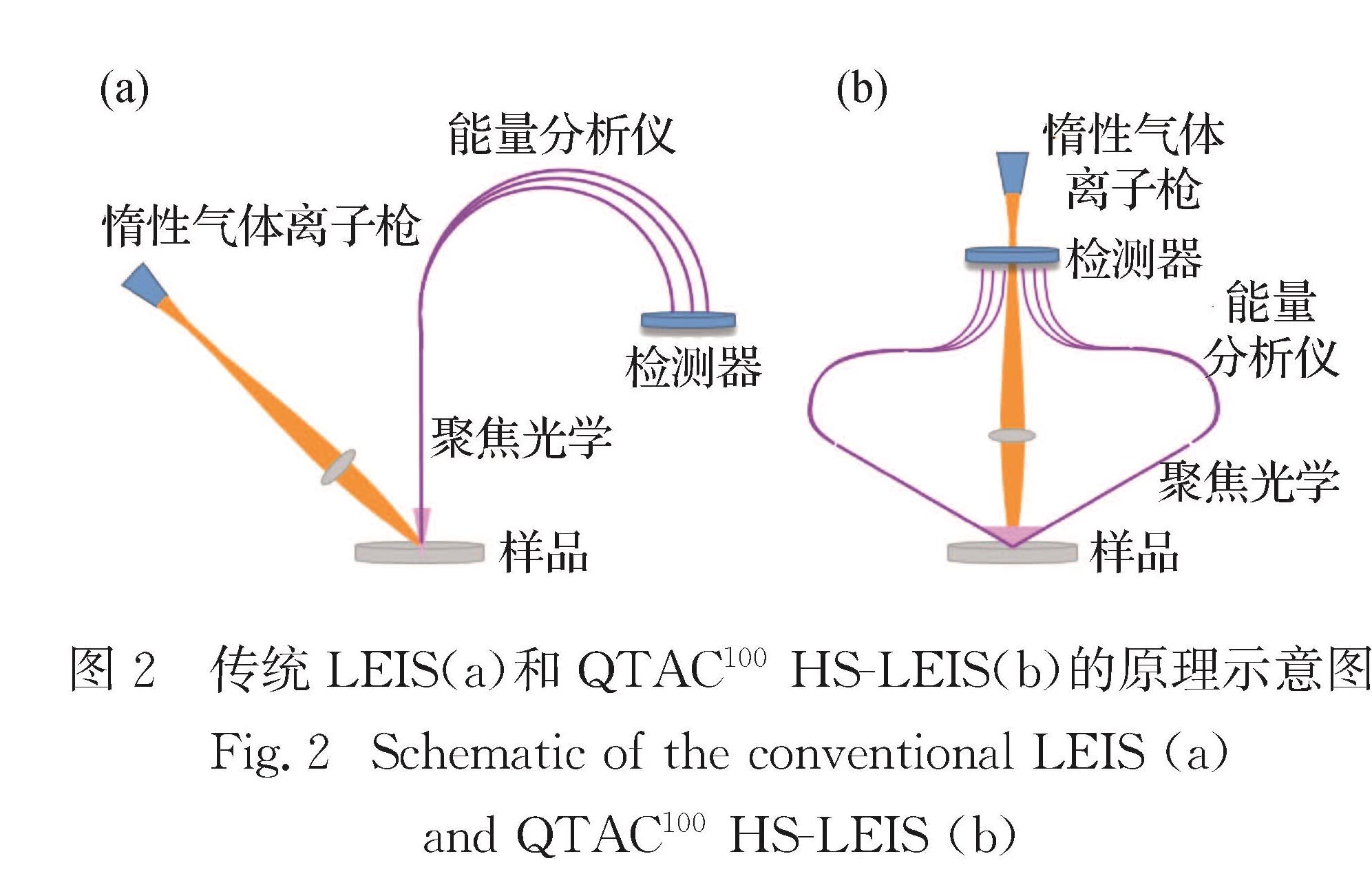
早期传统LEIS是通过光电子能谱仪上的半球形分析器检测获得(图2(a)),灵敏度较低,只局限于表面光滑的样品表面分析(如单晶样品),对于表面不规则的粉末样品检测到的信号非常弱,分析结果误差大.近年来,德国IONTOF公司生产的QTAC100采用筒镜能量分析器(cylindrical mirror analyzer,CMA),入射离子流垂直入射样品表面,并通过新型的360°全方位角离子收集器收集样品表面特定区域几乎全部的反射离子,其灵敏度是传统仪器的3 600倍(图2(b))[10-13,17-18].HS-LEIS表面元素检测限可达到0.001% 单原子层(Li~O:≥1%单原子层; F~Cl:1%~0.05% 单原子层; K~U:0.05%~0.001%单原子层),可应用于粗糙的粉末样品(包括绝缘样品)的各类材料分析中.根据出峰位置和峰强度可以获得样品表面元素组成和相对含量.但由于目前对散射截面和中和概率这两个因素的了解还不够,所以在对样品表面元素组成做定量分析时需要进行标准样品矫正.此外虽然低能离子主要和表面原子作用,但在实际测试中仍有部分离子会进入样品次表面,和次表面原子发生碰撞,从而造成元素峰左侧拖尾.通过拖尾峰和背景峰的高度可以大致判断表面元素的覆盖深度.不同惰性气体离子在样品表面发生碰撞的过程不同,得到的散射谱特性不同.4He+质量轻,在相同入射能量下对样品的表面损伤程度小,理论上能够分析He之后的所有元素,但在实际测试过程中由于二次离子散射的背景峰较高,所以对Li、Be、B等元素的灵敏度不高,出峰不明显,并且对邻近元素的分辨率也不高.20Ne+比4He+的质量大,分辨率较高,能够分析质量数相近的峰,但当其与表面质量数低的原子碰撞时容易发生溅射,因此只适用于质量数大于Si的元素分析.厦门大学购置的德国IONTOF 公司的QTAC100HS-LEIS仪还配备了XPS(Omicron公司的Sphera Ⅱ hemispherical的分析器),可实现LEIS-XPS联用(图3).此外本课题组还自行设计了2个样品预处理反应池,可实现催化剂在不同温度(最高600 ℃)、不同气氛下模拟真实反应/处理气氛,反应后气体抽真空,样品在真空状态下转移至HS-LEIS或XPS分析室,避免样品暴露于大气中,可最大程度地获得催化剂表面的真实情况.本文所述LEIS是将离子流密度为1 325 pA/cm2的3 keV 4He+或离子流密度为445 pA/cm2的5 keV 20Ne+作用于样品表面,一方面保证了检测器接收到的离子流密度能够得到较为显著的特征峰,另一方面避免了离子流密度过大导致表面发生溅射得到的样品信息并非仅最表层的信息.不同元素的HS-LEIS灵敏度因子通过测试对应的标准样品获得.目前XPS依旧被广泛用于近表面组成和化学态的分析,本文对比了HS-LEIS 和XPS表征测定样品表面组成的差异.其中:XPS测试在Omicron公司的 Sphera Ⅱ hemispherical的分析器上进行,以Al K(1 486.6 eV,300 W)为X射线辐射源,以C-1s(284.6 eV)的结合能校正其他元素的结合能.图2 传统LEIS(a)和QTAC100 HS-LEIS(b)的原理示意图
Fig.2 Schematic of the conventional LEIS(a)and QTAC100 HS-LEIS(b)2 HS-LEIS在多相催化中的应用
2.1 表面组成分析多相催化反应主要作用于催化剂表面,因此针对催化剂表面(a)HS-LEIS谱图;(b)XPS Pd-3d谱图;(c)根据XPS和HS-LEIS统计得出的5%Pd/TiO2在
程序升温氧化过程中表面Pd原子分数的变化趋势;(d)由HS-LEIS统计结果得出的
5%Pd/TiO2经过350 ℃氧化和500 ℃还原循环处理后表面Pd原子分数的变化.
组成的研究尤为重要.由于传统LEIS对粉末样品的响应信号弱,很难用于真实催化剂的表征中,所以在HS-LEIS发展起来之前人们大多通过XPS来测定粉末样品的表面组成和含量,但由于XPS检测结果反映的是样品近表层(10~20个原子层)的平均结果,并不能很好地关联催化剂表面组成和反应性能.为了更好地说明HS-LEIS在表面组成和活性组分分散度中的应用,本课题组[19]对比了5%Pd/TiO2(5%为质量分数,下同)在不同氧化还原反应条件下的HS-LEIS和XPS对表面组成的表征结果.图4 5%Pd/TiO2在不同温度氧化后的HS-LEIS和XPS谱图及其表面Pd原子分数(修改自文献[19])
Fig.4 HS-LEIS and XPS spectra and surface atomic fraction of Pd for the oxidation of the 5%Pd/TiO2 after oxidation at various temperatures(modified from Ref.[19])图4(a)是5%Pd/TiO2催化剂在不同温度氧化后的HS-LEIS谱图,可以看出,随着氧化温度升高,表面Pd信号逐渐增强,在350 ℃达到最大值,当温度进一步升高,Pd信号开始减弱.图4(b)是5%Pd/TiO2升温氧化过程中的XPS谱图,该体系中所有元素的结合能统一用位于458.9 eV的Ti4+-2p3/2峰进行标定,其中335 eV对应金属Pd(Pd0-3d5/2),337 eV对应PdO(Pd2+-3d5/2)的结合能.如图4(b)所示,升温氧化过程中金属Pd逐渐向PdO转变,在较低温度氧化时(100~300 ℃)PdO的生成速度较为缓慢,在350 ℃氧化气氛处理后,表面金属Pd迅速并且完全转化为体相PdO.温度进一步升高,PdO部分分解,近表面Pd含量降低.图4(c)是根据XPS和HS-LEIS两种测试结果统计给出的表面Pd原子分数随着温度变化的曲线,可以看出均呈现类似火山型曲线,即先升高后降低,在300~350 ℃时到达最大值,但通过HS-LEIS表征结果得到的表面Pd原子分数明显高于XPS的统计结果,说明HS-LEIS能够得到更加准确的催化剂表面组成表征结果.图4(d)为HS-LEIS统计结果得出的5%Pd/TiO2经过350 ℃氧化和500 ℃还原循环处理后表面Pd原子分数的变化,氧化状态下表面Pd原子分数是还原状态时的2.5倍,在多次循环处理过程中表面Pd原子分数的变化趋势可重复,说明在低于350 ℃时PdO在TiO2载体表面的分散度要明显优于金属Pd,Pd和载体的有效界面明显提高.
图5 不同载体负载的Au催化剂的HS-LEIS谱图[20]
Fig.5 HS-LEIS spectra of Au catalysts with different supports[20]图6 不同还原温度下2%Au/TiO2(a)和2%Au/TS-6(b)的HS-LEIS谱图及其Au信号变化曲线(c)和催化CO氧化反应的稳定性(d)[20]
Fig.6 HS-LEIS spectra for 2%Au/TiO2(a)and 2%Au/TS-6(b)after hydrogen reduction at various temperatures,the signal of Au as a function of reduction temperature(c),CO oxidation activities as a function of the reaction time(d)[20]2.2 表面活性组分的分散度催化反应主要发生在催化剂表面,因此催化剂表面活性组分的分散度决定了其催化反应性能.例如纳米Au催化剂对CO具有很好的催化活性,Au在催化剂表面的分散情况和热稳定性会影响其催化反应性能.本课题组[20]利用表面溶胶凝胶法制备了TiOx/SiO2(TS-6)复合载体,该载体中Ti以Ti—O—Si的形式高分散在SiO2表面,利用该载体进一步通过浸渍法制备了2%Au/TS-6 催化剂,同时还制备了普通TiO2负载的2%Au/TiO2催化剂作为对比.图5为2%Au/TiO2和2%Au/TS-6催化剂的HS-LEIS表征结果,通过对峰面积矫正计算得出2%Au/TS-6和2%Au/TiO2的表面Au信号所占比例分别为5.5%和3.5%,即在相同制备条件和相同Au负载量的情况下Au/TS-6催化剂中Au纳米颗粒的分散性更好,表面暴露出的Au活性位更多,同时Au/TS-6催化CO表现出的氧化活性更高.图6(a)~(c)为2%Au/TiO2和2%Au/TS-6催化剂经不同温度还原后的HS-LEIS 表征结果,由图可知,随着还原温度的升高2%Au/TiO2催化剂表面Au的信号强度明
显减弱,而2%Au/TS-6催化剂表面Au信号强度降低幅度较小,说明TiO2上负载的Au随着温度升高发生了明显的烧结,而TS-6上负载的Au烧结现象并不明显.这可能是TS-6载体上高分散的TiOx不仅提高了Au的分散度还提高了Au的抗烧结能力从而使催化剂的催化性能和稳定性得到改善(图6(d)).
2.3 双金属催化剂表面偏析研究对于双金属催化剂,在过去相当长的一段时间里,人们主要通过调整双金属的体相组成进而优化催化反应性能.但在实际催化反应过程中,反应温度、压力以及表面吸附物种等因素对双金属催化剂的尺寸、形态和表面组成都会有所影响,例如不同反应条件下某种金属在表面富集,导致表面和体相组成存在一定差异.这种表面重构过程导致暴露在表面的活性位点数量有所不同而表现出不同的催化反应性能.Goodman课题组[21-23]利用传统LEIS对真空退火过程中Mo(112)单晶上PdAu双金属膜表面元素组成的变化进行考察,发现Au倾向于在表面富集.Tenney等[24]通过LEIS研究发现:在TiO2(110)表面Pt-Au体系中Au趋向于在表面富集,当Au的体相摩尔分数高于50%时最表层几乎全部为Au,只有当Au的体相摩尔分数低于50%不能完全包裹Pt时,LEIS才检测到少量表面的Pt信号峰,如Au体相摩尔分数为25%时其在表面的占比达到65%; 但是在CO气氛下,CO会诱导Pt从体相析出,尤其是当表面全部被Au覆盖的情况下,Pt被诱导析出的现象更为明显.这种Au在表面富集的现象也同样存在于AuRh/TiO2(110)体系,甚至在室温下便能够发生[25],这主要是因为Au的表面自由能比Rh低引起的.限于传统LEIS的检测灵敏度不高,上述双金属体系的表面偏析现象都是基于对单晶模型催化剂的研究,然而真实的粉末颗粒状催化剂的表面组成和结构变化更为复杂.本课题组利用HS-LEIS和XPS对PdAu/TiO2粉末样品在氧化、还原和实际反应条件下的表面组成变化进行了详细研究,并构筑其在催化CO氧化反应过程中的构效关系[19].如图7所示:H2预还原的PdAu/TiO2最表层只有Ti、O、Pd和Au 4种元素峰,表面不存在其他污染物(图7(a)); 在氧化气氛中PdAu/TiO2随着氧化温度增加Pd逐渐被氧化生成PdO(图7(b)),Pd的XPS和HS-LEIS特征峰的峰面积逐渐增加,Au的峰面积逐渐减少,升温至450 ℃时表面Pd的峰面积开始出现减弱趋势,而Au峰面积增大(图7(a)~(c)),说明氧化过程中随着PdO的生成,Pd表面暴露量逐渐增多; 当氧化温度继续升高至500 ℃,表面Pd/Au原子比开始减小(图7(d)),这可能是因为500 ℃高温氧化后负载的双金属纳米粒子发生了烧结,从而导致表面Pd浓度降低.图7(d)对比了氧化反应过程中HS-LEIS和XPS两种测试手段得到的5%Pd0.97Au/TiO2催化剂上表面Pd/Au原子比的变化情况,它们具有相同的变化趋势,即先增大后减小.图7(d)黑色虚线为ICP-MS测定的体相Pd/Au摩尔比,可以看出,通过XPS表征得到的Pd/Au摩尔比和体相组成接近,而HS-LEIS给出的摩尔比要远大于体相组成,并且变化趋势更为显著,在450 ℃达到最大值,说明氧化过程中PdAu双金属纳米粒子中的金属Pd逐渐被氧化形成PdO并不断向表面迁移,上述结果再次证明HS-LEIS对表面元素组成的表征能够给出比XPS更为准确的结果,能够更加真实地反映催化剂的表面组成和变化.图7 500 ℃氢气预还原后5%Pd0.97Au/TiO2在各氧化温度下的HS-LEIS谱图(a)及其Pd-3d(b)和Au-4f(c)的XPS谱图和由XPS和HS-LEIS计算得出的表面Pd/Au原子比的变化趋势(d)(修改自文献[19])
Fig.7 HS-LEIS spectra(a)and XPS spectra of Pd-3d(b)and Au-4f(c)for the 5%Pd0.97Au/TiO2 prereduced of H2 at 500 ℃ and then oxidized at various temperatures,and atomic ratio of Pd/Au of surface evaluated from the XPS and HS-LEIS peak area(d)(modified from Ref.[19])为了进一步证实氧化后5%Pd6.8Au/TiO2 催化剂中PdO在表面富集的结果,利用5 keV 20Ne+对氧化后催化剂进行连续测试(溅射)获得一系列HS-LEIS谱图,从图8(a)可以直观地看出随着溅射深度增加,Pd信号峰强度逐渐减弱,当溅射深度达到2.4nm时表面Pd/Au原子比从13降到7.如图8(b)中结构示意图所示,连续测试(溅射)剖析过程中纳米颗粒表面Pd组分被逐渐剥离,暴露出更多的内层Au元素,剥离过程中测得的内层Pd相对含量逐渐减少,说明5% Pd6.8Au/TiO2表面Pd浓度比内层更高,氧化后催化剂呈现表面Pd富集的结构.Lee等[26]利用XAS发现,Al2O3负载的AuPd双金属也有类似的表面偏析核壳结构形成.Edwards等[27]通过电镜直观地看到焙烧后的AuPd/TiO2结构上的变化.Delannoy等[28]发现,当AuPd/TiO2室温暴露于400 Pa的O2气氛下1 min,高分辨透射电镜(HRTEM)图像就能观察到双金属纳米粒子转变为表面Pd富集的核壳结构,而在室温H2气氛下再次恢复至两种金属均匀分布的合金结构.5%Pd0.97Au/TiO2催化剂在H2气氛下程序升温还原过程的HS-LEIS结果表明[19]:Pd/Au原子比随着还原温度的增高逐渐减小(图9),与氧化过程呈现正好相反的趋势.空气氧化过程对应去合金化过程,H2还原过程中表面PdO重新被还原成金属Pd并再次形成合金,表面Pd含量减少,这一过程说明双金属体系表面组成因反应气氛的改变而相应地发生变化.图8 5%Pd6.8Au/TiO2的HS-LEIS(20Ne+)谱图(a)及其表面Pd/Au原子比随着溅射深度的变化(b)[19]
Fig.8 HS-LEIS(20Ne+)spectra of 5%Pd6.8Au/TiO2(a)and variation of Pd/Au atomic ratio on 5%Pd6.8Au/TiO2surface with sputtering depth(b)[19]进一步对不同体相组成的PdxAuy和PdxAuy/TiO2进行HS-LEIS表征,构筑双金属催化剂表面-体相组成相图.如图 10所示,无论是非负载型PdxAuy还是负载型5%PdxAuy/TiO2在H2气氛下表面Pd含量都稍高于体相组成,在空气中氧化后二者表面的Pd含量都明显增加,说明载体TiO2对双金属PdxAuy表面组成的影响并不显著.图中星号代表5%Pd0.97Au/TiO2经过500 ℃高温预还原并在200 ℃反应气氛下处理后的组成,它与500 ℃H2预处理后的组成接近.根据文献报道以Mo(111)单晶为基底的PdxAuy双金属薄膜在真空退火过程中Au在表面富集(图 10绿色线所示)[21-22].PdAu[23,29]、PtAu[24]和RhAu[25]纳米粒子在极性氧化物表面同样表现出Au在表面富集.但是PdxAuy在H2还原下表面还是略富集Pd,经空气氧化后表面Pd显著富集.上述研究表明采用不同气氛条件处理会引起催化剂表面组成不同.图9 根据HS-LEIS计算出的5%Pd0.97Au/TiO2表面Pd/Au原子比随着H2还原温度的变化[19]
Fig.9 Atomic ratio of Pd/Au as a function of the reduction temperature for the 5%Pd0.97Au/TiO2,which reduced by H2 and characterized by HS-LEIS[19]星号表示的是5%Pd0.97Au/TiO2经过500 ℃高温预还原
并在200 ℃反应气氛下处理后的组成,绿色线来源于
文献[22]报道的超高真空退火后的数据.
反应条件:催化剂60 mg,V(CO):V(O2):V(He)=1:1:98,流速 30 mL/min,反应温度90 ℃.图 10 分别经过450 ℃氧化和500 ℃还原后,TiO2负载和非负载PdxAuy催化剂表面-体相Pd/(Pd+Au)原子比(HS-LEIS)的变化相图[19]
Fig.10 Phase diagrams of surface atomic ratio of Pd/(Pd+Au)(HS-LEIS)as a function of the bulk value for both supported and unsupported PdxAuy catalysts after oxidation at 450 ℃ and reduction at 500 ℃[19]众所周知,多相催化大多发生在催化剂表面,其催化活性主要取决于表面组成和结构.将5%Pd0.97Au催化剂HS-LEIS表征结果与CO氧化活性相关联,如图 11(a)所示,预还原后催化剂催化CO氧化性能优于预氧化后的,并且随着还原温度的升高反应活性增加.表面Pd/Au原子比随H2气氛下程序升温逐渐降低(图9),而氧气氛下表面Pd/Au原子比增大(图7(d)).不同体相组成对CO氧化也有一定影响,如图 11(b)所示,500 ℃预还原后不同组成的PdxAuy/TiO2催化剂对CO氧化活性不同.以90 ℃时的转换频率(TOF)对最表层Pd/(Pd+Au)原子比作图(图 11(c)),当原子比小于0.65时催化活性较高,结合文献[30-31]结果推断当表面Pd原子被Au原子隔离时催化反应活性较高,当表面Pd含量过高容易形成Pd纳米团簇导致活性急剧降低.根据Shen等[32-33]报道,Au能够调整Pd表面的CO吸附能,相对于体相Pd,Au(111)上Pd覆盖度较低时CO吸附能较弱.Sellidj等[34]的研究结果也表明Pd/Au(111)体系中Pd覆盖度较低时,Pd的电子结构较容易受基底Au的影响,其表面CO结合能降低,但是表面完全覆盖Pd原子后,其表面CO吸附能与Pd(111)上的CO吸附能一致.图 11 不同预处理后5%Pd0.97Au/TiO2(a)和500 ℃预还原后不同组成的5%PdxAuy/TiO2(b)催化CO氧化的活性,以及90 ℃时不同成5%PdxAuy/TiO2催化CO反应的TOF对最表层Pd/(Pd+Au)原子比作图(c)[19]
Fig.11 Oxidation activity of CO catalyzed by 5%Pd0.97Au/TiO2 under different pretreatment(a)and 5%PdxAuy/TiO2 which prereduced under 500 ℃(b), CO TOF as a function of the surface atomic ratio of Pd/(Au+Pd)for 5%PdxAuy/TiO2 react at 90 ℃(c[19]不同载体和处理条件对表面组成、形态、分散度以及化学态的影响显著.本课题组[35]研究报道了PtCux/TiO2在氧化状态下发生去合金现象,表面形成CuO,在还原状态下重新生成PtCux合金; 并利用HS-LEIS 表征结果得到PtCux合金和PtCux/TiO2的表面组成对体相组成的相图(图 12).由图 12(a)可以明显看出对于PtCux/TiO2催化剂无论是氧化状态还是还原状态下表面Pt/(Pt+Cu)原子比都明显低于体相,说明Cu高度分散于PtCux/TiO2表面,
并且氧化状态下表面Cu原子分数高于还原状态下.如图 12(b)所示,PtCux合金催化剂的表面Pt/(Pt+Cu)原子比也低于体相,Cu在表面富集,但在还原状态下其表面Cu原子分数高于PtCux/TiO2,氧化状态下其表面Cu原子分数低于PtCux/TiO2,由此可知载体对合金表面金属含量具有一定的影响.类似的情况同样发生于PtSn/SiO2体系[36].根据Martin等[37]报道PdPt/Al2O3催化剂在800 ℃焙烧后能够形成PdPt双金属合金和PdO,PdO存在于PdPt纳米粒子表面或者以孤立的PdO团簇出现在氧化物载体上.PdPt合金纳米粒子在不同气氛下处理后其表面组成和化学态有所不同,氧化状态下发生去合金反应,Pd被氧化生成PdO后向表面偏析形成PdO壳,还原状态下表面重新生成PdPt合金和金属Pd.图 12 PtCux/TiO2催化剂(a)和PtCux催化剂(b)的表面-体相组成相图[35]
Fig.12 Phase diagrams of the surface composition versus the bulk composition for PtCux/TiO2 catalyst(a),and PtCux catalyst(b)[35]2.4 表面活性位研究多相催化大多发生在催化剂表面,如何确定表面活性位,理解催化反应机理是设计和优化催化材料的关键.Zhu等[38]报道了Ru(纳米团簇)-Ni/NiO(Ru纳米团簇负载在Ni/NiO纳米粒子上)对苯加氢的活性要明显优于RuNi合金和Ru/Ni纳米粒子,并通过HS-LEIS表征对比了Ni/NiO/C、Ru/C、Ru-Ni/NiO/C、Ru-Ni/Ni(OH)2/C以及RuNi(合金)/C的表面组成情况.4He+ HS-LEIS 谱图表明Ru-Ni/NiO/C表面存在C、O、Ni和Ru.Ni/NiO/C 20Ne+谱只显示Ni的峰,Ru/C 20Ne+ 谱只显示Ru峰,Ru-Ni/Ni(OH)2/C、RuNi(合金)/C和Ru-Ni/NiO/C表面Ru和Ni同时存在,但是Ru-Ni/NiO/C表面Ru的含量要明显高于Ru-Ni/Ni(OH)2/C和RuNi(合金)/C,说明Ru在Ru-Ni/NiO/C表面高度分散.利用20Ne+离子流对样品连续测试时,样品表面被溅射可以获得样品不同深度的组成变化.Ru-Ni/NiO/C随着溅射扫描时间(溅射深度)增加,表面Ru的信号减弱,Ni的信号出现并逐渐增强,进一步证明Ru主要以纳米团簇的形式存在于Ru-Ni/NiO/C 表面.RuNi(合金)/C随着溅射扫描时间增加其Ru/Ni 原子比几乎不变,证明RuNi 在表面形成合金.通过进一步对比Ru-Ni/NiO/C、Ru-Ni/Ni(OH)2/C和RuNi(合金)/C几种催化剂对苯加氢的反应活性,推断Ru在Ru(纳米团簇)-Ni/NiO(纳米粒子)催化剂中Ru纳米团簇和Ni/NiO 之间具有协同作用.Ru提供H2吸附位和解离位,解离后的氢通过Ni“桥”转移到苯上,最终苯在NiO上活化生成环己烷.纳米团簇/纳米粒子/纳米氧化物这种不同金属间尤其是贵金属(Ru、Pt、Rh、Pd、Au等)和过渡金属(Ni、Fe、Co、Cu等)间的协同作用为多相催化剂的设计提供了一个新的思路.
Pt-Fe(OH)x/TiO2纳米催化剂具有较高的CO氧化活性[39],HS-LEIS表征结果表明当其表面同时存在Fe和Pt并形成Fe3+—OH—Pt 活性界面时对CO氧化表现出较高的活性.但由于Fe3+—OH—Pt 活性界面不稳定容易发生水解,导致催化剂容易失活.为了稳定Fe3+—OH—Pt 活性界面,引入Ni(OH)2与Fe(OH)x相互作用形成稳定的Pt-FeNi(OH)x/TiO2催化剂.此外Ni(OH)2 还起到解离表面吸附的水分子的作用.HS-LEIS结果(图 13)显示Pt-FeNi(OH)x/TiO2表面同时存在Pt、Fe和Ni,其界面协同促进CO在室温下即可被氧化,且催化剂寿命长达一个月以上.
图 13 Pt-Fe(OH)x/TiO2(a)和Pt-FeNi(OH)x/TiO2(b)的HS-LEIS谱图[39]
Fig.13 HS-LEIS spectra of the Pt-Fe(OH)x/TiO2(a)and Pt-FeNi(OH)x/TiO2(b)[39]2.5 核壳结构表征在许多催化反应中,具有核壳结构的催化剂都表现出极佳的催化性能,但这种优势的原因还有待进一步研究.虽然目前HRTEM经常被用来判定催化剂是否存在核壳结构,但HRTEM通常观测的只是催化剂局部的范围,很难区分原子质量接近、衬度相近的不同元素,而且对于一些氧化物基底负载的贵金属催化剂很难通过HRTEM来判断是否存在核壳结构,此外通过HRTEM很难分辨表面是被部分覆盖还是完全覆盖.HS-LEIS具有只检测催化剂最表层原子的灵敏度,不仅可以用于表面组成的测定,对催化剂的核壳结构判定也能给出更为直接的证据.
Pt/TiO2能够光催化还原CO2生成CH4或者CO.Zhai等[40]以TiO2为基底,光还原H2PtCl6 悬浊液获得0.9%Pt/TiO2,其中Pt平均粒径为3.1 nm; 将0.9%Pt/TiO2投入一定浓度的CuSO4溶液中,通过控制光照时间获得不同Cu含量的Cu/Pt/TiO2催化剂,标记为Cu/Pt/TiO2-x h,其中x h为光沉积时长.通过ICP-MS测试得知,随着光沉积时间延长,Cu含量逐渐增加.通过HRTEM可以看到,随着光沉积时间延长,Cu逐渐在Pt/TiO2表面沉积形成Cu壳层,但是HRTEM表征无法给出Pt表面何时被Cu完全覆盖.HS-LEIS 表征结果显示:随着光沉积时间延长,Cu的特征峰出现并逐渐增强,而Pt特征峰逐渐减弱; 当光沉积时长为5 h时,Pt特征峰完全消失,表明此时Pt表面被Cu完全覆盖形成Pt@Cu2O核壳结构.关联Cu/Pt/TiO2-x h光催化还原CO2生成CH4和CO的性能,在光沉积时长为5 h时,Cu/Pt/TiO2-5 h催化剂上Pt表面被Cu完全覆盖时催化性能最佳.根据HS-LEIS表征结果推断,CO2和H2O吸附在Cu2O表面,TiO2受光激发产生的光生电子经由Pt核转移到Cu2O壳层将CO2和H2O还原成CH4和CO,同时Cu2O壳层抑制了H2O在Pt表面直接分解生成H2,从而提高了光催化还原CO2的活性和选择性,获得最佳催化性能.当光沉积时间进一步延长至10 h时,由于Cu2O壳层的厚度偏大,不利于Pt核转移电子至Cu2O表面,导致Cu/Pt/TiO2-10 h催化活性降低.图 14 Pt/C和Pt@h-BN/C-700催化剂的HS-LEIS谱图[41]
Fig.14 HS-LEIS spectra of Pt/C and Pt@h-BN/C-700 catalysts[41]具有核壳结构的Pt@h-BN对CO的氧化性能要高于Pt/C催化剂[41].如图 14 HS-LEIS表征结果所示Pt/C催化剂表面存在大量的Pt,而Pt@h-BN表面Pt的信号峰非常弱,几乎被B和N形成的h-BN外壳所覆盖(由于B和N的灵敏度低所以信号峰不强).此外文献[41]还通过HRTEM进一步证明了Pt@h-BN的核壳结构.Pt@h-BN核壳结构对CO氧化具有较高的氧化活性是因为h-BN外壳不仅可以保护里层的Pt纳米粒子不容易被污染或者烧结,同时CO 和O2可以通过h-BN 外壳进入内核Pt的表面,从而提高催化剂的活性、选择性和稳定性.
核壳结构的PtRu@h-BN/C催化剂在质子交换膜燃料电池氢氧化(HOR)中的催化活性和传统的PtRu/C催化剂性能相差不大,但其抗CO中毒性要明显优于PtRu/C[42].如图 15(a)HS-LEIS表征结果所示PtRu/C 表面主要为高度分散的Pt和Ru,而PtRu@h-BN/C表面几乎检测不到Pt和Ru,说明Pt和Ru被h-BN所覆盖形成PtRu@h-BN核壳结构.图 15(b)HRTEM结果也显示PtRu表面被h-BN包裹形成PtRu@h-BN/C核壳结构,且其粒径大小和PtRu/C相当.图 15(c)和(d)中XPS 测得的N-1s和B-1s的结合能和文献报道的h-BN结合能[43-44]一致,说明h-BN在表面形成.利用苯并噻唑与PtRu表面能够发生不可逆转的螯合作用,也可以进一步证明PtRu@h-BN/C核壳结构.PtRu表面形成的h-BN外壳不仅可以提高其抗CO中毒性,还可以提高其抗烧结性和抑制C被氧化.
(d)中绿色峰是实验峰,可将其分解拟合成蓝色和红色的2种价态的峰.
图 15 PtRu/C和PtRu@h-BN/C 催化剂的HS-LEIS谱图(a),PtRu@h-BN/C催化剂的HRTEM图(b)、XPS N-1s(c)和B-1s(d)谱图[42]
Fig.15 HS-LEIS spectra of the PtRu/C and PtRu@h-BN/C catalysts(a), HRTEM images(b), XPS N-1s(c)and B-1s(d)spectra of the PtRu@h-BN/C catalyst[42]3 结论与展望
HS-LEIS作为表面灵敏的一种表征手段,既可用于测定表面化学组分,又可推断一些表面结构,一定条件下也可进行半定量的分析工作,其探测极限在1%~0.001%单原子层.就成分分析而言,由于LEIS具有只检测最外层原子的表面灵敏度,所以特别适用于研究催化剂的表面组成、活性组分分散度、表面偏析、表面活性位、不同反应条件下表面的变化以及反应机理等.利用Ne+或Ar+容易使样品表面发生溅射现象,通过连续测试逐层剥离可以获得由表层到里层的元素组成变化,可以用于判定样品结构,如合金和核壳结构等.利用HS-LEIS可以获得不同条件下表面组成对体相组成的相图,可以建立表面组成、结构和反应性能的构效关系,对更好地理解催化作用机理、设计新的催化剂和优化工业过程催化剂具有重要意义.
但目前HS-LEIS在上述应用中仍存在一定的局限性.如在表面组成含量分析中,由于目前对散射截面和中和概率这两个因素的准确测量还比较难,需要通过对已知标准样品进行灵敏度因子矫正; 而粉末样品压片成型得到的表面紧实度不同也会影响HS-LEIS的谱峰强度,因此在实际测试过程中很难获得样品表面组成的绝对含量.此外对于相邻的2种元素因其原子质量相近也难以分辨,需根据其原子轻重选用能获得较高分辨率的质量大的离子,如Ne+、Ar+、Kr+等,当然质量越大的元素对表面的剥离也越严重,同时对轻元素不灵敏,因此在分辨率足够的条件下应尽量选用质量小的离子作为离子源; 在定性或定量过程中也可以通过测试标准样确定某具体元素的峰形状和位置,然后进行分峰处理.在利用Ne+或者Ar+连续测试逐层剥离来判定样品结构时,存在表面择优溅射的现象,即表面较轻的元素更易被溅射,较重的元素更不易被溅射,因此随着溅射深度的增加获得的样品组成和实际情况有一定的偏差.在对表面活性位和反应机理等的研究中,由于样品反应后需要抽真空再转移至分析室,而真空状态下和反应条件下的样品表面状态存在一定的差异,导致分析结果和实际情况可能存在一定的偏差.
总而言之,HS-LEIS能够为催化表面研究提供强有力的证据支撑,但也存在一定的局限性.今后随着科学技术的发展,若能对散射截面及中和概率做进一步理论研究,并通过测试一系列不同标准样品获得不同元素的灵敏度因子数据库,提高仪器元素分辨率,实现原位状态下表面变化的实时检测,必将使HS-LEIS的应用范围更加广泛.
- [1] SOMORJAI G A,LI Y.Introduction to surface chemistry and catalysis[M].2nd Ed.[S.l.]:John Wiley & Sons Inc.,2010.
- [2] RODRIGUEZ J A,HANSON J C,CHUPAS P J.In-situ characterization of heterogeneous catalysts[M].Hoboken:John Wiley & Sons,Inc.,2013.
- [3] TADA M,IWASAWA Y.Chemical design and in situ characterization of active surfaces for selective catalysis[J].Annual Review of Materials Research,2005,35(1):397-426.
- [4] LI T B,YARMOFF J A.The orientation of CO intercalated between graphene and Ru(0001)[J].Surface Science,2019,680:6-10.
- [5] MAMEDOV N V,SINELNIKOV D N,KURNAEV V A,et al.LEIS analysis of the W surface during water vapor adsorption[J].Vacuum,2018,148:248-253.
- [6] BEIKLER R,TAGLAUER E.Surface segregation at the binary alloy CuAu(100)studied by low-energy ion scattering[J].Surface Science,2016,643:138-141.
- [7] JOHANSSON T P,ULRIKKEHOLM E T,HERNANDEZ FERNANDEZ P,et al.Pt skin versus Pt skeleton structures of Pt3Sc as electrocatalysts for oxygen reduction[J].Topics in Catalysis,2014,57(1/2/3/4):245-254.
- [8] VILLAR-GARCIA I J,FEARN S,DE GREGORIO G F,et al.The ionic liquid-vacuum outer atomic surface:a low-energy ion scattering study[J].Chemical Science,2014,5(11):4404-4418.
- [9] DRUCE J,TÉLLEZ H,SIMRICK N,et al.Surface composition of solid oxide electrode structures by laterally resolved low energy ion scattering(LEIS)[J].International Journal of Hydrogen Energy,2014,39(35):20850-20855.
- [10] TER VEEN H R J,KIM T,WACHS I E,et al.Applications of high sensitivity-low energy ion scattering(HS-LEIS)in heterogeneous catalysis[J].Catalysis Today,2009,140(3/4):197-201.
- [11] CUSHMAN C V,BRÜNER P,ZAKEL J,et al.Low energy ion scattering(LEIS):a practical introduction to its theory,instrumentation,and applications[J].Analytical Methods,2016,8(17):3419-3439.
- [12] GOEBL D,BRUCKNER B,ROTH D,et al.Low-energy ion scattering:a quantitative method?[J].Nuclear Instruments and Methods in Physics Research Section B:Beam Interactions with Materials and Atoms,2015,354:3-8.
- [13] BRONGERSMA H H,DRAXLER M,DE RIDDER M,et al.Surface composition analysis by low-energy ion scattering[J].Surface Science Reports,2007,62(3):63-109.
- [14] RAFATI A,TER VEEN R,CASTNER D G.Low-energy ion scattering:determining overlayer thickness for functionalized gold nanoparticles[J].Surface and Interface Analysis,2013,45(11/12):1737-1741.
- [15] SMITH D P.Scattering of low-energy noble gas ions from metal surfaces[J].Journal of Applied Physics,1967,38(1):340-347.
- [16] BRONGERSMAL H H,MU P M.Analysis of the outermost atomic layer of a surface by low-energy ion scattering[J].Surface Science,1973,35:393-412.
- [17] BRONGERSMA H H,GREHL T,SCHOFIELD E R,et al.Analysis of the outer surface of platinum-gold catalysts by low-energy ion scattering: improved resolution allows selective analysis of mixed metal systems[J].Platinum Metals Review,2010,54(2):81-87.
- [18] PRU。S∨A S,PROCHÁZKA P,BÁBOR P,et al.Highly sensitive detection of surface and intercalated impurities in graphene by LEIS[J].Langmuir,2015,31(35):9628-9635.
- [19] LI Y Y,HU J,MA D D,et al.Disclosure of the surface composition of TiO2 supported gold-palladium bimetallic catalysts by high-sensitivity low-energy ion scattering spectroscopy[J].ACS Catalysis,2018,8(3):1790-1795.
- [20] 李晓坤,马冬冬,郑燕萍,等.TiOx/SiO2复合载体上高分散Au催化剂的CO氧化性能[J].物理化学学报,2015,31(9):1753-1760.
- [21] CHEN M S,KUMAR D,YI C W,et al.The promotional effect of gold in catalysis by palladium-gold[J].Science,2005,310(5746):291-293.
- [22] YI C W,LUO K,WEI T,et al.The composition and structure of Pd-Au surfaces[J].The Journal of Physical Chemistry B,2005,109(39):18535-18540.
- [23] LUO K,WEI T,YI C W,et al.Preparation and characterization of silica supported Au-Pd model catalysts[J].The Journal of Physical Chemistry B,2005,109(49):23517-23522.
- [24] TENNEY S A,RATLIFF J S,ROBERTS C C,et al.Adsorbate-induced changes in the surface composition of bimetallic clusters:Pt-Au on TiO2(110)[J].The Journal of Physical Chemistry C,2010,114(49):21652-21663.
- [25] ÓVÁRI L,BUGYI L,MAJZIK Z.Surface structure and composition of Au-Rh bimetallic nanoclusters on TiO2(110):a LEIS and STM study[J].The Journal of Physical Chemistry C,2008:112:18011-18016.
- [26] LEE K E,SHIVHARE A,HU Y,et al.Supported bimetallic AuPd clusters using activated Au25 clusters[J].Catalysis Today,2017,280:259-265.
- [27] EDWARDS J K,SOLSONA B E,LANDON P,et al.Direct synthesis of hydrogen peroxide from H2 and O2 using TiO2-supported Au-Pd catalysts[J].Journal of Catalysis,2005,236(1):69-79.
- [28] DELANNOY L,GIORGIO S,MATTEI J G.Surface segregation of Pd from TiO2-supported AuPd nanoalloys under CO oxidation conditions observed in situ by ETEM and DRIFTS[J].ChemCatChem,2013,5(9):2707-2716.
- [29] HAIRE A R,GUSTAFSON J,TRANT A G,et al.Influence of preparation conditions on the depth-dependent composition of AuPd nanoparticles grown on planar oxide surfaces[J].Surface Science,2011,605(1/2):214-219.
- [30] VENEZIA A M,LIOTTA L F,PANTALEO G,et al.Activity of SiO2 supported gold-palladium catalysts in CO oxidation[J].Applied Catalysis A:General,2003,251(2):359-368.
- [31] SCOTT R W J,SIVADINARAYANA C,WILSON O M,et al.Titania-supported PdAu bimetallic catalysts prepared from dendrimer-encapsulated nanoparticle precursors[J].Journal of the American Chemical Society,2005,127(5):1380-1381.
- [32] SHEN X Y,FRANKEL D J,HERMANSON J C,et al.Photoemission studies of ordered Pd overlayers on Au(111):implications for CO chemisorption[J].Physical Review B,1985,32(4):2120-2125.
- [33] SHEN X Y,FRANKEL D J,LAPEYRE G J,et al.Photoemission and high-resolution electron-energy-loss spectroscopy studies of CO chemisorption on thin Pd films on Au(111)[J].Physical Review B,1986,33(8):5372-5377.
- [34] SELLIDJ A,KOEL B E.Electronic and CO chemisorp-tion properties of ultrathin Pd films vapor deposited on Au(111)[J].Physical Review B,1994,49(12):8367-8376.
- [35] HUANG J J,SONG Y Y,MA D D,et al.The effect of the support on the surface composition of PtCu alloy nanocatalysts:in situ XPS and HS-LEIS studies[J].Chinese Journal of Catalysis,2017,38(7):1229-1236.
- [36] LI Y Y,HUANG J J,ZHENG Y P,et al.Surface compo-sitions of oxide supported bimetallic catalysts:a compared study by high-sensitivity low energy ion scattering spectroscopy and X-ray photoemission spectro-scopy[J].The Chemical Record,2019,19(7):1432-1443.
- [37] MARTIN N M,NILSSON J,SKOGLUNDH M,et al.Characterization of surface structure and oxidation/reduction behavior of Pd-Pt/Al2O3 model catalysts[J].The Journal of Physical Chemistry C,2016,120:28009-28020.
- [38] ZHU L H,JIANG Y Y,ZHENG J B,et al.Ultrafine nanoparticle-supported Ru nanoclusters with ultrahigh catalytic activity[J].Small,2015,11(34):4385-4393.
- [39] CHEN G X,ZHAO Y,FU G,et al.Interfacial effects in iron-nickel hydroxide-platinum nanoparticles enhance catalytic oxidation[J].Science,2014,344(6183):495-499.
- [40] ZHAI Q G,XIE S J,FAN W Q,et al.Photocatalytic conversion of carbon dioxide with water into methane:platinum and copper(Ⅰ)oxide Co-catalysts with a core-shell structure[J].Angewandte Chemie International Edition,2013,52(22):5776-5779.
- [41] SUN M M,FU Q,GAO L J,et al.Catalysis under shell:improved CO oxidation reaction confined in Pt@h-BN core-shell nanoreactors[J].Nano Research,2017,10(4):1403-1412.
- [42] SUN M M,LV Y,SONG Y J,et al.CO-tolerant PtRu@h-BN/C core-shell electrocatalysts for proton exchange membrane fuel cells[J].Applied Surface Science,2018,450:244-250.
- [43] ZHANG Y H,WENG X F,LI H,et al.Hexagonal boron nitride cover on Pt(111):a new route to tune molecule-metal interaction and metal-catalyzed reactions[J].Nano Letters,2015,15(5):3616-3623.
- [44] KIM G,JANG A R,JEONG H Y,et al.Growth of high crystalline,single-layer hexagonal boron nitride on recyclable platinum foil[J].Nano Letters,2013,13(4):1834-1839.

![图4 5%Pd/TiO2在不同温度氧化后的HS-LEIS和XPS谱图及其表面Pd原子分数(修改自文献[19])<br/>Fig.4 HS-LEIS and XPS spectra and surface atomic fraction of Pd for the oxidation of the 5%Pd/TiO2 after oxidation at various temperatures(modified from Ref.[19])](2020年05期/pic34.jpg)
![图5 不同载体负载的Au催化剂的HS-LEIS谱图[20]<br/>Fig.5 HS-LEIS spectra of Au catalysts with different supports[20]](2020年05期/pic35.jpg)
![图6 不同还原温度下2%Au/TiO2(a)和2%Au/TS-6(b)的HS-LEIS谱图及其Au信号变化曲线(c)和催化CO氧化反应的稳定性(d)[20]<br/>Fig.6 HS-LEIS spectra for 2%Au/TiO2(a)and 2%Au/TS-6(b)after hydrogen reduction at various temperatures,the signal of Au as a function of reduction temperature(c),CO oxidation activities as a function of the reaction time(d)[20]](2020年05期/pic36.jpg)
![图7 500 ℃氢气预还原后5%Pd0.97Au/TiO2在各氧化温度下的HS-LEIS谱图(a)及其Pd-3d(b)和Au-4f(c)的XPS谱图和由XPS和HS-LEIS计算得出的表面Pd/Au原子比的变化趋势(d)(修改自文献[19])<br/>Fig.7 HS-LEIS spectra(a)and XPS spectra of Pd-3d(b)and Au-4f(c)for the 5%Pd0.97Au/TiO2 prereduced of H2 at 500 ℃ and then oxidized at various temperatures,and atomic ratio of Pd/Au of surface evaluated from the XPS and HS-LEIS peak area(d)(modified from Ref.[19])](2020年05期/pic37.jpg)
![图8 5%Pd6.8Au/TiO2的HS-LEIS(20Ne+)谱图(a)及其表面Pd/Au原子比随着溅射深度的变化(b)[19]<br/>Fig.8 HS-LEIS(20Ne+)spectra of 5%Pd6.8Au/TiO2(a)and variation of Pd/Au atomic ratio on 5%Pd6.8Au/TiO2surface with sputtering depth(b)[19]](2020年05期/pic38.jpg)
![图9 根据HS-LEIS计算出的5%Pd0.97Au/TiO2表面Pd/Au原子比随着H2还原温度的变化[19]<br/>Fig.9 Atomic ratio of Pd/Au as a function of the reduction temperature for the 5%Pd0.97Au/TiO2,which reduced by H2 and characterized by HS-LEIS[19]](2020年05期/pic39.jpg)
![图 10 分别经过450 ℃氧化和500 ℃还原后,TiO2负载和非负载PdxAuy催化剂表面-体相Pd/(Pd+Au)原子比(HS-LEIS)的变化相图[19]<br/>Fig.10 Phase diagrams of surface atomic ratio of Pd/(Pd+Au)(HS-LEIS)as a function of the bulk value for both supported and unsupported PdxAuy catalysts after oxidation at 450 ℃ and reduction at 500 ℃[19]](2020年05期/pic40.jpg)
![图 11 不同预处理后5%Pd0.97Au/TiO2(a)和500 ℃预还原后不同组成的5%PdxAuy/TiO2(b)催化CO氧化的活性,以及90 ℃时不同成5%PdxAuy/TiO2催化CO反应的TOF对最表层Pd/(Pd+Au)原子比作图(c)[19]<br/>Fig.11 Oxidation activity of CO catalyzed by 5%Pd0.97Au/TiO2 under different pretreatment(a)and 5%PdxAuy/TiO2 which prereduced under 500 ℃(b), CO TOF as a function of the surface atomic ratio of Pd/(Au+Pd)for 5%PdxAuy/TiO2 react at 90 ℃(c[19]](2020年05期/pic41.jpg)
![图 12 PtCux/TiO2催化剂(a)和PtCux催化剂(b)的表面-体相组成相图[35]<br/>Fig.12 Phase diagrams of the surface composition versus the bulk composition for PtCux/TiO2 catalyst(a),and PtCux catalyst(b)[35]](2020年05期/pic42.jpg)
![图 13 Pt-Fe(OH)x/TiO2(a)和Pt-FeNi(OH)x/TiO2(b)的HS-LEIS谱图[39]<br/>Fig.13 HS-LEIS spectra of the Pt-Fe(OH)x/TiO2(a)and Pt-FeNi(OH)x/TiO2(b)[39]](2020年05期/pic43.jpg)
![图 14 Pt/C和Pt@h-BN/C-700催化剂的HS-LEIS谱图[41]<br/>Fig.14 HS-LEIS spectra of Pt/C and Pt@h-BN/C-700 catalysts[41]](2020年05期/pic44.jpg)
![图 15 PtRu/C和PtRu@h-BN/C 催化剂的HS-LEIS谱图(a),PtRu@h-BN/C催化剂的HRTEM图(b)、XPS N-1s(c)和B-1s(d)谱图[42]<br/>Fig.15 HS-LEIS spectra of the PtRu/C and PtRu@h-BN/C catalysts(a), HRTEM images(b), XPS N-1s(c)and B-1s(d)spectra of the PtRu@h-BN/C catalyst[42]](2020年05期/pic45.jpg)
