(1.厦门大学化学化工学院,醇醚酯化工清洁生产国家工程实验室,福建 厦门 361005; 2.中海油天津化工研究设计院有限公司,天津 300131)
1,4-丁炔二醇; 1,4-丁二醇; 加氢; Pd-Ni 基催化剂; 碳纳米管
(1.National Engineering Laboratory for Green Chemical Productions of Alcohols-Ethers-Esters,College of Chemistry and Chemical Engineering,Xiamen University,Xiamen 361005,China; 2.CenerTech Tianjin Chemical Research and Design Institute Co.,Ltd.,Tianjin 300131,China)
1,4-butynediol; 1,4-butanediol; hydrogenation; Pd-Ni based catalysts; carbon nanotubes(CNTs)
DOI: 10.6043/j.issn.0438-0479.201811046
备注
鉴于1,4-丁炔二醇加氢制1,4-丁二醇的生产工艺一般涉及高压高温,分别以α-Al2O3和碳纳米管(CNTs)为载体,研究了近室温(30 ℃)近常压(0.2 MPa)下1,4-丁炔二醇的Pd(Ni)基催化剂的加氢性能及其结构特征.结果发现,Pd-Ni双金属催化剂可以实现1,4-丁炔二醇的完全转化.对于产物1,4-丁二醇的选择性,还原法制备的1%Pd-1%Ni/CNTs仅达60.6%,而分步浸渍法制备的1%Pd-1%Ni/α-Al2O3和1%Pd-1%Ni/CNTs则分别达到89.1%和98.9%.X射线衍射(XRD)、氢气程序升温还原(H2-TPR)及透射电镜(TEM)等表征结果表明:具有合适相互作用、合金形式(部分)以及高度分散的Pd-Ni物种对1,4-丁炔二醇加氢具有重要作用,有利于反应中间产物1,4-丁烯二醇进一步加氢至1,4-丁二醇; 且CNTs具有较优的储氢能力,以CNTs为载体有利于提高Pd-Ni基催化剂表面的氢浓度,进而促进1,4-丁烯二醇加氢.
The production of 1,4-butanediol(BDO)from 1,4-butynediol(B3D)is usually under high pressure and high temperature.In this study,the hydrogenation properties and structural characteristics of the Pd(Ni)based catalysts supported on α-Al2O3 and carbon nanotubes(CNTs)respectively for B3D hydrogenation were investigated under close to room temperature(30 ℃)and atmospheric pressure(0.2 MPa).The results demonstrate that B3D hydrogenation can be completely converted with Pd-Ni bimetallic catalysts.Selectivity of BDO just achieved 60.6% for 1%Pd-1%Ni/CNTs synthesized with chemical reduction method,while it increased to 89.1% and 98.9% for 1%Pd-1%Ni/α-Al2O3 and 1%Pd-1%Ni/CNTs catalysts prepared with stepwise impregnation method.The characterization results from X-ray diffraction(XRD),hydrogen temperature-programmed reduction(H2-TPR)and transmission electron microscope(TEM)show that the high-dispersed Pd-Ni species,partially composed of alloy and with suitable interactions,play a vital role in B3D hydrogenation, and improve the ability of hydrogenation of 1,4-butenediol(B2D)to BDO.Besides,the CNTs with excellent hydrogen-storage performance,when used as supports,lead to the increase of hydrogen species concentration on the surface of Pd-Ni based catalyst,and promote the hydrogenation of B2D to BDO.
引言
1,4-丁二醇(BDO)是一种应用广泛的有机和精细化工原料,可以生产聚氨酯树脂、聚对苯二甲酸丁二醇酯、聚四亚甲基乙二醇醚等产品,是医药、化工等工业不可或缺的基本有机原料[1].截至2017年2月,全球BDO总产能为399万t,而中国大陆的产能已达207.9万t.BDO生产技术主要源于巴斯夫、三菱化学、国际特品公司(ISP)等[2].
目前,BDO的生产工艺包括炔醛法(又称为Reppe法)[1,3-5]、丁二烯法[6]、环氧丙烷(丙烯醇法)[7]以及顺酐法[8].鉴于我国“多煤”的能源特点,国内的 BDO 生产工艺大部分采用以乙炔和甲醛为原料的炔醛法,其中1,4-丁炔二醇(B3D)加氢制BDO是炔醛法的重要过程之一.原有的生产工艺中,粗B3D溶液加氢制备BDO的反应压强高达30 MPa,反应温度为70~140 ℃[3].该法存在乙炔分压高易引起爆炸及乙炔易聚合导致催化剂失活等缺点.后续改良的炔醛法主要有BASF工艺、Linde/Yukong工艺、ISP工艺、INVISTA工艺以及国内山西三维改进的Reppe法工艺[1].这些工艺均采用高压工艺(12~33 MPa)和雷尼Ni或负载型的Ni基催化剂,反应温度一般在100~200 ℃.
悬浮床或淤浆床反应工艺一般采用雷尼Ni催化剂.该催化剂通过不完全碱处理提高其机械强度,可用于高温、高压的固定床反应器[2].随后,人们尝试往雷尼Ni催化剂中添加第二组分(如Cu、Mo、Cr)以提高B3D的加氢速率及BDO的选择性[9-11].负载型的Ni基催化剂也广泛用于B3D二段加氢工艺中.GAF公司开发了以Al2O3、活性炭、硅酸镁、硅铝氧化物等为载体的Ni/Cu/Mn催化剂[12-13].BASF公司开发了以Al2O3和SiO2为复合载体,添加Ni、Cu、Mn、Al等至少一种元素作为活性组分的高温高压加氢催化剂[14].ISP工艺中采用γ-Al2O3负载的Ni/Cu/Mn催化剂,并应用于该工艺中的二段高压加氢[15].可见,B3D 加氢制BDO主要集中于Ni 基催化剂,而贵金属如Pd基催化剂的加氢产物多涉及1,4-丁烯二醇(B2D)的合成[4].
综上,B3D加氢过程,特别是二段加氢工艺,往往涉及高压反应,且技术多依赖国外大公司.本研究根据B3D加氢反应的特点,分别以碳纳米管(CNTs)和α-Al2O3为载体,以贵金属-非贵金属为催化剂的活性组分,研究催化剂的构效关系,以期开发反应条件温和且高效的加氢催化剂.
1 实验部分
2 结果与讨论
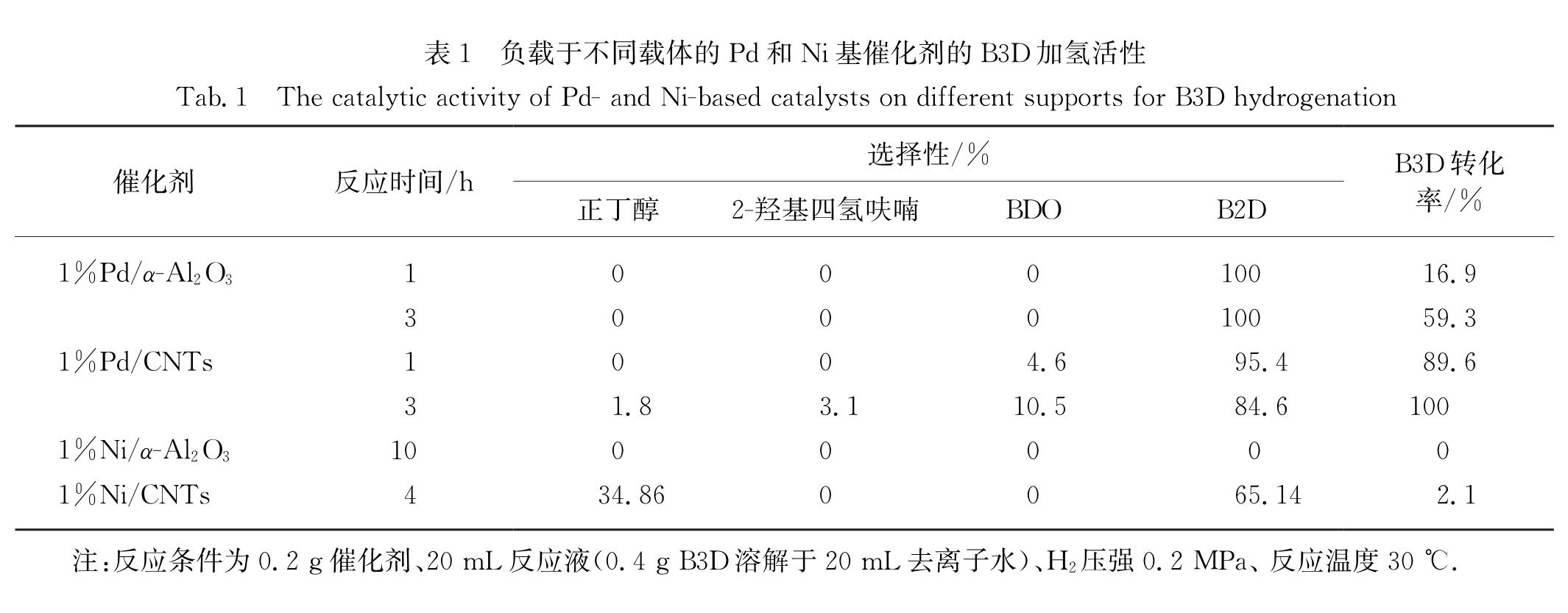
2.1 单金属催化剂的加氢活性分别以α-Al2O3和CNTs为载体,采用常规浸渍法制备的单金属催化剂对B3D的加氢反应性能如表1所示:在反应温度为30 ℃,H2压强为0.2 MPa下反应1和3 h后,1%Pd/α-Al2O3催化剂对B3D的转化率分别为16.9%和59.3%,且反应产物停留在B2D; 而1%Pd/CNTs则可以较快地对B3D完全加氢,在反应1 h 后B3D的转化率达到89.6%,反应3 h后可以实现完全转化,尽管反应产物含有B2D进一步加氢的产物BDO,但是BDO的选择性仍有待提高.而单金属Ni基催化剂则几乎没有活性.
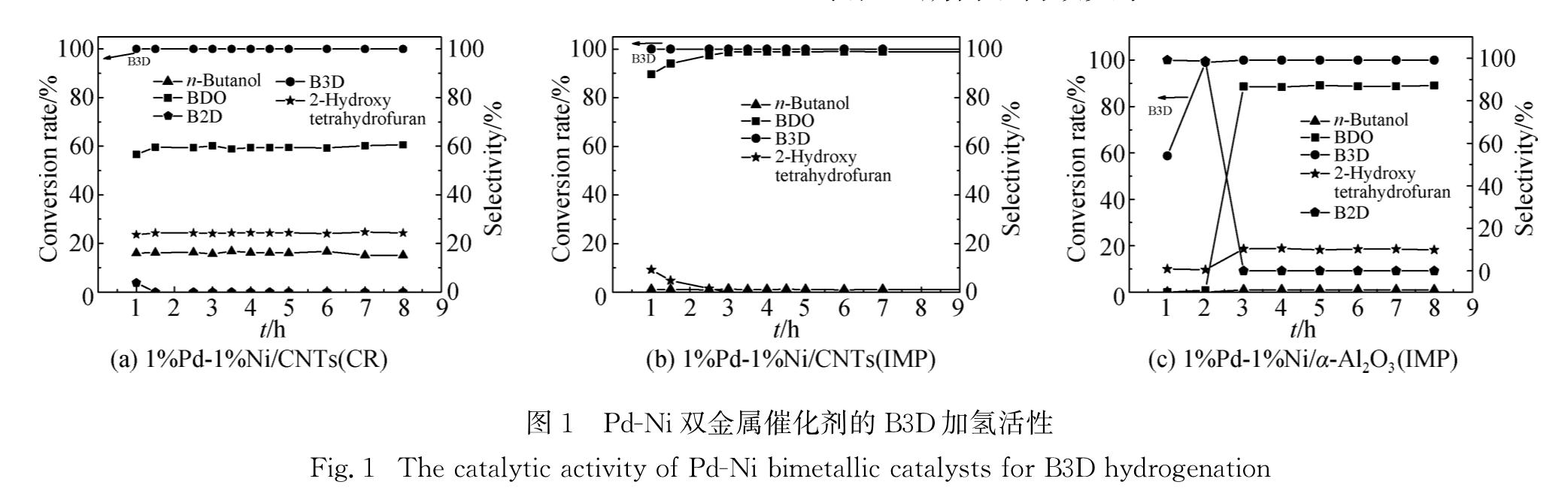
2.2 Pd-Ni双金属催化剂的加氢活性对所制备的1%Pd-1%Ni/CNTs(IMP)和1%Pd-1%Ni/CNTs(CR)进行活性评价,结果(图1)表明:1%Pd-1%Ni/CNTs(CR)在反应1 h后实现了B3D的完全加氢转化,BDO的选择性达到56.6%; 反应1.5 h后产物分布基本保持稳定,其中BDO、2-羟基四氢呋喃、正丁醇的选择性范围分别为58.9%~60.6%,24.0%~24.7%,15.1%~16.8%,此时BDO的选择性仍较低.分步浸渍法制备的1%Pd-1%Ni/CNTs(IMP)催化剂同样在反应1 h后实现了B3D的完全加氢转化,而且在反应3 h后BDO的选择性可以达到98.9%,且副产物仅有1.29%的正丁醇.
为了便于比较,本研究还制备了1%Pd-1%Ni/α-Al2O3(IMP).结果表明,该催化剂的加氢活性稍弱,反应1 h后仅实现了B3D的部分转化,转化率为58.8%; 反应3 h后其产物分布也基本保持稳定,但此时的BDO选择性最高为89.1%(图1).可见,无论是CNTs还是α-Al2O3负载的Pd-Ni基催化剂,其催化加氢活性均优于单金属Pd基催化剂; 而且载体以CNTs为佳,制备方法以分步浸渍法为优.下面进行相应的表征以期揭示构效关系.
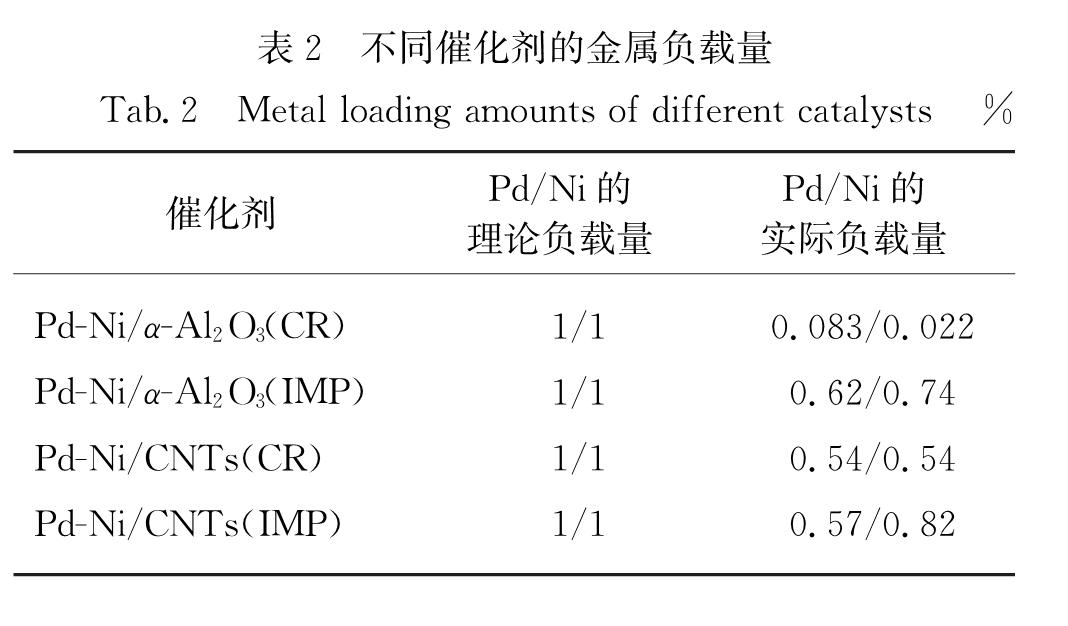
2.3 催化剂的组成及载体的织构特征利用ICP对所制备的双金属催化剂进行金属负载量(质量分数)的测定,结果如表2所示.可以看出实际负载量低于理论负载量,尤其是在α-Al2O3载体上用还原法基本无法实现Pd负载,CNTs载体上分步浸渍法和还原法的Pd负载量基本接近,采用分步浸渍法制备的催化剂上Ni的负载量较高.
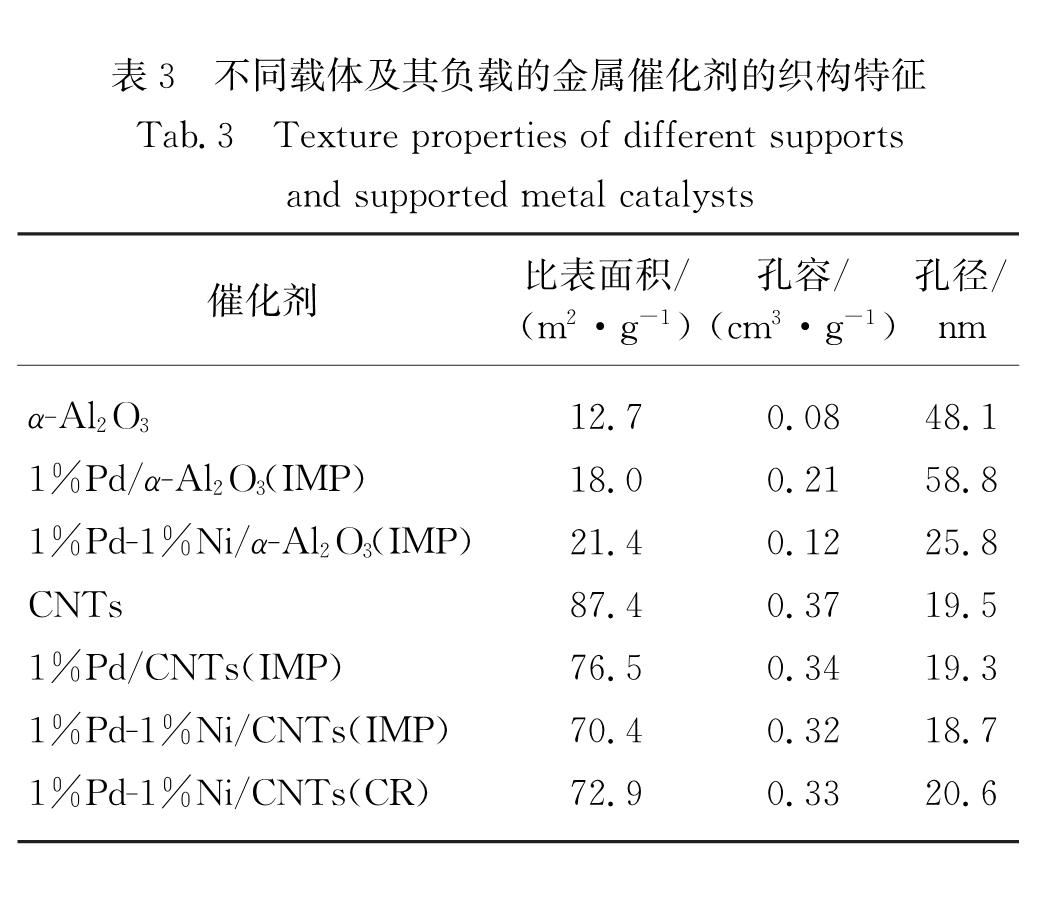
以氮气吸脱附实验表征α-Al2O3和CNTs负载金属催化剂的织构特征.结果(表3)发现,尽管α-Al2O3的比表面积和孔容较小,但它和CNTs均存在较大的介孔; 负载金属后的催化剂与载体相比,α-Al2O3载体的比表面积、孔容和孔径均发生了明显变化,而CNTs
载体的织构特征变化不大.结合金属负载量较低(仅1%),可以推测上述两种载体对反应物和产物的扩散影响较弱.
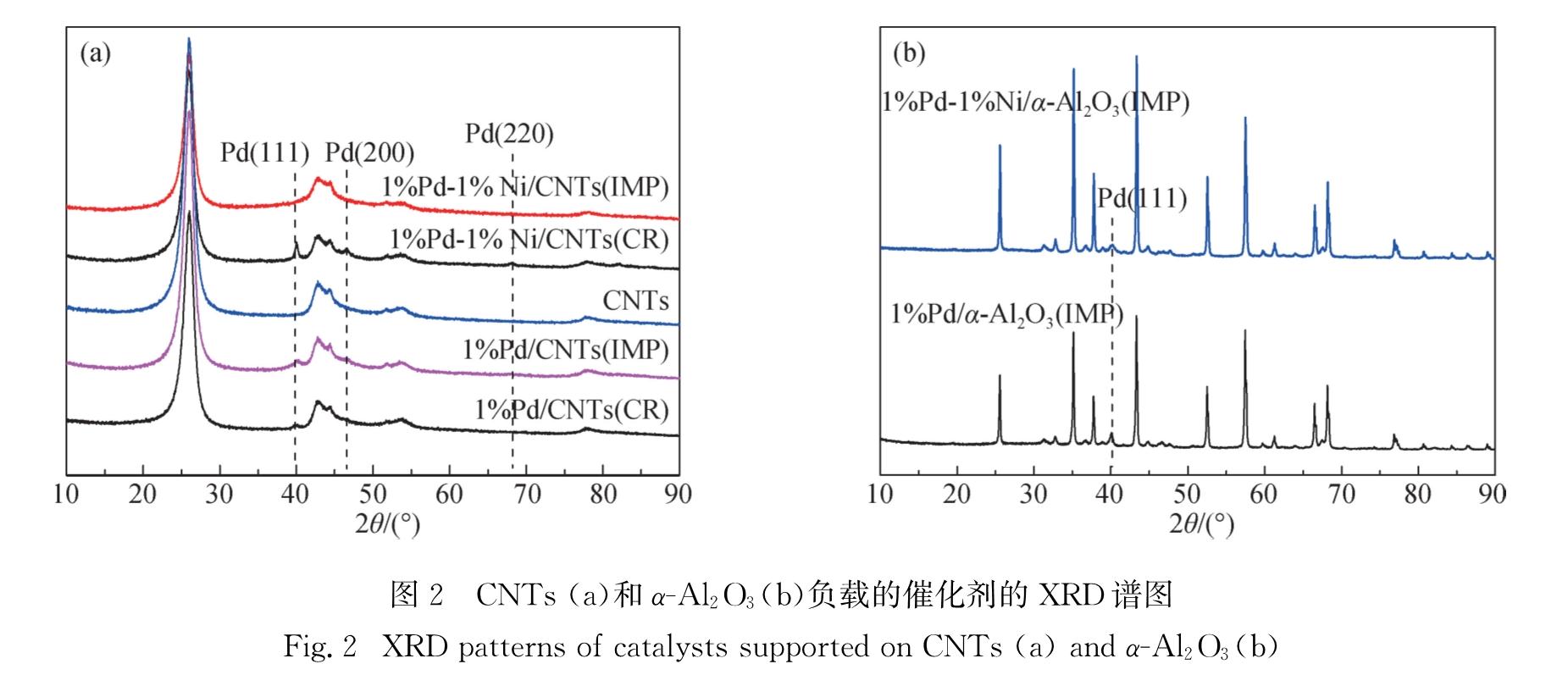
2.4 催化剂的晶相特征图2为单、双金属催化剂的XRD谱图.所有催化剂均在300 ℃、V(H2):V(N2)=1:9的气氛下进行了预还原.根据已有文献报道,2θ为44.4°,51.7°,76.3°的特征衍射峰分别对应Ni(111)、Ni(200)和Ni(220)晶面,而2θ为37.0°,42.9°,62.1°的特征衍射峰分别对应NiO(111)、NiO(200)和NiO(220)晶面[17]; 2θ为40.1°,46.3°,68.2°的特征衍射峰则分别对应Pd(111)、Pd(200)和Pd(220)晶面[18].根据谢乐公式计算结果发现,1%Pd/α-Al2O3(IMP)的Pd金属粒径(17.5 nm)相对较大,这可能与其比表面积较小有关; 而1%Pd/CNTs(IMP)的金属粒径则较小,约2.7 nm.
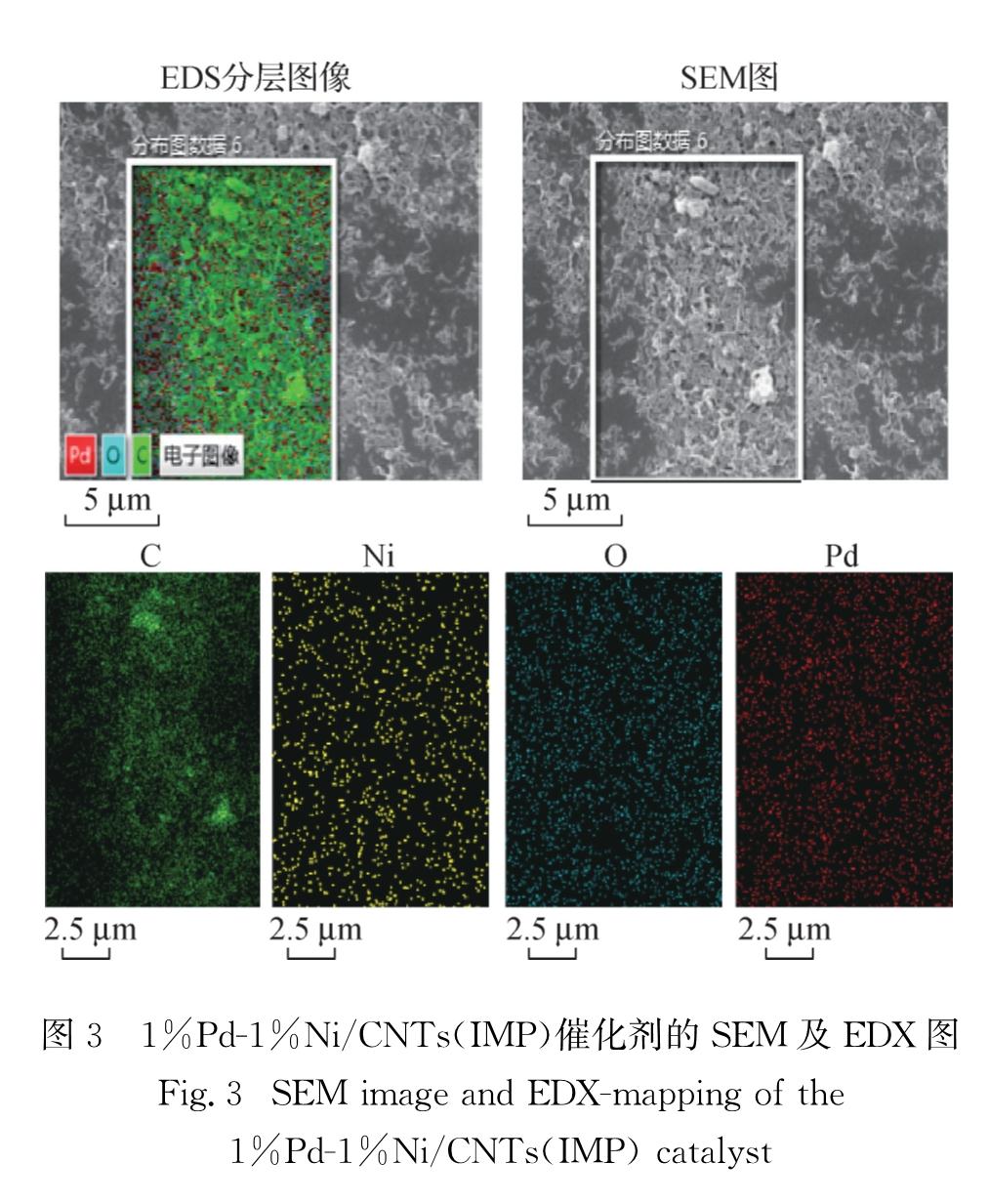
由图2(a)可见:1%Pd/CNTs(IMP)、1%Pd/CNTs(CR)和1%Pd-1%Ni/CNTs(CR)催化剂均存在Pd(111)、Pd(200)、Pd(220)晶面对应的特征衍射峰; 而1%Pd-1%Ni/CNTs(IMP)催化剂并没有发现任何对应于Pd金属各晶面的特征衍射峰,这说明Pd金属颗粒在该催化剂表面均匀分散.此外,1%Pd-1%Ni/CNTs(CR)和1%Pd-1%Ni/CNTs(IMP)催化剂均没有发现明显的Ni金属组分的特征衍射峰,说明Ni金属组分在催化剂表面均匀分散.这与1%Pd-1%Ni/CNTs(IMP)催化剂SEM的EDX分析结果一致(图3).对比1%Pd-1%Ni/CNTs(CR)和1%Pd-1%Ni/CNTs(IMP)的特征衍射峰强弱可以发现,不同方法(分步浸渍法和还原法)负载Ni组分会造成Pd金属分散度上的差异.与还原法制备的Pd-Ni双金属催化剂相比,分步浸渍法制备的Pd-Ni双金属催化剂上Pd和Ni的分散更均匀,其金属分散度有较大的提高.
由图2(b)可见, 1%Pd-1%Ni/α-Al2O3(IMP)和1%Pd/α-Al2O3(IMP)催化剂均在2θ为40.09°处出现了Pd(111)的特征衍射峰,且单金属催化剂的衍射峰强度要大于双金属的衍射峰强度,这说明单金属催化剂的Pd晶粒尺寸大于双金属催化剂,后者的金属分散性优于前者.显然,1%Pd-1%Ni/α-Al2O3(IMP)催化剂上Pd的分散性不如1%Pd-1%Ni/CNTs(IMP)催化剂上.结合图1(b)和图1(c)的活性结果,可以推测Pd、Ni组分的分散及相互作用会影响BDO的选择性.因此,下面针对Pd和Ni组分的相互作用进一步表征.
图2 CNTs(a)和α-Al2O3(b)负载的催化剂的XRD谱图
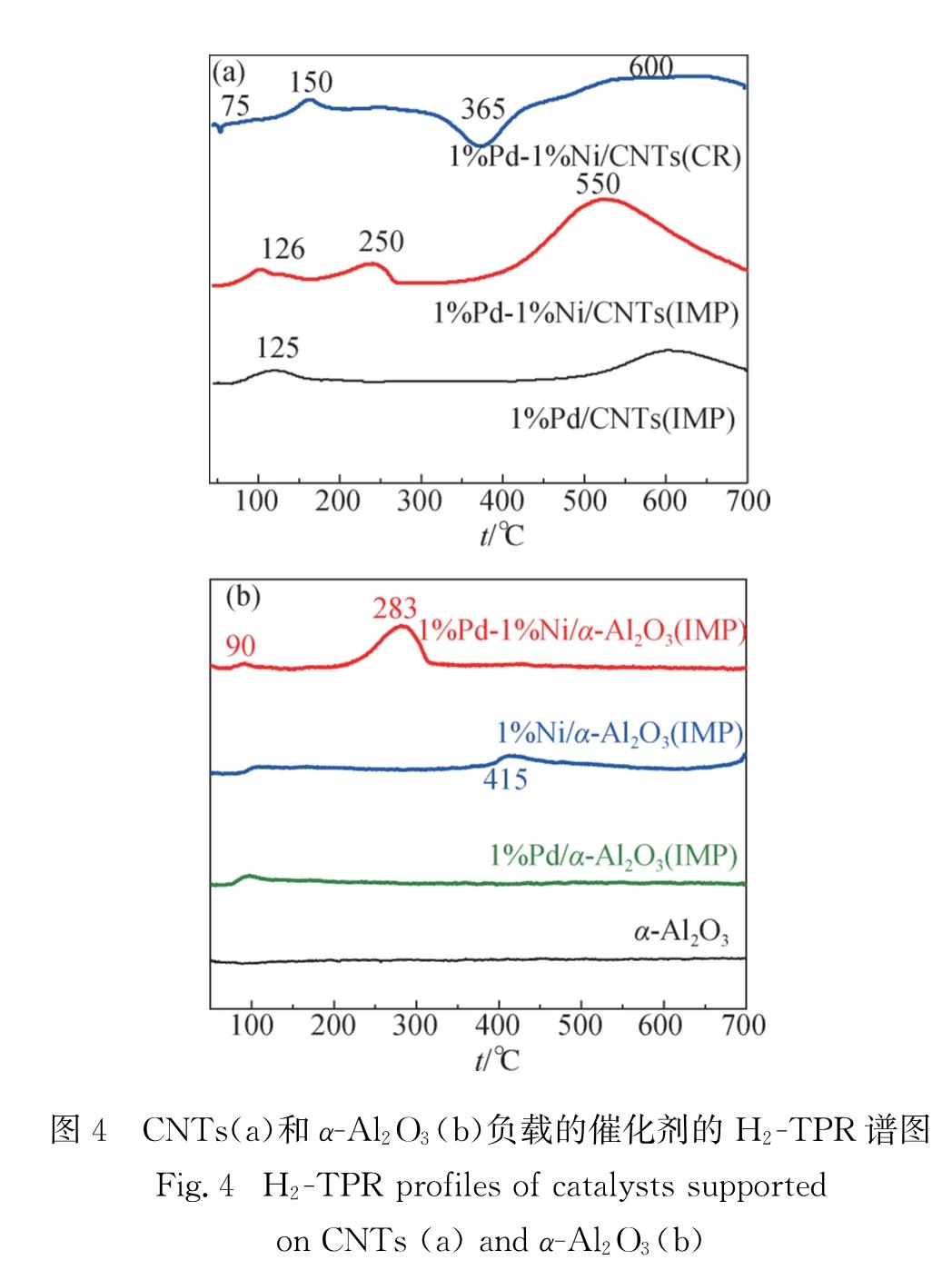
Fig.2 XRD patterns of catalysts supported on CNTs(a)and α-Al2O3(b)2.5 催化剂的还原性能及金属特征图4为催化剂的H2-TPR表征结果.可以看到,还原法制备的1%Pd-1%Ni/CNTs(CR)催化剂存在4个特征峰:位于75 ℃的倒峰归属为有利于完全加氢的β-PdH物种的分解峰[18-19]; 位于150 ℃的特征峰归属为PdO或NiO物种由于氢溢流效应的还原峰; 由于CNTs载体是一种较优的储氢材料,经过离子处理能提高CNTs在温和条件下的吸附储氢量,所以位于365 ℃的倒峰很有可能是由于CNTs存在带来的氢气反溢流现象; 而600 ℃的特征峰则可能是CNTs加氢生成甲烷反应形成的 [20-22].
分步浸渍法制备的1%Pd-1%Ni/CNTs(IMP)催化剂存在3个明显的还原峰,分别位于126,250和550 ℃.同样地,高温区550 ℃的特征峰可能是由于CNTs加氢生成甲烷反应形成[20-22]; 而PdO转化成 Pd0的还原温度在126 ℃左右[18,23-26]; 同时NiO的还原温度向低温区偏移,即NiO还原峰峰顶温度从300 ℃以上[18]移至250 ℃附近.分步浸渍法制备的1%Pd-1%Ni/α-Al2O3(IMP)催化剂于283 ℃处也存在1个强还原峰,与1%Ni/α-Al2O3(IMP)催化剂相比,其NiO的还原峰从415 ℃移至283 ℃.因此,可以
图4 CNTs(a)和α-Al2O3(b)负载的催化剂的H2-TPR谱图
Fig.4 H2-TPR profiles of catalysts supported on CNTs(a)and α-Al2O3(b)推测1%Pd-1%Ni/CNTs(IMP)和1%Pd-1%Ni/α-Al2O3(IMP)催化剂的Pd与Ni金属组分之间存在相互作用或形成合金[18,22-23].
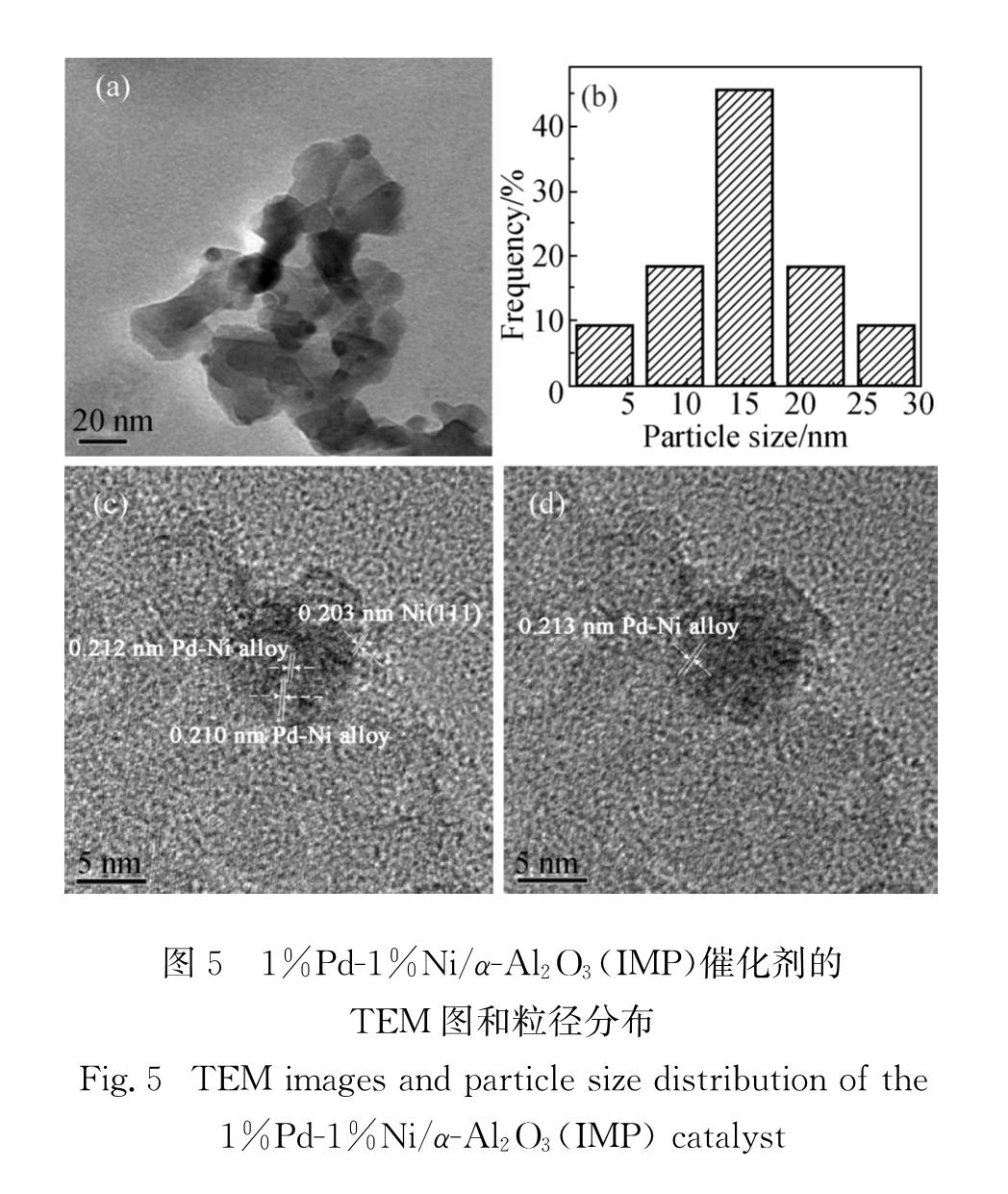
为此,对1%Pd-1%Ni/CNTs(IMP)和1%Pd-1%Ni/α-Al2O3(IMP)催化剂进行TEM表征.由于CNTs的干扰,1%Pd-1%Ni/CNTs(IMP)难以拍到高分辨的金属颗粒,无法精确统计其表面金属离子的粒径分布情况,所以未给出其TEM图.但从图3可以看出1%Pd-1%Ni/CNTs(IMP)催化剂的Pd和Ni物种都均匀分散.从图5可以看出1%Pd-1%Ni/α-Al2O3(IMP)催化剂的平均粒径为14.3 nm,并且从高分辨率的TEM图观测到,其存在间距为0.203~0.213 nm的晶格条纹.根据催化剂的金属组分,可以判定分步浸渍法制备的Pd-Ni基催化剂确实存在Pd-Ni合金相.
图5 1%Pd-1%Ni/α-Al2O3(IMP)催化剂的TEM图和粒径分布
Fig.5 TEM images and particle size distribution of the 1%Pd-1%Ni/α-Al2O3(IMP)catalyst2.6 构效关系分析1%Pd-1%Ni/CNTs(IMP)催化剂在100%转化率的条件下,BDO的选择性可以达到98%以上; 而1%Pd-1%Ni/CNTs(CR)催化剂在同等条件下产物BDO的选择性仅能达到59%左右.结合二者的XRD和H2-TPR结果,1%Pd-1%Ni/CNTs(IMP)催化剂中Pd-Ni双金属间的相互作用、合金形式及高分散性影响Pd-Ni物种的电子状态,有利于增强对底物B3D和中间产物B2D的吸附,以避免其他副反应的发生[27-29].Kesmodel等[30]研究发现催化剂多位点或高压的反应过程有利于产生含碳中间体物种,该物种由于易转化而难以直接检测,普遍认为其有利于三键直接加氢生成单键产物.而本研究以α-Al2O3为载体制备的Pd-Ni双金属催化剂的催化活性及结构表征也表现出类似的结果.
1%Pd/α-Al2O3(IMP)和1%Pd-1%Ni/α-Al2O3(IMP)均能够快速转化B3D(表1和图1(c)).根据产物分布可知,1%Pd/α-Al2O3(IMP)不能实现B2D 的进一步加氢,而1%Pd-1%Ni/α-Al2O3(IMP)则可以在B2D产物的选择性接近100%时将B2D进一步转化为BDO,尽管BDO的选择性最高仅为89.1%.这说明Pd-Ni双金属间的相互作用及部分合金形式有利于第一步加氢产物B2D的进一步转化.
根据上述分析可知,采用分步浸渍法制备的双金属催化剂均能够将B3D完全转化,其中以CNTs为载体的催化剂BDO选择性高达98.9%,而以α-Al2O3为载体的催化剂BDO选择性仅有89.1%,这说明CNTs载体确实有利于B2D向BDO转化.文献[31-34]的研究结果表明氢浓度(或者分压)的增加有助于提高反应速率以及加氢产物的生成,而CNTs较好的储氢能力则有利于提高催化剂表面的氢浓度,从而有助于加氢产物的生成,提高催化剂的加氢活性.可见,由于CNTs具有较优异的储氢性能,CNTs负载的高度分散的Pd(Ni)物种对B3D或B2D的反应速率大幅提高,即在动力学上有利于完全加氢产物BDO的生成[35].这也进一步说明催化剂表面的氢浓度对B3D完全加氢形成BDO具有重要影响[34-35].结合1%Pd-1%Ni/CNTs(CR)的加氢活性数据可知,高分散的Pd-Ni活性组分可能与CNTs起协同作用.
3 结 论
本研究分析了B3D低温低压高效加氢催化剂Pd-Ni/α-Al2O3和Pd-Ni/CNTs的催化性能和结构特征.在反应温度为30 ℃,H2压强为0.2 MPa的条件下,1%Pd-1%Ni/CNTs(IMP)催化剂能够在1 h内实现B3D的完全转化,并且反应3 h后产物BDO的选择性稳定在98%以上.
表征结果表明,Pd-Ni双金属间的相互作用及合金形式有利于第一步加氢产物B2D的进一步转化.这可能是由于Pd-Ni物种电子状态发生改变,有利于增强对底物B3D和中间产物B2D的吸附,避免了其他副反应的发生.而CNTs载体具备较优的储氢性能,使其负载的高度分散的Pd(Ni)物种对B3D或B2D的反应速率大幅提高,即在动力学上有利于完全加氢产物BDO的生成.将本研究中反应条件温和、高效的加氢催化剂应用于B3D加氢过程,可以显著降低加氢工艺(如现有二段加氢工艺)在高压方面的苛刻要求.
1.1 试 剂水合肼、氯化钯(PdCl2)、氯化镍(NiCl2)和氢氧化钠(NaOH)均为分析纯试剂,购自国药集团化学试剂有限公司; α-Al2O3和B3D均为分析纯试剂,购自上海阿拉丁生化科技股份有限公司; CNTs为实验室自制; H2、N2和Ar纯度均为99.999%,购自林德气体(厦门)有限公司.
1.2 催化剂的制备1.2.1 单金属催化剂采用常规浸渍法制备单金属Pd基催化剂:分别称取2 g的α-Al2O3和CNTs固体粉末,各加入适量PdCl2溶液(pH=1~2),搅拌1 h后过滤、烘干,在500 ℃马弗炉中焙烧,制得相应的催化剂,分别记为1%Pd/α-Al2O3和1%Pd/CNTs.反应前催化剂在氢气气氛、300 ℃下还原3 h.
1.2.2 双金属催化剂采用分步浸渍法制备Pd-Ni双金属催化剂:取2 g CNTs或α-Al2O3固体粉末加入适量的 NiCl2溶液,超声15 min,60 ℃下烘干即得1%Ni/CNTs(IMP)或1%Ni/α-Al2O3(IMP); 取适量PdCl2溶液(pH=1~2),加入2 g 1%Ni/CNTs(IMP)或1%Ni/α-Al2O3(IMP)固体粉末,超声15 min,60 ℃下烘干,置于反应炉中在V(H2):V(N2)=1:9混合气中300 ℃下进行还原预处理,升温速率为2 ℃/min,制得的催化剂分别记为1%Pd-1%Ni/CNTs(IMP)和1%Pd-1%Ni/α-Al2O3(IMP).
采用化学还原和化学置换结合的方法[16](下文简称还原法),制备Pd-Ni双金属催化剂:取2.5 g 载体(α-Al2O3或CNTs)于锥形瓶中,加所需量的水、NaOH和25 mL水合肼,搅拌1 h后加入所需量的NiCl2溶液,搅拌1 h后过滤、烘干; 然后加入适量PdCl2溶液,搅拌1 h后过滤、60 ℃下烘干6 h,在V(H2):V(N2)=1:9的混合气中300 ℃下焙烧3 h,制得的催化剂分别记为1%Pd-1%Ni/α-Al2O3(CR)和1%Pd-1%Ni/CNTs(CR).上述金属比例均为投料质量分数,实际质量分数通过电感耦合等离子体发射光谱(ICP)测定.
1.3 催化剂的评价方法以75 mL耐压反应釜为评价装置来测试催化剂的加氢活性:取0.4 g 淡黄色B3D片状固体溶于20 mL 去离子水,加入0.2 g催化剂,控制相应的反应温度、H2压力,每隔0.5 h取样1次.反应产物用岛津公司气相色谱仪(GC 2014C)的火焰离子检测器(FID)进行分析.B3D的转化率以及产物B2D和BDO的选择性计算公式如下:
X=(∑nifiAi)/(fB3DAB3D+∑nifiAi)×100%,(1)
SB2D=(fB2DAB2D)/(∑nifiAi)×100%,(2)
SBDO=(fBDOABDO)/(∑nifiAi)×100%.(3)
其中,X为B3D的转化率,SB2D和SBDO分别为B2D和BDO的选择性,A为各物种的峰面积,f为校正因子,i为产物,n为产物总个数.
1.4 催化剂的物化性能表征样品的物相结构分析在Rigaku公司的Ultima Ⅳ X射线衍射(XRD)仪上完成,Cu靶,Kα辐射,工作电压35 kV,工作电流20 mA,扫描速度10(°)/min,扫描范围10°~90°; 以Micromeritics公司的TriStar Ⅱ 3020自动物理吸附仪(氮气吸脱附)测定催化剂的织构特征; 利用Micromeritics公司的Auto Chem Ⅱ 2920自动程序升温化学吸附仪,在V(H2):V(Ar)=5:95气氛下进行氢气程序升温还原(H2-TPR),分析催化剂的氧化还原特性.使用日本电子株式会社的JEM1400透射电镜(TEM)获取催化剂的颗粒尺寸、形貌与晶格参数等信息,加速电压为300或200 kV.使用日本电子株式会社的JEM2100F TEM配备的扫描透射电镜(STEM)模式,采集明像场和暗像场,并配合能谱(EDX)实现微区元素分析.
- [1] 陈海红.1,4-丁二醇生产工艺及其技术进展[J].精细石油化工进展,2014,15(1):46-49,58.
- [2] 华烁科技股份有限公司.煤制1,4-丁二醇新技术及衍生物应用展望[C]∥2017煤基含氧化学品及衍生物发展论坛.义马:中国石油和化学工业联合会,2017:54-57.
- [3] REPPE W,STEINHOFER A,SPAENIG H,et al.Alkynols by the reaction of acetylene with aldehydes and ketones:US2300969[P].1942-08-20.
- [4] 刘响,廖启江,张敏卿.1,4-丁炔二醇加氢过程研究进展[J].化工进展,2017,36(8):2787-2797.
- [5] 王翔宇,罗平,李耀会,等.1,4-丁二醇生产工艺技术评价[J].化工设计通讯,2017,43(11):14-15.
- [6] HILES A G,TUCK M W M.PROCESS:WO1990GB01167[P].1990-07-27.
- [7] COUTEAU W,DUNGELHOEFF M L,HENDRICKX A,et al. Catalytic process for the production of butane-1,4-diol from butenedioic acid:DE2553959A1[P].1986-04-22.
- [8] TAYLOR P D,VANDERSPURT T H.1,4-Butanediol:US4083882A[P].1978-04-11.
- [9] HORT E V,GRAHAM D E.Hydrogenation of 2-butyne-1,4-diol to 1,4-butanediol:US2967893[P].1961-01-10.
- [10] HADLEY R L.Hydrogenation catalyst:US2948687[P].1960-08-09.
- [11] HORT E V,DE THOMAS W R.Raney nickel catalyst:GB2104794A[P].1983-05-13.
- [12] WETHERILL F E.1,4-Butanediol:US3449445A[P].1969-06-10.
- [13] DE THOMAS W R.Hydrogenation catalyst:EP19880304443[P].1988-05-17.
- [14] DE THOMAS W R.Hydrogenation catalysts and process for conversion of 1,4-butynediol to 1,4-butanediol:US4795733A[P].1989-08-23.
- [15] DE THOMAS W R,HORT E V.Catalyst comprising Raney nickel with adsorbed molybdenum compound:US4153578A[P].1979-05-08.
- [16] ZHU L H,CAO M H,LI L,et al.Synthesis of different ruthenium nickel bimetallic nanostructures and an investigation of the structure-activity relationship for benzene hydrogenation to cyclohexane[J].ChemCatChem,2014,6(7):2039-2046.
- [17] UL HAQ M,WEN Z,ZHANG Z Y,et al. A two-step synthesis of nanosheet-covered fibers based on α-Fe2O3/NiO composites towards enhanced acetone sensing[J].Scientific Reports,2018,8(1):1705.
- [18] DUTTA A,DATTA J.Energy efficient role of Ni/NiO in PdNi nano catalyst used in alkaline DEFC[J].Journal of Materials Chemistry A,2014,2(9):3237-3250.
- [19] LEDERHOS C R,BADANO J M,QUIROGA M E,et al.Influence of Ni addition to a low-loaded palladium catalyst on the selective hydrogenation of 1-heptyne[J].Quimica Nova,2010,33(4):816-820.
- [20] SHAH K A,TALI B A.Synthesis of carbon nanotubes by catalytic chemical vapour deposition:a review on carbon sources,catalysts and substrates[J].Materials Science in Semiconductor Processing,2016,41:67-82.
- [21] CHEN P,WU X,LIN J,et al.High H2 uptake by alkali-doped carbon nanotubes under ambient pressure and moderate temperatures[J].Science,1999,285(5424):91-93.
- [22] CHEN P,ZHANG H B,LIN G D,et al.Growth of carbon nanotubes by catalytic decomposition of CH4 or CO on a Ni-MgO catalyst[J].Carbon,1997,35(10/11):1495-1501.
- [23] ZHANG Y Y,DIAO W J,MONNIER J R,et al.Pd-Ag/SiO2 bimetallic catalysts prepared by galvanic displacement for selective hydrogenation of acetylene in excess ethylene[J].Catalysis Science & Technology,2015,5(8):4123-4132.
- [24] ZHANG Q W,LI J,LIU X X,et al.Synergetic effect of Pd and Ag dispersed on Al2O3 in the selective hydroge-nation of acetylene[J].Applied Catalysis A:General,2000,197(2):221-228.
- [25] NORONHA F B,SCHMAL M,PRIMET M,et al.Characterization of palladium-copper bimetallic catalysts supported on silica and niobia[J].Applied Catalysis A:General,1991,78(1):125-139.
- [26] MUSOLINO M G,CUTRUPI C M S,DONATO A,et al.Cis-2-butene-1,4-diol as probe for studying isomeriza-tion versus hydrogenation and hydrogenolysis reactions[J].Applied Catalysis A:General,2003,243(2):333-346.
- [27] BOND G C,MANN R S.The catalytic hydrogenation of unsaturated hydrocarbons.Part Ⅳ.The kinetics of the hydrogenation of acetylene over supported and unsupported iron,cobalt,and copper,and over some nickel-cobalt and nickel-copper alloys[J].Journal of the Chemical Society,1959.doi:10.1039/JR9590003566.
- [28] SINGH A K,XU Q.Synergistic catalysis over bimetallic alloy nanoparticles[J].ChemCatChem,2013,5(3):652-676.
- [29] LI M,ZHANG N,LONG R,et al.PdPt alloy nanoca-talysts supported on TiO2:maneuvering metal-hydrogen interactions for light-driven and water-donating selective alkyne semihydrogenation[J].Small,2017,13(23):1604173.
- [30] KESMODEL L L,DUBOIS L H,SOMORJAI G A.LEED analysis of acetylene and ethylene chemisorption on the Pt(111)surface:evidence for ethylidyne formation[J].The Journal of Chemical Physics,1979,70(5):2180-2188.
- [31] CHAUDHARI R V,PARANDE M G,RAMACHA-NDRAN P A,et al.Hydrogenation of butynediol to cis-butenediol catalyzed by Pd-Zn-CaCO3:reaction kinetics and modeling of a batch slurry reactor[J].AIChE Journal,1985,31(11):1891-1903.
- [32] FISHWICK R P,NATIVIDAD R,KULKARNI R,et al.Selective hydrogenation reactions:a comparative study of monolith CDC,stirred tank and trickle bed reactors[J].Catalysis Today,2007,128(1/2):108-114.
- [33] TELKAR M M,RODE C V,RANE V H,et al.Selective hydrogenation of 2-butyne-1,4-diol to 2-butene-1,4-diol:roles of ammonia,catalyst pretreatment and kinetic studies[J].Applied Catalysis A:General,2001,216(1/2):13-22.
- [34] WOOD J,BODENES L,BENNETT J,et al.Hydro-genation of 2-butyne-1,4-diol using novel bio-palladium catalysts[J].Industrial & Engineering Chemistry Research,2010,49(3):980-988.
- [35] 华萱,王承学.丁炔二醇加氢制1,4-丁二醇反应动力学研究[J].吉林工学院学报,1992,43(3/4):142-148.