(山西大学复杂系统研究所,疾病防控的数学技术与大数据分析山西省重点实验室,山西 太原 030006)
(Shanxi Key Laboratory of Mathematical Techniques and Big Data Analysis on Disease Control and Prevention,Complex Systems Research Center,Shanxi University,Taiyuan 030006,China)
Ca2+ oscillations; inositol 1,4,5-trisphosphate receptor; bell-shaped curve; bifurcation analysis
DOI: 10.6043/j.issn.0438-0479.201901030
备注
细胞质钙离子(Ca2+)常以浓度振荡变化的方式控制许多生理活动,内质网上的三磷酸肌醇受体(inositol 1,4,5-trisphosphate receptor,IP3R)通道是产生钙振荡的关键因素,因此研究其振荡机制具有重要意义.虽然钙振荡已被广泛建模,但大部分模型细胞质与内质网中钙振荡的范围与实验观测数据差异较大.通过整合最近的实验结果,基于IP3R通道活性对细胞质Ca2+浓度依赖的钟型曲线构建了一个新的钙振荡模型.模型结果除了可以很好地模拟实验中关于钙振荡范围的数据,还可重复多种实验现象.对模型进行参数敏感性分析后,进一步采用单参数分岔分析分别研究了两个高敏感参数,即细胞质内Ca2+缓冲蛋白的总浓度和IP3R通道激活Ca2+的解离常数(K1)对钙振荡的影响,发现它们对钙信号有相反的作用.对三磷酸肌醇(IP3)浓度和K1进行双参数分岔分析的结果表明K1对IP3能产生钙振荡的区域及其振幅有重要影响,揭示可以通过改变K1影响细胞对外界刺激的响应及其钙振荡模式.该研究有助于理解钙振荡机制,并可为后续理论研究提供框架.
Oscillations in cytosolic calcium concentration(cCa_Cyt)regulate a diverse range of cellular processes.Dynamic properties of inositol 1,4,5-trisphosphate receptor(IP3R)located on the endoplasmic reticulum are crucial for the generation of Ca2+ oscillations.Thus,it is of great interest to determine mechanisms governing such oscillations.Although Ca2+ oscillations have been modeled extensively,one major problem with almost all published models lies in that the oscillatory ranges of cCa_Cyt and calcium concentration in endoplasmic reticulum(cCa_ER)do not agree with recent experimental data.By integrating recent experimental results,a new calcium oscillation model is constructed based on bell-shaped dependence of IP3R gating on cCa_Cyt.The cCa_Cyt and cCa_ER obtained by the model lie in ranges of experimental results.In addition,the model can successfully reproduce several features described in experimental studies.After parameter sensitivity analysis of the model,the single-parameter bifurcation analysis is conducted to study the impact of two high-sensitivity parameters,i.e.,the total concentration of cytoplasmic Ca2+ binding protein and IP3R dissociation constant for activating Ca2+(K1)on Ca2+ oscillations. Results suggest that they exert an opposite effect on calcium signal.The result of two-parameter bifurcation analysis of IP3 concentration and K1 indicates that K1 plays a crucial role on the region of IP3 concentration that can generate Ca2+ oscillations and their amplitudes,revealing that K1 can affect the response of cells to external stimuli and the Ca2+ oscillatory pattern of the cells.This study not only helps to understand the mechanism of Ca2+ oscillations,but also provides a framework for subsequent theoretical research.
引言
钙离子(Ca2+)是细胞内最常用且最重要的信使分子之一[1],它常以浓度振荡变化的方式控制着几乎一切生理活动[2-3].为了产生钙振荡,内质网里的Ca2+需要进出细胞质.当细胞处于静息状态时,细胞质中游离Ca2+浓度cCa_Cyt在0.1 μmol/L左右,而内质网的Ca2+浓度cCa_ER高达约500 μmol/L[4-5].但当细胞受到外界刺激而做出响应时,内质网中的Ca2+通过位于其膜上的三磷酸肌醇受体(inositol 1,4,5-trisphosphate receptor,IP3R)通道释放到细胞质中,使cCa_Cyt升高到1~5 μmol/L[4-5],此过程为钙振荡的上升相.钙振荡的下降相主要由同样位于内质网膜上的肌浆网钙泵(sarco/endoplasmic reticulum Ca2+-ATPase,SERCA)的逆浓度梯度转运Ca2+而决定[6].修饰钙振荡的成分还包括内质网漏钙通道[7]、细胞质Ca2+缓冲蛋白[8]和线粒体[9]等.
钙振荡的重要性使得它在近30年来一直是生物学家研究的热点,而其动力学行为也引起了众多数理学家的关注[10],他们基于不同的生物学机制构建了许多经典模型.如Meyer和Stryer[11]建立的三磷酸肌醇(IP3)-Ca2+互作用模型,Goldbeter等[12]基于钙致钙释放建立的双钙库模型,Marhl等[13]考虑细胞质、内质网、线粒体以及Ca2+缓冲蛋白等4个组分构建的复杂钙振荡模型.有不少经典模型[14-16]是基于IP3R通道活性对cCa_Cyt依赖的钟型曲线(即低浓度促进通道开放,而高浓度抑制通道开放)[17-18]构建的,影响最广的当属De Young-Keizer模型[14].随后的大多数模型是以这些经典模型为基础建立的[19-22].上述模型中,除了Qi等[20]构造的钙微域模型外,其余模型的模拟结果中cCa_Cyt的峰值均小于3 μmol/L,很多甚至小于1 μmol/L[13-14,21],而cCa_ER则只有几到数十μmol/L,远小于实际观测值.
本文中利用文献[23-25]中实验机理,构建了一个基于IP3R通道活性对cCa_Cyt钟型依赖的新模型,由该模型得到的cCa_Cyt变化范围大且符合实验观测结果.该模型不仅可使人们更深入地理解钙振荡产生的机制,而且可应用到实验中使生物学家更好地解释和预测实验结果.
1 模型与方法
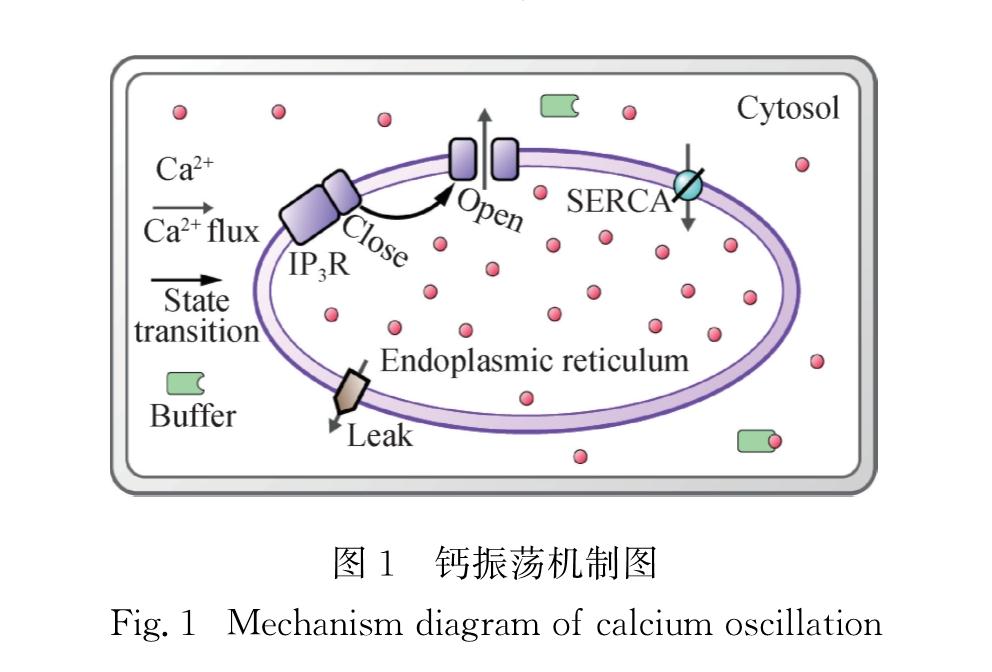
1.1 Ca2+振荡一个封闭细胞内,cCa_Cyt的变化主要由3个因素决定(图1):1)内质网中的Ca2+经IP3R通道释放到细胞质中的流量(j<sub>IP3R); 2)内质网中的Ca2+从漏钙通道渗漏到细胞质中的流量(jLeak); 3)细胞质中的Ca2+被SERCA泵入内质网的流量(jSERCA).
Ca2+由内质网流向细胞质的驱动力是它们之间的浓度差,所以
jIP3R=vIP3Rpopen(cCa_ER-cCa_Cyt),(1)
jLeak=vLeak(cCa_ER-cCa_Cyt),(2)
其中,vIP3R为IP3R通道的最大流速,vLeak为漏钙通道的渗漏速率,popen为IP3R通道的开放概率.
jSERCA常用希尔函数来描述,其希尔系数为2,代表SERCA每次可泵入2个Ca2+[26],
jSERCA=(vSERCA(cCa_Cyt)2)/((KSERCA)2+(cCa_Cyt)2),(3)
其中vSERCA为SERCA的最大流量,KSERCA为SERCA的激活常数.因此,细胞质中总的Ca2+浓度cCa_CT随时间的变化可表示为
(dcCa_CT)/(dt)=jIP3R+jLeak-jSERCA.(4)
由于细胞质与内质网中Ca2+的浓度相差上千倍,所以必须考虑Ca2+缓冲蛋白的作用才能使得cCa_Cyt和cCa_ER均达到实验测量值.细胞质中Ca2+缓冲蛋白与Ca2+的结合满足质量守恒
cCa_Cyt+cCa_B=cCa_CT,(5)
cB_f+cCa_B=cB_T.(6)
其中,cCa_B表示细胞质中与Ca2+缓冲蛋白结合的Ca2+浓度,cB_f表示细胞质中自由Ca2+缓冲蛋白的浓度,cB_T表示细胞质内Ca2+缓冲蛋白的总浓度.
因为Ca2+与Ca2+缓冲蛋白的结合很快,所以可以快速达到平衡.若Kd为解离常数,则
cCa_Cyt=(KdcCa_B)/(cB_f).(7)
由式(5)~(7)可以得到cCa_CT与cCa_Cyt的关系式
cCa_CT=cCa_Cyt(1+(cB_T)/(Kd+cCa_Cyt)).(8)
再对式(8)运用链式法则可得
(dcCa_Cyt)/(dt)=g(cCa_Cyt)(jIP3R+jLeak-jSERCA),(9)
其中函数
g(cCa_Cyt)=(1+(KdcB_T)/((Kd+cCa_Cyt)2))-1.
1.2 IP3R通道动力学IP3R通道的Ca2+流量除了与内质网和细胞质Ca2+的浓度差有关外,还与它的开放概率有关,此概率又由它所处的状态所决定,因此接下来描述IP3R通道的动力学变化.
IP3R通道是由4个亚基构成的多聚体[27],最新的研究结果表明各亚基间通过互动调节IP3R通道的构象从而控制其开关状态[25]; 因此,亚基之间并非相互独立,而是作为一个整体被调控.文献[23]假设IP3R通道有2个激活Ca2+的结合位点、2个抑制Ca2+的结合位点和1个IP3结合位点.
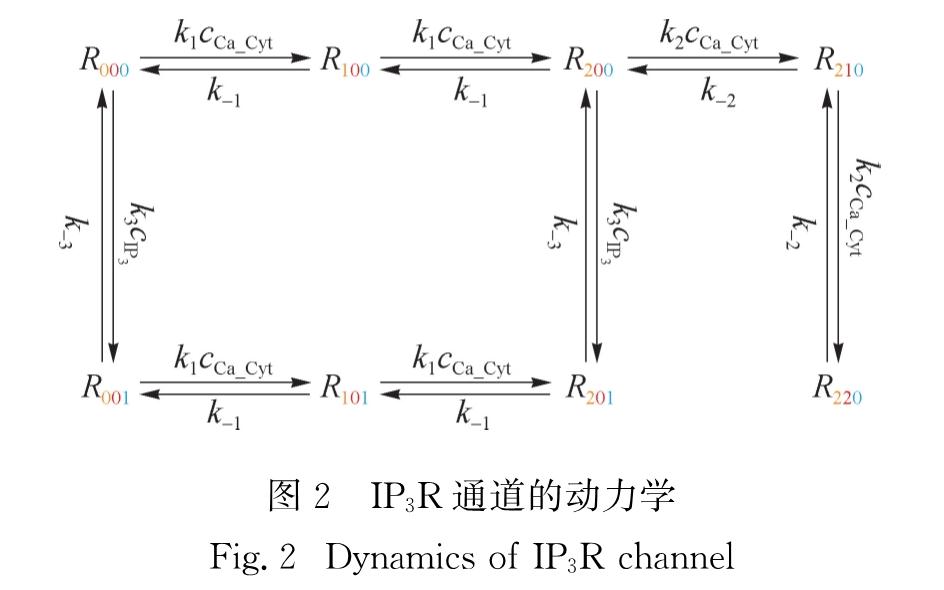
基于此,本研究构建了一个8态IP3R通道模型.如图2所示,用Rijk表示IP3R通道所处的状态,Rijk表示该状态所占的百分比,其中i表示激活Ca2+的结合位点,j表示抑制Ca2+的结合位点,k表示IP3结合位点,cIP</sub>3为细胞内IP3的浓度.根据文献[23]所述,IP3与激活Ca2+的结合是相互独立的,而IP3和抑制Ca2+的结合不能同时发生,每一类型的位点必须结合完毕才能启动其他类型位点的结合,抑制Ca2+的结合发生在激活Ca2+结合之后,且Ca2+只能逐个结合,所以8个状态所占的百分比分别为R000、R001、R101、R201、R100、R200、R210和R220.它们之间的状态转换由Ca2+和IP3的结合和解离决定,kl是结合速率常数,k-l是解离速率常数,Kl是解离常数,且Kl=k-l/kl(l=1, 2, 3).
图2 IP3R通道的动力学
Fig.2 Dynamics of IP3R channelIP3R通道各状态的变化方程为:
{(dR000)/(dt)=-v1-v7,
(dR100)/(dt)=v1-v2,
(dR200)/(dt)=v2-v5-v8,
(dR210)/(dt)=v5-v6,
(dR001)/(dt)=-v3+v7,
(dR101)/(dt)=v3-v4,
(dR201)/(dt)=v4+v8,(10)
其中,vn (n=1, 2,…,8)是关于IP3浓度cIP和cCa_Cyt的函数,其详细表达式见附录A(http:∥jxmu.xmu.edu.cn/upload/html/20190420.html).由于8个状态的和为1,故R220态的变化可由上述7态决定.
此8态中,R000和R001为低通导态,IP3结合后会诱导IP3R通道向高通导态转变,因此R101和R201是主要的开放态[23-24],其余为失活态,IP3R通道的开放概率为[23]
popen=0.075R000+0.075R001+R101+R201.(11)
1.3 IP3R通道开放概率popen可用确定性矩阵转换方法[28-29]来计算.当系统处于平衡状态时,Rijk态的百分比(xijk)均可用x000表示,如:
x001=(cIP3)/(K3)x000,(12)
x101=(cIP3cCa_Cyt)/(KK1)x000,(13)
x201=(cIP3(cCa_Cyt)2)/(K12K3)x000.(14)
将其归一化,即
qijk=(xijk)/Z,(15)
其中Z是归一化因子,
Z=∑xijk=
(1+(cIP3)/(K3)+(cCa_Cyt)/(K1)+((cCa_Cyt)2)/(K12)+(cIP3cCa_Cyt)/(K1K3)+
(cIP3(cCa_Cyt)2)/(K12K3)+((cCa_Cyt)3)/(K12K2)+((cCa_Cyt)4)/(K12K22))x000,(16)
故popen的表达式为
popen=0.075q000+0.075q001+q101+q201.(17)
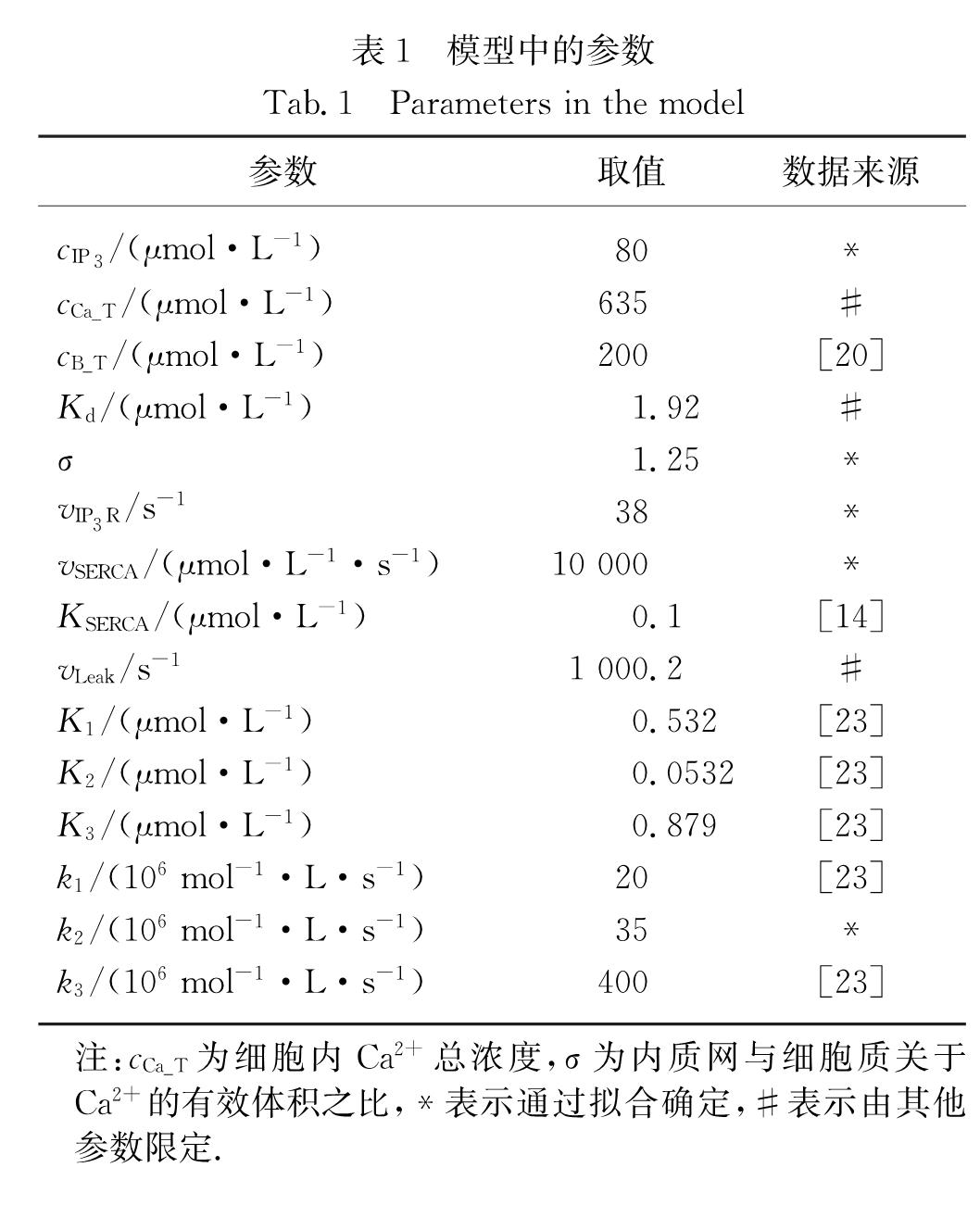
1.4 模型参数模型共有15个参数,其标准取值见表1(下文中若某参数的取值为非标准值,则在图注中说明).IP3R通道动力学所涉及的参数主要来源于文献[23],cB_T和KSERCA来源于已发表模型[14,20],其余参数由上述参数限定(附录B,http:∥jxmu.xmu.edu.cn/upload/html/20190420.html)或通过拟合实验结果[4-5,23]确定.
注:cCa_T为细胞内Ca2+总浓度,σ为内质网与细胞质关于Ca2+的有效体积之比,*表示通过拟合确定,#表示由其他参数限定.
1.5 参数敏感性分析参数敏感性分析可以确定参数对于模型结果的影响,通常采用局部敏感性系数(Slocal)来表征[30]:
Slocal=(ap)/o(Δo)/(Δap),
其中,ap为参数值,o为该值对应的钙振荡的振幅或周期,△ap和△o则分别为ap与o的变化量.Slocal>0表示参数值与钙振荡的振幅或周期呈正相关,反之呈负相关.本文中规定:若|Slocal|<1则该参数为低敏感参数,若|Slocal|>2为高敏感参数,在1~2之间为中等敏感参数.
2 结果与分析
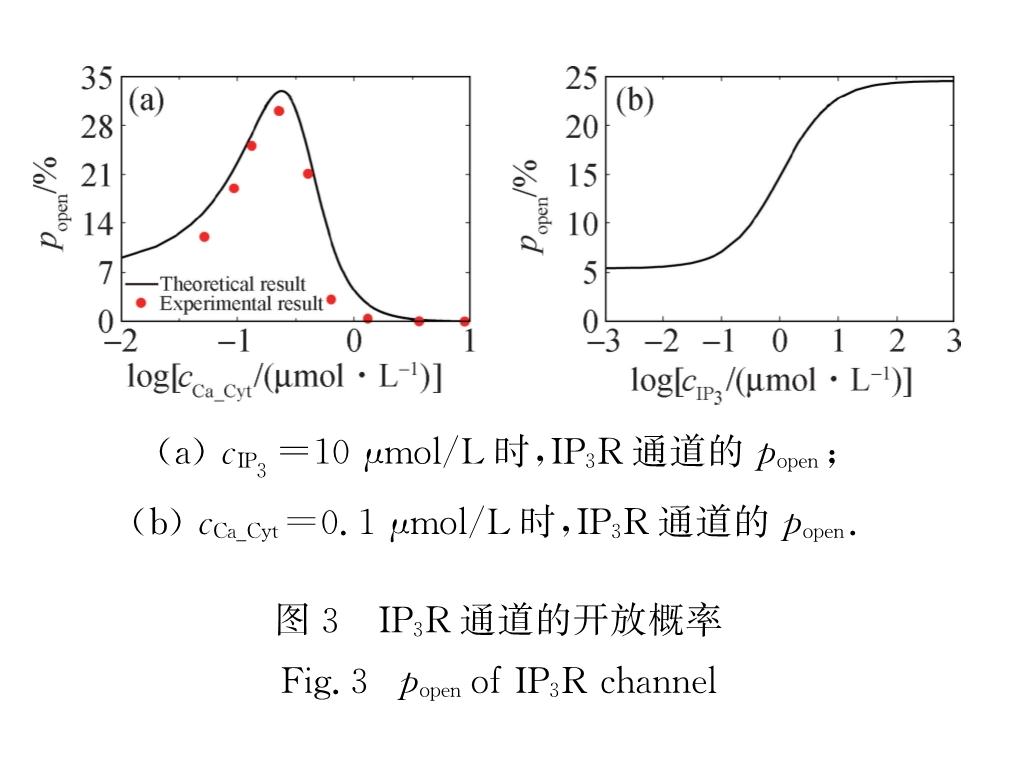
2.1 钟型曲线本研究构建的钙振荡模型的核心部分为IP3R通道8态转化动力学,它能产生IP3R通道活性对cCa_Cyt依赖的钟型曲线.图3(a)中实线表示cIP3为10 μmol/L时,由确定性矩阵转换方法计算得到的popen随cCa_Cyt变化的钟型曲线,圆点为文献[23]中的实验数据,可见理论结果与实验结果的吻合度较高.当cCa_Cyt固定在0.1 μmol/L时,计算结果(图3(b))显示随着cIP3的增加,popen先逐渐增大后基本不变,
(a)cIP3=10 μmol/L时,IP3R通道的popen;
(b)cCa_Cyt=0.1 μmol/L时,IP3R通道的popen.
图3 IP3R通道的开放概率
Fig.3 popen of IP3R channel这也符合已发表的实验结果[31].因此本研究建立的关于IP3R通道的8态模型可以较好地反映IP3R通道的动力学特性.
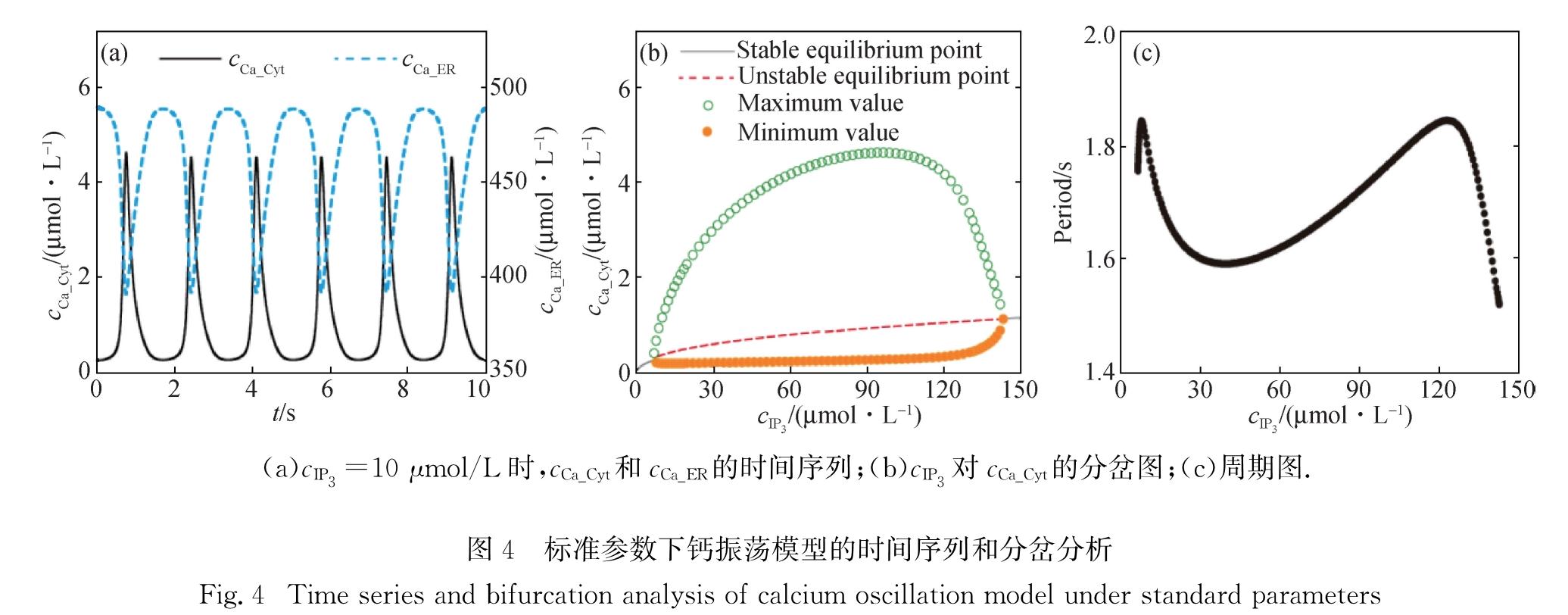
2.2 钙振荡接下来通过对钙振荡模型进行数值模拟研究细胞内Ca2+的动力学.图4(a)所示为cCa_Cyt和cCa_ER随时间变化的曲线,它们均呈周期性变化,cCa_Cyt的振幅在5 μmol/L以下,每次振荡中cCa_ER会由500 μmol/L下降到400 μmol/L以下,符合实际观测值[4-5].
时间序列只能反映特定cIP3下cCa_Cyt的变化情况,为了更全面地了解细胞质钙振荡的动力学行为,以cIP3作为分岔参数进行分岔分析.由图4(b)可以看出,cIP3较低和较高时Ca2+分别呈低稳态和高稳态,只有cIP</sub> 3适中时才会引起钙振荡,这些行为与实验现象相符[32-33].振荡区域内cCa_Cyt的振幅在0.15~5 μmol/L之间,变化范围较大,而周期变化范围较小(1.7 s左右,图4(c)),因此在标准参数下本模型属于典型的振幅调控模型[34].
(a)cIP3=10 μmol/L时,cCa_Cyt和cCa_ER的时间序列;(b)cIP3对cCa_Cyt的分岔图;(c)周期图.
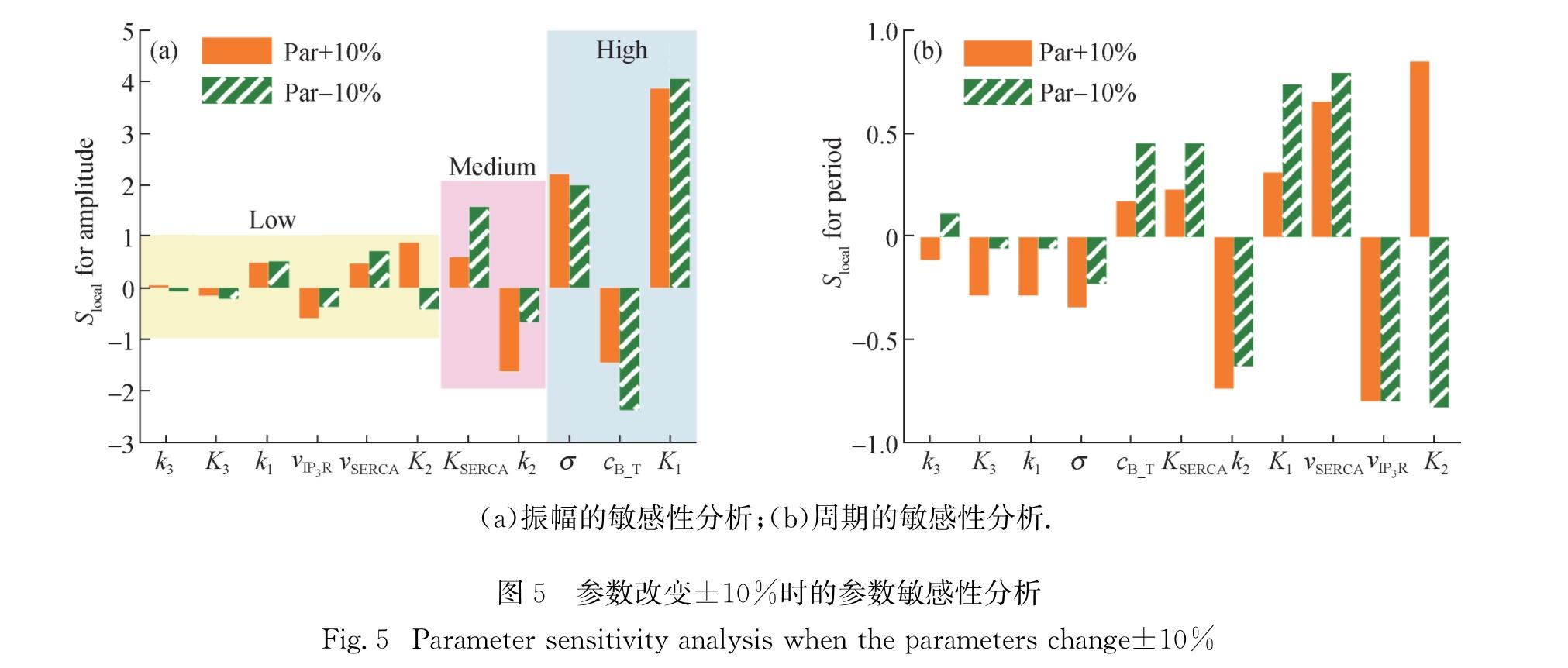
2.3 参数敏感性分析通过参数敏感性分析可以系统地了解模型参数对钙振荡的振幅和周期的影响.由图5(a)可知,对于钙振荡的振幅来说,内质网与细胞质的有效体积之比σ、cB_T和K1为高敏感参数; 图5(b)关于钙振荡周期的参数敏感性分析显示所有参数均为不敏感参数.这也从另一个角度说明了在标准参数下本模型属于振幅调控模型[34].
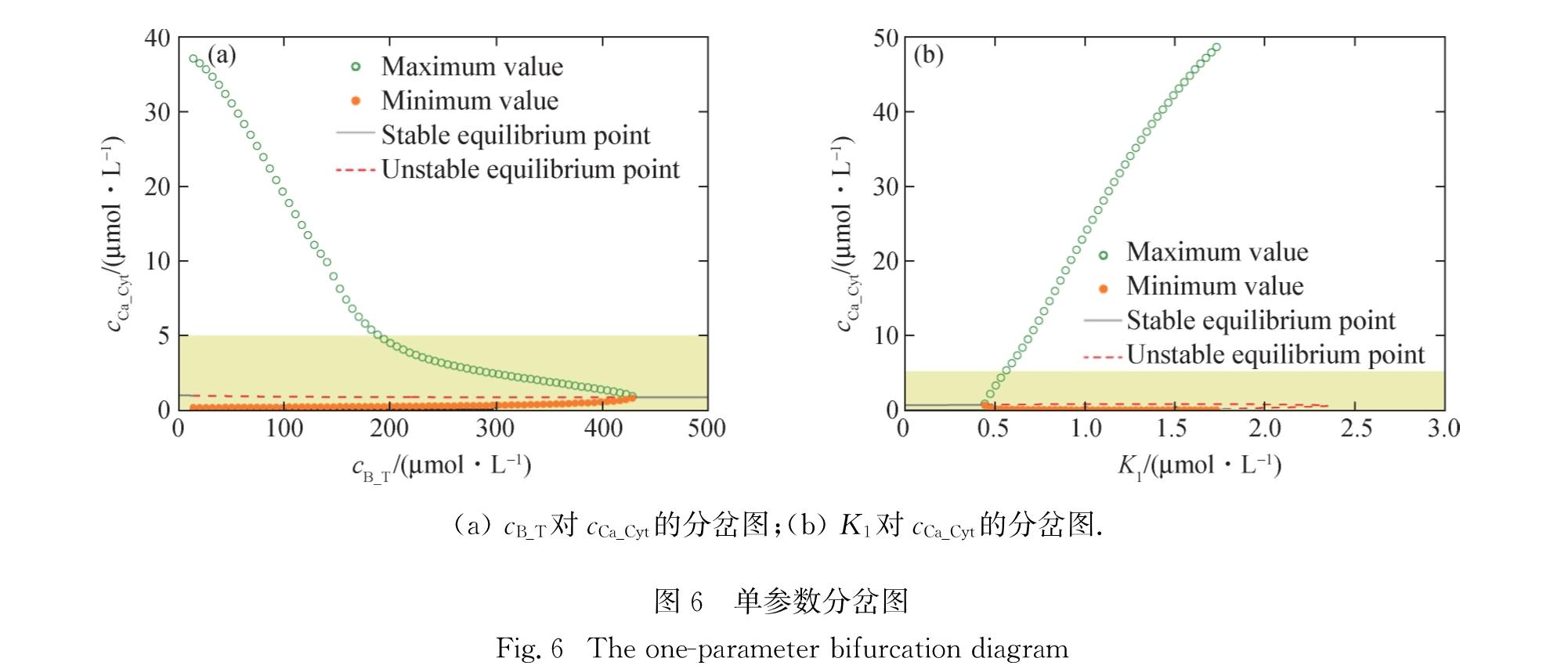
2.4 cB_T和K1单参数分岔分析参数敏感性分析结果表明:对于钙振荡的振幅来说,参数σ、cB_T和K1为高敏感参数.由于σ为内质网与细胞质的有效体积之比,属于人为较难控制的量,故接下来只对cB_T和K1进行单参数分岔分析.首先,细胞质内Ca2+缓冲蛋白可以结合Ca2+而降低后者的浓度,其对cCa_Cyt变化有直接作用.图6(a)显示随着缓冲蛋白总量cB_T的增多,cCa_Cyt的振幅逐渐减小直至消失,这一现象与最近发表的实验结果一致[35].其次,激活Ca2+的解离常数K1影响popen,从而间接影响cCa_Cyt变化.图6(b)显示当K1较小时,细胞质钙不振荡,随着K1的增大,钙振荡的振幅增加,但K1增大到某一值后振荡现象消失.需要指出的是:单参数分岔分析的主要目的是阐明目标参数对结果变化的影响趋势,为了能够完整地显示2个分岔点,部分cCa_Cyt超出了生理范围,因此在图6中用色块标记出生理范围部分.
(a)振幅的敏感性分析;(b)周期的敏感性分析.
图5 参数改变±10%时的参数敏感性分析
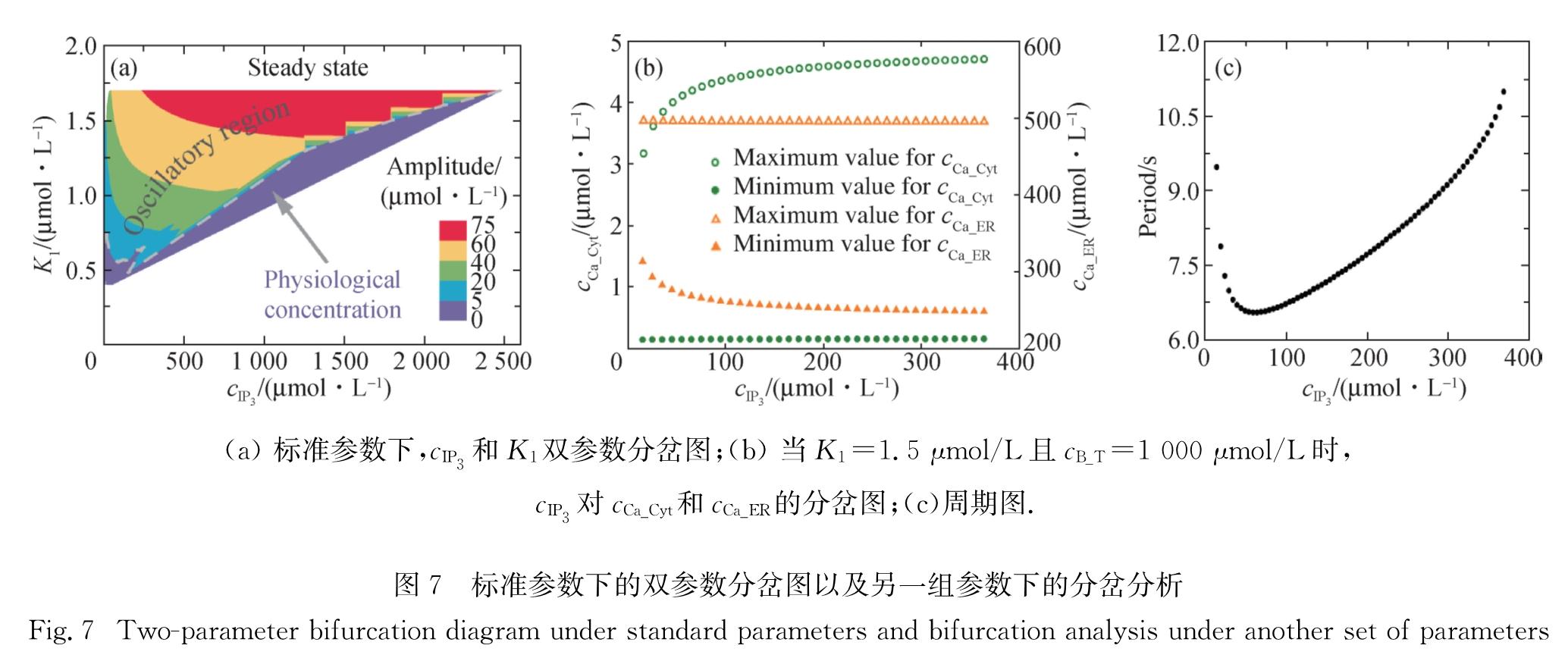
Fig.5 Parameter sensitivity analysis when the parameters change±10%(a)cB_T对cCa_Cyt的分岔图;(b)K1对cCa_Cyt的分岔图.2.5 cIP3和K1双参数分岔分析从对激活Ca2+的解离常数K1的单参数分岔分析发现,其标准参数值0.532处于霍夫分支点的边缘,这可能仅对应于某一特定类型的细胞.在不同类型的细胞中K1的值可能不同,因此对cIP3和K1进行了双参数分岔分析,结果表明K1不仅对钙振荡的振幅有重要作用,而且影响能产生钙振荡的cIP3的取值.图7(a)显示,当K1<0.4 μmol/L或K1>1.8 μmol/L时系统无振荡行为(白色区域); 当0.4 μmol/L≤K1≤1.8 μmol/L时,随着K1的增大,钙振荡区域(彩色区域)不断增大,钙振荡的振幅也越来越大.当cIP3取标准参数值80 μmol/L时,大部分K1所对应的cCa_Cyt超出了生理范围.由图6(a)结果可知,增加细胞质内Ca2+缓冲蛋白总量cB_T的值可降低钙振荡的振幅.线粒体由于其显著的摄钙能力而常被认为是细胞质Ca2+的缓冲系统[9,36],本模型并未明确考虑线粒体的摄钙作用,因此增大cB_T的值也可看成是一种隐式考虑线粒体的方法.
图7(b)为K1=1.5 μmol/L且cB_T=1 000 μmol/L时,cCa_Cyt和cCa_ER随cIP3变化的分岔图,可以看出cCa_Cyt的振幅依然维持在5 μmol/L以下,cCa_ER变化的范围在250~500 μmol/L之间,可以对应更多的实验结果[4-5].此时钙振荡的周期扩大到6~12 s之间(图7(c)).在此组参数下,cCa_Cyt的振幅变化范围较小,而周期变化范围较大,本模型变为典型的频率调控模型[34].
(a)标准参数下,cIP3和K1双参数分岔图;(b)当K1=1.5 μmol/L且cB_T=1 000 μmol/L时,
cIP3对cCa_Cyt和cCa_ER的分岔图;(c)周期图.
3 结 论
Ca2+常以浓度振荡变化的方式调控细胞内很多活动[37],因此研究其振荡机制有重要的意义[38].现已发表的大部分钙振荡模型为早期经典模型的推广,其结果中cCa_Cyt的峰值大多小于3 μmol/L,cCa_ER的峰值则至多仅达到几十μmol/L[11-16],与最新实验观测结果[4-5]相差甚远.本文基于对IP3R通道研究的最新成果[23-25],建立了一个新的钙振荡模型,此模型的核心部分为IP3R通道8态转换的动力学,它能够较好地拟合IP3R通道活性对cCa_Cyt依赖的钟型曲线[23].由模型得到的cCa_Cyt的振幅在0.15~5 μmol/L之间,cCa_ER的变化范围在250~500 μmol/L之间,与实验数据相吻合[4-5].除此之外,本研究的模型结果还重现了许多实验现象[31,34-35].
以往模型所得结果中cCa_Cyt和cCa_ER的振荡范围大多小于实验值,其主要原因之一是并未考虑Ca2+缓冲蛋白的作用[11-12,14-16],本文中构建的模型明确地考虑了它的作用并将其作为调控钙振荡振幅的关键因素.该模型借鉴了De Young-Keizer模型[14]的建模思想,但除了是否考虑Ca2+缓冲蛋白之外,还有2点重要的差别:1)De Young-Keizer模型假设IP3R通道的4个亚基是相互独立的,本文中的模型认为IP3R通道作为一个整体被调控.2)在De Young-Keizer模型中,激活Ca2+位点和抑制Ca2+位点与Ca2+的结合虽相互独立,但前者的解离常数小于后者,所以Ca2+先与激活Ca2+位点结合后与抑制Ca2+位点结合; 在本文中的模型激活Ca2+位点与抑制Ca2+位点按先后顺序结合Ca2+,这是二者在产生钟型曲线机制上的差别,也造成了本文中的模型可以在很广的cIP3范围内产生钙振荡.
参数敏感性分析结果显示内质网与细胞质的有效体积之比σ、细胞质内Ca2+缓冲蛋白的总浓度cB_T和激活Ca2+的解离常数K1为高敏感参数,对钙振荡有显著影响.利用单参数分岔分析分别预测了cB_T和K1对钙信号的影响,发现它们对钙信号有相反的作用:增大cB_T会使钙振荡的振幅变小,而增大K1会使其变大.双参数分岔分析表明K1对cIP3能产生钙振荡的区域及其振幅有很大影响,K1的值还可决定钙振荡为调幅模式还是调频模式,这不仅说明不同细胞类型间K1的值不同,而且暗示可以通过基因工程技术改变K1从而影响细胞对外界刺激的响应进而决定细胞命运.
综上所述,本研究基于IP3R通道活性对cCa_Cyt依赖的钟型曲线构建了一个新的钙振荡模型,该模型相比于之前的模型在cCa_Cyt和cCa_ER的振幅方面更加接近实验结果.因此,该模型不仅对于人们理解钙振荡机制有重要的意义,而且可以应用到相关实验中使研究者更好地解释和预测实验结果.
- [1] BERRIDGE M J,LIPP P,BOOTMAN M D.The versatility and universality of calcium signalling[J].Nature Reviews Molecular Cell Biology,2000,1(1):11-21.
- [2] BERRIDGE M J,BOOTMAN M D,LIPP P.Calcium:a life and death signal[J].Nature,1998,395(6703):645-648.
- [3] 牛帅,帅建伟,祁宏.Bcl-2蛋白抑制钙信号的建模与全局动力学分析[J].物理学报,2017,66(23):238701.
- [4] SUZUKI J,KANEMARU K,IINO M.Genetically encoded fluorescent indicators for organellar calcium imaging[J].Biophysical Journal,2016,111(6):1119-1131.
- [5] GIORGI C,DANESE A,MISSIROLI S,et al.Calcium dynamics as a machine for decoding signals[J].Trends in Cell Biology,2018,28(4):258-273.
- [6] TOYOSHIMA C,IWASAWA S,OGAWA H,et al.Crystal structures of the calcium pump and sarcolipin in the Mg2+-bound E1 state[J].Nature,2013,49(7440):260-264.
- [7] CHANG Y Q,BRUNI R,KLOSS B,et al.Structural basis for a pH-sensitive calcium leak across membranes[J].Science,2014,344(6188):1131-1135.
- [8] BERRIDGE M J,BOOTMAN M D,RODERICK H L.Calcium signalling:dynamics,homeostasis and remodelling[J].Nature Reviews Molecular Cell Biology,2003,4(7):517-529.
- [9] RIZZUTO R,DE STEFANI D,RAFFAELLO A,et al.Mitochondria as sensors and regulators of calcium signalling[J].Nature Reviews Molecular Cell Biology,2012,13(9):566-578.
- [10] DUPONT G,SNEYD J.Recent developments in models of calcium signalling[J].Current Opinion in Systems Biology,2017,3:15-22.
- [11] MEYER T,STRYER L.Molecular model for receptor-stimulated calcium spiking[J].Proceedings of the National Academy of Sciences,1988,85(14):5051-5055.
- [12] GOLDBETER A,DUPONT G,BERRIDGE M J.Minimal model for signal-induced Ca2+ oscillations and for their frequency encoding through protein phosphorylation[J].Proceedings of the National Academy of Sciences,1990,87(4):1461-1465.
- [13] MARHL M,HABERICHTER T,BRUMEN M,et al.Complex calcium oscillations and the role of mitochondria and cytosolic proteins[J].Biosystems,2000,57(2):75-86.
- [14] DE YOUNG G W,KEIZER J.A single-pool inositol 1,4,5-trisphosphate-receptor-based model for agonist-stimulated oscillations in Ca2+ concentration[J].Proceedings of the National Academy of Sciences,1992,89(20):9895-9899.
- [15] ATRI A,AMUNDSON J,CLAPHAM D,et al.A single-pool model for intracellular calcium oscillations and waves in the Xenopus laevis oocyte[J].Biophysical Journal,1993,65(4):1727-1739.
- [16] SNEYD J,DUFOUR J F.A dynamic model of the type-2 inositol trisphosphate receptor[J].Proceedings of the National Academy of Sciences,2002,99(4):2398-2403.
- [17] BEZPROZVANNY I,WATRAS J,EHRLICH B E.Bell-shaped calcium-response curves of Ins(1,4,5)P3-and calcium-gated channels from endoplasmic reticulum of cerebellum[J].Nature,1991,351:751-754.
- [18] FINCH E A,TURNER T J,GOLDIN S M.Calcium as a coagonist of inositol 1,4,5-trisphosphate-induced calcium release[J].Science,1991,252(5004):443-446.
- [19] SNEYD J,TSANEVA-ATANASOVA K,YULE D I,et al.Control of calcium oscillations by membrane fluxes[J].Proceedings of the National Academy of Sciences,2004,101(5):1392-1396.
- [20] QI H,LI L X,SHUAI J W.Optimal microdomain crosstalk between endoplasmic reticulum and mitochondria for Ca2+ oscillations[J].Scientific Reports,2015,2015(5):7984.
- [21] SNEYD J,HAN J M,WANG L W,et al.On the dynamical structure of calcium oscillations[J].Proceedings of the National Academy of Sciences,2017,114(7):1456-1461.
- [22] LI X,ZHANG S X,LIU X J,et al.Dynamic analysis on the calcium oscillation model considering the influences of mitochondria[J].Biosystems,2018,163:36-46.
- [23] SHINOHARA T,MICHIKAWA T,ENOMOTO M,et al.Mechanistic basis of bell-shaped dependence of inositol 1,4,5-trisphosphate receptor gating on cytosolic calcium[J].Proceedings of the National Academy of Sciences,2011,108(37):15486-15491.
- [24] HAMADA K,MIYATAKE H,TERAUCHI A,et al.IP3-mediated gating mechanism of the IP3 receptor revealed by mutagenesis and X-ray crystallography[J].Proceedings of the National Academy of Sciences,2017,114(18):4661-4666.
- [25] PAKNEJAD N,HITE R.Structural basis for the regulation of inositol trisphosphate receptors by Ca2+ and IP3[J].Nature Structural & Molecular Biology,2018,25(8):660-668.
- [26] WINTHER A M L,BUBLITZ M,KARLSEN J L,et al.The sarcolipin-bound calcium pump stabilizes calcium sites exposed to the cytoplasm[J].Nature,2013,495(7440):265-269.
- [27] FAN G Z,BAKER M L,WANG Z,et al.Gating machinery of InsP3R channels revealed by electron cryomicroscopy[J].Nature,2015,527(7578):336-341.
- [28] SHUAI J W,YANG D P,PEARSON J E,et al.An investigation of models of the IP3R channel in Xenopus oocyte[J].Chaos,2009,19(3):037105.
- [29] CAI X H,LI X,QI H,et al.Comparison of gating dynamics of different IP3R channels with immune algorithm searching for channel parameter distributions[J].Physical Biology,2016,13(5):056005.
- [30] 牛帅,孙小强,祁宏.改进双钙库模型的分岔分析[J].中山大学学报(自然科学版),2018,57(5):132-139.
- [31] MAK D O D,MCBRIDE S,FOSKETT J K.Inositol 1,4,5-tris-phosphate activation of inositol tris-phosphate receptor Ca2+ channel by ligand tuning of Ca2+ inhibition[J].Proceedings of the National Academy of Sciences,1998,95(26):15821-15825.
- [32] JACOB R,MERRITT J E,HALLAM T J,et al.Repetitive spikes in cytoplasmic calcium evoked by histamine in human endothelial cells[J].Nature,1988,335(6185):40-45.
- [33] LECHLEITER J D,JOHN L M,CAMACHO P.Ca2+ wave dispersion and spiral wave entrainment in Xenopus laevis oocytes overexpressing Ca2+ ATPases[J].Biophysical Chemistry,1998,72(1):123-129.
- [34] DE PITTA M,VOLMAN V,LEVINE H,et al.Coexistence of amplitude and frequency modulations in intracellular calcium dynamics[J].Physical Review E,2008,77(3):030903.
- [35] PECZE L,BLUM W,SCHWALLER B.Routes of Ca2+ shuttling during Ca2+ oscillations[J].Journal of Biological Chemistry,2015,290(47):28214-28230.
- [36] GIORGI C,MARCHI S,PINTON P.The machineries,regulation and cellular functions of mitochondrial calcium[J].Nature Reviews Molecular Cell Biology,2018,19(11):713-730.
- [37] 吴晨旭,帅建伟,MERLITZ H.软物质体系动力学特性及生物体系物质与信号的传输[J].厦门大学学报(自然科学版),2011,50(2):239-244.
- [38] SNEYD J,TSANEVA-ATANASOVA K,REZNIKOV V,et al.A method for determining the dependence of calcium oscillations on inositol trisphosphate oscillations[J].Proceedings of the National Academy of Sciences,2006,103(6):1675-1680.