< br/>通信作者:wshuang@jmu.edu.cn < br/>
(1.集美大学水产学院,福建 厦门 361021; 2.厦门大学海洋与地球学院,福建 厦门 361102; 3.福建省海洋生物资源开发利用协同创新中心,福建 厦门 361021)
(1.College of Fisheries,Jimei University,Xiamen 361021,China; 2.College of Ocean and Earth Sciences,Xiamen University,Xiamen 361102,China; 3.Fujian Collaborative Innovation Center for Exploitation and Utilization of Marine Biological Resources,Xiamen 361021,China)
Scylla paramamosain; Crustin; cDNA cloning; antimicrobial activity; scanning electron microscopy
DOI: 10.6043/j.issn.0438-0479.201808007
备注
< br/>通信作者:wshuang@jmu.edu.cn < br/>
Crustins是一类较早发现并广泛分布在甲壳动物中且富含半胱氨酸的阳离子抗菌肽,能够参与抗菌免疫应答.从拟穴青蟹(Scylla paramamosain)中克隆获得一个Crustin基因新变体,命名为SpCrus1a,其cDNA序列全长744 bp,开放阅读框编码113个氨基酸,成熟肽分子质量10.03 ku,理论等电点8.30.表达分析结果发现其转录本主要存在于鳃、卵巢、上皮组织中,经脂多糖刺激后SpCrus1a表达会上调.体外合成SpCrus1a的第29~47位氨基酸(SpCrus1a29-47)进行抗菌活性实验,发现其对革兰氏阳性菌具有较强的抗菌活性,而对被测的革兰氏阴性菌抗菌活性较弱或无抗菌活性.浓度24 μmol/L的合成肽SpCrus1a29-47能够在5 min内杀死大多数的金黄色葡萄球菌(Staphylococcus aureus),在120 min内杀死全部的金黄色葡萄球菌.扫描电镜分析发现合成肽SpCrus1a29-47可造成金黄色葡萄球菌表面结构崎岖不平,高浓度SpCrus1a29-47会引起细菌大量死亡.上述结果表明SpCrus1a是抗菌肽Crustin的新变体.
Crustins are cationic cysteine-rich antimicrobial peptides discovered earlier and widely distributed across the crustaceans,and involved in the antimicrobial immune responses.In this study,a novel Crustin isoform was cloned from Scylla paramamosain,namely SpCrus1a.The full-length cDNA of SpCrus1a was 744 bp,with an open reading frame encoding a peptide of 113 amino acids.The predicted molecular mass of the mature protein was 10.03 ku with an estimated pI of 8.30.The transcriptional transcript of SpCrus1a was highly expressed in gills,ovary and carapace by RT-PCR analysis,and was up-regulated in gills after lipopolysaccharide challenge.The antimicrobial activity experiment was performed with the synthetic peptide from 29 to 47 amino acid residues of SpCrus1a(SpCrus1a29-47).It was found that the synthetic peptide showed more strong anti-bacterial activity against Gram-positive bacteria,but had no or little antimicrobial activity against selected Gram-negative bacteria.Most of Staphylococcus aureus were killed by the synthetic peptide SpCrus1a29-47(24 μmol/L)within 5 min and all were killed within 120 min.Observation by scanning electron microscopy revealed that the surface of S. aureus cells treated with the synthetic peptide SpCrus1a29-47appeared to be rough and distorted,and higher concentration of SpCrus1a29-47 could cause cell death.The above results demonstrate that SpCrus1a is a novel Crustin isoform.
引言
抗生素的发现与应用为人类生命的延长带来了福音,大大提高了人们对疾病的抵抗能力,然而近十几年来,抗生素滥用导致的耐药性使人们一直在寻求替代品[1-2],抗菌肽(antimicrobial peptides)由于其天然的抗细菌、真菌、病毒等特性而成为其中最有潜力的替代品之一[3].抗菌肽,也称为宿主防御肽,是先天免疫系统的基础组分,不仅可迅速消除入侵的病原体,也可启动其他免疫反应.1981年瑞典科学家Boman等[4]首次从昆虫中分离获得抗菌肽,称为天蚕素(cecropin),随后在植物[5]、细菌[6]中均有抗菌肽的报道.甲壳动物中的抗菌肽最早于1996年在普通滨蟹(Carcinus maenas)中发现[7],但与其他许多物种相比,发现的种类偏少.
1999年,Relf等[8]在普通滨蟹的血淋巴中分离得到一个分子质量11.5 ku且富含半胱氨酸的阳离子抗菌肽,具有抑制革兰氏阳性菌的活性,后来被确定为Crustin家族成员.Crustins是一类富含半胱氨酸的阳离子抗菌肽,分子质量为7~14 ku,C端含有该家族蛋白分子中高度保守、以4个二硫桥为核心的乳清酸性蛋白(whey acidic protein,WAP)结构域[9],在斑节对虾(Penaeus monodon)[10]、日本囊对虾(Marsupenaeus japonicus)[11]等中均有报道.典型的Crustins包括3个部分,即N端的信号肽、多域区(multi-domain region)和C端的WAP结构域.根据WAP结构域的数量和多域区结构的不同,可细分为5种类型,除Ⅳ型有2个WAP结构域外[12],其他4种均仅含有1个WAP,不同在于多域区:Ⅰ型为半胱氨酸富集区,多见于蟹类[13]、龙虾[14]等; Ⅱ型为半胱氨酸和甘氨酸富集区,Ⅲ型为脯氨酸和精氨酸富集区,Ⅱ、Ⅲ型多见于对虾[15-16]; Ⅴ型为半胱氨酸和芳香族氨基酸富集区,首次发现于蚁类[17].
拟穴青蟹(Scylla paramamosain)是我国重要的经济蟹类,在我国南方是一种重要的海水养殖品种,但一直存在高死亡率现象,其主要依靠先天性免疫防御外源微生物的入侵,迄今尚无有效的防治措施.抗菌肽Crustins是甲壳动物先天性免疫中一类重要的效应分子,目前在拟穴青蟹中已经发现CrusSp[18]、SpCrus2[19]、SpCrus3和SpCrus4[20]以及SpCrus5[21].本研究从拟穴青蟹中克隆获得一个Crustin基因新变体,命名为SpCrus1a,并对其序列进行生物信息学分析,进而分析SpCrus1a在脂多糖(LPS)刺激下的免疫响应及体外合成部分肽段的抗菌活性,以期为认识Crustin家族提供新的基础资料.
1 材料与方法
1.1 主要试剂Trizol总RNA提取试剂盒购自Invitrogen公司,FastStart Universal SYBR Green Master(Rox)购自Roche公司,GoScriptTM 反转录试剂盒和DNase 试剂盒购自Promega公司,ZX EasyTaq PCR SuperMix购自全式金公司,LPS(大肠杆菌(Escherichia coli)055:B5)购自Sigma公司,凝胶回收试剂盒购自东盛公司,Bradford蛋白浓度测定试剂盒购自碧云天生物技术研究所,pMD18-T载体、DNA连接试剂盒购自TaKaRa公司,琼脂糖购自Promega公司,胰蛋白胨和酵母粉购自OXOID公司,营养肉汤培养基和MH(Mueller-Hinton)培养基购自广东环凯微生物公司.
1.2 拟穴青蟹的处理拟穴青蟹购自福建省厦门市集美区水产品市场,个体质量(300±10)g,壳宽(12±0.5)cm.采样前,于暂养池(3.45 mx1.25 m)暂养2 d,备用.将拟穴青蟹置于冰上麻醉5min.体表消毒后,采集血淋巴细胞(蟹抗凝剂:NaCl 450 mmol/L,葡萄糖100 mmol/L,柠檬酸26 mmol/L,柠檬酸三钠30 mmol/L,乙二胺四乙酸10 mmol/L,pH 4.6,用0.22 μm滤膜过滤除菌)、心脏、肝胰腺、鳃、卵巢和上皮的组织/器官样品,置于1 mL Trizol试剂中匀浆,备用.
1.3 SpCrus1a基因的克隆参考Trizol试剂盒说明书提取拟穴青蟹样品总RNA,在分光光度计(NanoDrop 2000)下检测其浓度和纯度(要求A260/A280比值范围在1.8~2.0),经1.5%(质量分数,下同)琼脂糖凝胶电泳检测其完整性.将处理后的总RNA样品采用GoScriptTM反转录试剂盒进行反转录,得到cDNA.
以血淋巴组织的cDNA为模板,PCR反应体系:引物SpCrus1a-F和SpCrus1a-R(表1)各1μL,2xEasyTaq PCR SuperMix 8.5 μL,cDNA模板1 μL,无菌Milli-Q水补充至25 μL.PCR反应条件:94 ℃ 3 min; 94 ℃ 30 s,59 ℃ 40 s,72 ℃ 45 s,30个循环; 72 ℃ 10 min.PCR产物经1.5%琼脂糖凝胶电泳检测,参考东盛凝胶回收试剂盒说明书进行目的片段回收.然后用TaKaRa DNA连接试剂盒将PCR回收产物与pMD18-T载体连接,并转化到大肠杆菌DH5α感受态细胞,经阳性克隆鉴定后测序验证.
1.4 SpCrus1a基因在正常组织/器官中的转录表达反转录获得拟穴青蟹组织/器官(包括血淋巴细胞、心脏、肝胰腺、鳃、卵巢和上皮)的cDNA模板,以β-actin为内参进行半定量反转录PCR(RT-PCR)检测,反应体系:SpCrus1a-qF和SpCrus1a-qR(表1)各0.5 μL,2xEasyTaq PCR SuperMix 12.75 μL,cDNA模板1 μL,无菌Milli-Q水补充至25 μL.PCR反应条件:94 ℃ 3 min; 94 ℃ 30 s,66 ℃(SpCrus1a)/64 ℃(β-actin)30 s,72 ℃ 45 s,其中SpCrus1a执行35个循环,β-actin执行25个循环; 72 ℃ 10 min.扩增产物采用1.5%琼脂糖凝胶电泳进行检测.
1.5 SpCrus1a基因的免疫响应表达模式分析将拟穴青蟹随机分为两组:对照组注射蟹生理盐水(NaCl 496 mmol/L,KCl 9.52 mmol/L,MgSO4 12.8 mmol/L,CaCl2 16.2 mmol/L,MgCl2 0.84 mmol/L,NaHCO3 5.95 mmol/L,4-羟乙基哌嗪乙磺酸20 mmol/L,pH 7.4,121 ℃高压灭菌20 min),LPS组注射质量浓度为2 mg/mL的LPS(溶于蟹生理盐水),按200 μL/只于第四步足基部注射.在注射后6,12,18和24 h采集拟穴青蟹的鳃样品(每组每个时间点随机挑取3只).按1.3节方法分别提取总RNA,反转录成cDNA后进行实时荧光定量PCR(qRT-PCR)检测,反应体系:SpCrus1a-qF和SpCrus1a-qR(表1)各0.32 μL,cDNA模板3 μL,SYBR Green Master 10 μL,无菌Milli-Q水补至20 μL.PCR反应条件:95 ℃ 10 min; 95 ℃变性30 s,66 ℃(SpCrus1a)/64 ℃(β-actin)30 s,72 ℃ 25 s,荧光采集点83 ℃(SpCrus1a)/84 ℃(β-actin)5 s,执行40个循环.
数据处理与统计:β-actin作为内参,对组织样品的表达量进行标准化处理,SpCrus1a的相对表达量以同一时间点LPS组样品的标准化表达量除以对应时间点对照组样品的标准化表达量表示.所有数据均用平均值±标准差的方式表示.用SPSS软件进行数据统计分析,用Origin8软件作图.
1.6 SpCrus1a部分肽段合成和抗菌实验菌株来源SpCrus1a的部分肽段委托武汉东湖新技术开发区金垦生化试剂经营部和南京金斯瑞生物科技有限公司以固相合成方法合成.
抗菌实验所用菌株:施氏假单胞菌(Pseudomonas stutzeri)、荧光假单胞菌(P.fluorescens)、弗氏志贺氏菌(Shigella flexner)、大肠杆菌、藤黄微球菌(Micrococcus luteus)、金黄色葡萄球菌(Staphylococcus aureus)、谷氨酸棒杆菌(Corynebacterium glutamicum)和溶壁微球菌(Micrococcus lysodeikticus)均购自中国科学院微生物研究所菌种保藏中心(CGMCC).
1.7 合成肽最小抑菌浓度(MIC)的测定合成肽用无菌Milli-Q水溶解并过滤除菌,分别稀释至96,48,24,12,6 μmol/L,置于冰上备用; 取被测细菌菌株,涂布于营养肉汤平板上,倒置过夜培养12~16 h; 挑取3~4个克隆接种于营养肉汤斜面培养基上,继续培养12~16 h; 磷酸钠盐缓冲液(10 mmol/L,pH 7.2,下同)冲洗新鲜制备的营养肉汤斜面细菌培养物,调整菌体A600为0.003.MIC的测定在无菌96孔细胞培养板(Nest公司)中进行,设置阳性对照组(加50 μL磷酸钠盐缓冲液和50 μL菌悬液)、空白对照组(加50 μL合成肽样品和50 μL磷酸钠盐缓冲液)和待测实验组(加50 μL合成肽样品和50 μL菌悬液),在最适条件下培养24~48 h后计算MIC.实验重复3次,每次每种被测菌株3个平行样.
1.8 合成肽杀菌动力学分析选取金黄色葡萄球菌为待测菌,调整合成肽浓度为24 μmol/L,将稀释的合成肽过滤除菌后添加50 μL于96孔细胞培养板中,与50 μL菌悬液混合均匀,并按照1.7节设置阳性对照组和空白对照组.合成肽与菌悬液共孵育5,15,30,60,90和120 min后,从96孔细胞培养板中取阳性对照组、待测实验组、空白对照组重悬,分别吸取6 μL金黄色葡萄球菌悬液稀释于600 μL磷酸钠盐缓冲液中,混匀后吸取40 μL涂布至营养肉汤平板上,37 ℃下倒置培养18~24 h,记录金黄色葡萄球菌单克隆数量,绘制杀菌动力学曲线,用GraphPad Prism 7软件分析并作图.
1.9 合成肽抗菌作用的扫描电子显微镜观察调整金黄色葡萄球菌菌体浓度为1x107 cfu/mL(cfu表示克隆形成单位); 将合成肽用无菌Milli-Q水分别稀释至48和96 μmol/L.750 μL菌悬液与750 μL合成肽稀释液混合,孵育1 h后6 000 g离心5 min,弃上清.加入1 mL 2.5%(体积分数)戊二醛重悬菌液,冰上静置2 h后6 000 g离心5 min,弃上清.加入1 mL磷酸盐缓冲液(PBS)重悬菌液,静置10 min后6 000 g离心5 min,弃上清.将高浓度的菌悬液滴加在载玻片上,冰上静置30 min后加入PBS浸泡15 min,吸去PBS,依次用30%,50%,70%,90%和无水乙醇梯度脱水,每次静置15 min.用叔丁醇脱水10次,每次10 min,然后在干燥杯中加满叔丁醇,4 ℃下过夜.待叔丁醇结晶后,采用临界点干燥法干燥样品,将样品喷金后于SUPRA55场发射扫描电子显微镜(Zeiss公司)观察.实验重复3次,每次2个平行样.
1.10 生物信息学分析网址及软件引物设计和分析利用Primer Premier 5.0软件; BLAST分析在http:∥blast.ncbi.nlm.nih.gov/Blast.cgi上进行; 开放阅读框(open reading frame,ORF)的查找与翻译利用http:∥www.fr33.net/translator.php在线工具; 信号肽预测在http:∥www.cbs.dtu.dk/services/SignalP/上进行; 预测蛋白功能结构域、分子量和理论等电点在http:∥web.expasy.org/computepi/和http:∥smart.embl-heidelberg.de/smart/setmode.cgi上进行.
2 结果与分析
2.1 SpCrus1a基因的克隆与序列分析克隆获得一个Crustin基因新变体,命名为SpCrus1a.cDNA序列长度为744 bp,其中5'-非翻译区(5'-untranslated region,5'-UTR)为186 bp,ORF为342 bp,编码113个氨基酸,3'-UTR为216 bp(图1).生物信息学分析显示,SpCrus1a的N端存在由20个氨基酸组成的信号肽,C端有一个由8个保守半胱氨酸为主构成的WAP结构域,预测其成熟肽分子质量为10.03 ku,理论等电点为8.30; 此外,在信号肽和WAP结构域之间存在着半胱氨酸富集区,符合典型的Ⅰ型Crustins结构特征(图2).
TAG为终止密码子; ATG为起始密码子; AATAA为加尾信号; 下划线为信号肽; 阴影部分为WAP结构域.
2.2 SpCrus1a在正常组织/器官中的转录表达以β-actin为内参基因,采用半定量RT-PCR的方法检测SpCrus1a基因在正常养殖的拟穴青蟹不同组织/器官中的转录表达情况,结果显示(图3):SpCrus1a在所有检测的组织/器官中均有不同程度的表达,其中在鳃中表达量最高,上皮、卵巢次之,而血淋巴细胞、肝胰腺和心脏中的转录表达量较低.H:心脏; Hc:血淋巴细胞; Hp:肝胰腺; G:鳃; O:卵巢; C:上皮.
2.3 LPS刺激下SpCrus1a在鳃中的转录表达用LPS对拟穴青蟹进行活体刺激,并对刺激后不同时间点(6,12,18,24 h)的鳃样品进行qRT-PCR检测,结果发现:LPS诱导后24 h,鳃中SpCrus1a基因表达量相比于对照组呈现极显著上调(p<0.01),且上调幅度最大,为对照组的5.63倍; 此外,SpCrus1a基因在6 h表达水平也有显著上调(p<0.05)(图4).*表示差异显著(p<0.05),**表示差异极显著(p<0.01).
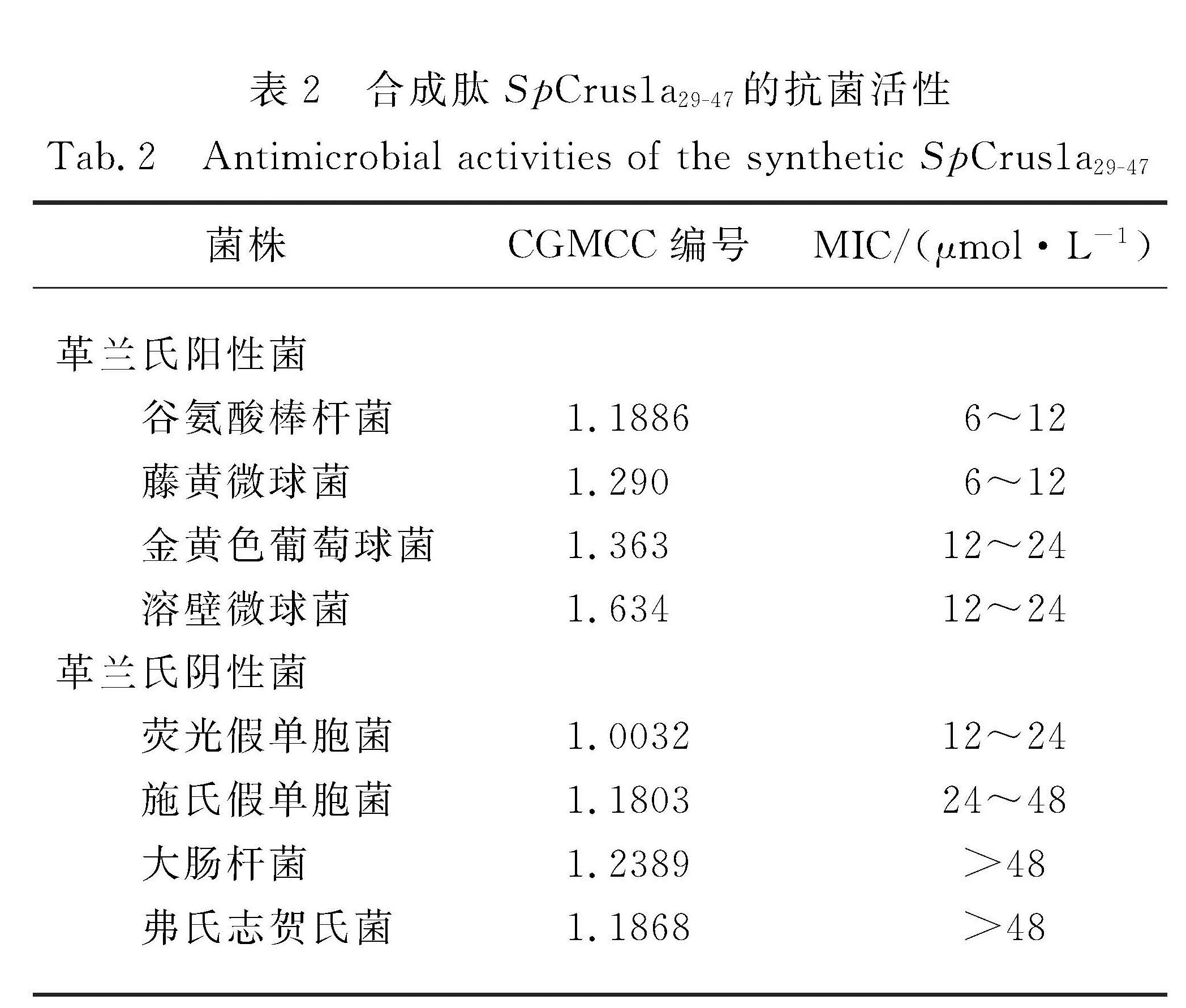
2.4 合成肽SpCrus1a29-47的抗菌活性经过SMART软件预测分析并设计合成SpCrus1a的第29~47位氨基酸多肽,命名为SpCrus1a29-47,理化性质如下:序列CRSWCKRPGHPEKNAFYCC,预测分子质量2.28 ku,预测等电点8.92,合成肽纯度高于95%.将合成肽SpCrus1a29-47倍比稀释至96~6 μmol/L,与等体积的菌悬液共同孵育24~48 h后计算MIC,结果显示(表2):其中SpCrus1a29-47对被测的革兰氏阳性菌如谷氨酸棒杆菌和藤黄微球菌具有较强的抗菌活性(MIC=6~12 μmol/L),对溶壁微球菌和金黄色葡萄球菌具有一定的抗菌活性(MIC=12~24 μmol/L); 被测的革兰氏阴性菌中,对荧光假单胞菌(MIC=12~24 μmol/L)和施氏假单胞菌(MIC=24~48 μmol/L)有一定的抗菌活性,对大肠杆菌及弗氏志贺氏菌无抗菌活性(MIC>48μmol/L).
表2 合成肽SpCrus1a29-47的抗菌活性
Tab.2 Antimicrobial activities of the synthetic SpCrus1a29-472.5 合成肽SpCrus1a29-47的杀菌动力学曲线金黄色葡萄球菌属于多重耐药性致病菌,拟穴青蟹物种中的多条Crustins[19-20]对其有抗菌活性.合成肽SpCrus1a29-47(浓度24 μmol/L)与金黄色葡萄球菌(吸光度A600约为0.003)共孵育一段时间后,测定其杀菌动力学数据,结果如图5所示:随着孵育时间延长,金黄色葡萄球菌的存活率不断降低,共孵育5 min时菌落存活率降至50%,共孵育90 min时菌落存活率仅为10%,共孵育120 min时菌落存活率为0.可见SpCrus1a29-47能够短时间内杀死大多数的金黄色葡萄球菌,2 h内杀死全部的金黄色葡萄球菌.
图5 合成肽SpCrus1a29-47对金黄色葡萄球菌的杀菌动力学曲线
Fig.5 Kinetic curve of killing S. aureus by the synthetic SpCrus1a29-472.6 合成肽SpCrus1a29-47对金黄色葡萄球菌超微结构的影响将金黄色葡萄球菌与合成肽SpCrus1a29-47(48,96 μmol/L)共孵育1 h,经过固定、脱水、干燥和喷金后使用扫描电子显微镜观察其超微结构的变化.结果显示:在与无菌Milli-Q 水共孵育的对照组中,正常的金黄色葡萄球菌细胞表面完整、光滑,细胞形态未发生改变(图6(a)); 而与一定浓度的合成肽共孵育后,金黄色葡萄球菌的表面变得粗糙,表面结构崎岖不平(图6(b)); 在更高的合成肽浓度下出现大量细胞碎片,细菌死亡(图6(c)).
图6 扫描电镜观察合成肽SpCrus1a29-47对金黄色葡萄球菌形态的影响
Fig.6 Effects of the synthetic SpCrus1a29-47 on morphology of S. aureus by scanning electron microscopy3 讨 论
本研究从拟穴青蟹中获得一个Crustin基因新变体,命名为SpCrus1a.预测其成熟肽分子质量为10.03 ku,理论等电点为8.30.序列分析显示其具有Crustin家族的特征性结构,包括N端的信号肽、C端的WAP结构域以及两者之间的半胱氨酸富集区,符合典型Ⅰ型Crustins结构特征.
大多数Crustins在血淋巴细胞中持续高表达,如在日本囊对虾[22]和蜘蛛蟹(Paralithodes camtschaticus)[23]中.本研究发现SpCrus1a基因的转录本主要分布于鳃、卵巢和上皮中.已报道的拟穴青蟹Ⅰ型Crustins中,CrusSp[18]主要分布在血淋巴、鳃、肠、肌肉中,SpCrus3和SpCrus4[20]主要在鳃中表达; 已报道的拟穴青蟹Ⅱ型Crustins中,SpCrus2[19]和SpCrus5[21]均在鳃中高表达.上述研究表明Crustins在组织表达模式上较多样,而其他已发现的拟穴青蟹Crustin基因在鳃中的表达量均显著高于其他组织,与本研究获得的SpCrus1a基因表达模式类似,由此认为鳃可能是生成或释放SpCrust1a的主要场所之一.
LPS主要存在于革兰氏阴性细菌细胞壁表面,是一种与细菌感染相关的分子模式.在Ⅰ型Crustins的细菌诱导实验中,三疣梭子蟹(Portunus trituberculatus)的PtCrustin和PtCrustin2基因在受到溶藻弧菌(Vibrio alginolyticus)感染后24 h表达显著上调,分别上调3.5倍(p<0.01)和13.8倍(p<0.05),而PtCrustin3基因的响应更早,在8 h时就显著上调(p<0.05)[13,24]; SpCrus1a可能和上述Crustins基因类似,参与拟穴青蟹的抗细菌免疫过程; 白斑综合征病毒感染的日本囊对虾鳃组织的转录分析发现,抗菌肽MjSWD基因在6和12 h表达水平上升,24 h表达水平下降,而48 h表达水平又显著上升,达到新的峰值[25].SpCrus1a表达变化情况与MjSWD类似,推测LPS刺激的拟穴青蟹体内出现细菌增殖从而引发SpCrus1a二次反应.
由于抗菌肽在体内含量甚微,直接从体内提取并分离纯化蛋白费时又费力,目前常用转基因表达技术和固相合成方法来获得高产量的抗菌肽,且化学合成方法用于生产少于30个氨基酸的多肽具有较高的效益成本比[26].本研究中SpCrus1a的部分合成肽段SpCrus1a29-47的抗菌实验结果表明,其对革兰氏阳性菌如谷氨酸棒杆菌、藤黄微球菌具有较强的抗菌活性(MIC=6~12 μmol/L),对金黄色葡萄球菌、溶壁微球菌也具有一定的抗菌活性(MIC=12~24 μmol/L),而革兰氏阴性菌中对荧光假单胞菌(MIC=12~24 μmol/L)和施氏假单胞菌(MIC=24~48 μmol/L)有一定的抗菌活性,对大肠杆菌及弗氏志贺氏菌无抗菌活性(MIC>48 μmol/L).已报道的拟穴青蟹Ⅰ型Crustins中,CrusSp[18]对藤黄微球菌(MIC=0.156~0.312 μmol/L)有较强的抗菌活性,而对大肠杆菌、肺炎克雷伯菌等革兰氏阴性菌无活性; SpCrus3[20]对金黄色葡萄球菌(MIC=3.125~6.25 μmol/L)和枯草芽孢杆菌(MIC=6.25~12.5 μmol/L)有较强的抗菌活性,而对大肠杆菌及哈维氏弧菌的抗菌活性偏低(MIC>25 μmol/L).比较可知SpCrus1a29-47的抗菌活性和CrusSp和SpCrus3相似,对革兰氏阳性菌具有较强的抗菌活性,对被测的革兰氏阴性菌无活性或活性较弱,符合Crustin家族抗菌肽对革兰氏阳性菌有更强抗菌活性的特点,但SpCrus1a29-47的MIC高于CrusSp和SpCrus3.因本研究仅对SpCrus1a的第29~47位氨基酸设计合成并检测其功能,SpCrus1a基因整个编码序列的抗菌活性还有待进一步研究.
扫描电子显微镜结果表明,分别用2倍MIC(48 μmol/L)和4倍MIC(96 μmol/L)的合成肽SpCrus1a29-47对金黄色葡萄球菌进行处理,可以使金黄色葡萄球菌形态发生改变,表面出现凹陷甚至导致菌体裂解.类似地,斑节对虾的2个变体CrustinPm1和CrustinPm7用10倍MIC来处理金黄色葡萄球菌时,造成了菌体细胞表面变得粗糙,并被碎片覆盖[27].推测合成肽段SpCrus1a29-47可能是通过与金黄色葡萄球菌的细胞膜相互作用来杀死细菌.
4 结 论
本研究中克隆获得一个Crustin基因新变体,命名为SpCrus1a.RT-PCR结果显示SpCrus1a在鳃中的表达量最高,且LPS刺激后会有上调表达.设计并合成的部分肽段SpCrus1a29-47在抗菌实验中表明其对革兰氏阳性菌有较强的抗菌活性,对被测的革兰氏阴性菌无活性或活性较弱.杀菌动力学曲线结果表明合成肽SpCrus1a29-47能在短时间内杀死大部分金黄色葡萄球菌,扫描电镜发现在合成肽SpCrus1a29-47的处理下金黄色葡萄球菌表面变得粗糙甚至细菌裂解死亡.上述结果为后续研究合成肽SpCrus1a29-47的抗菌机制奠定了基础.
- [1] WALSH C.Where will new antibiotics come from[J].Nature Reviews Microbiology,2003,1(1):65-70.
- [2] COATES A,HU Y M,BAX R,et al.The future challenges facing the development of new antimicrobial drugs[J].Nature Reviews Drug Discovery,2002,1(11):895-910.
- [3] SØRENREN O E,BORREGAARD N,COLE A M.Antimicrobial peptides in innate immune responses[M]∥Contributions to microbiology.Basel:KARGER,2008:61-77.
- [4] BOMAN H G,STEINER H.Humoral immunity in Cecropia pupae[J].Current Topics in Microbiology & Immunology,1981,95(4):75-91.
- [5] AVITABILE C,CAPPARELLI R,RIGANO M M,et al.Antimicrobial peptides from plants:stabilization of the γ core of a tomato defensin by intramolecular disulfide bond[J].Journal of Peptide Science,2013,19(4):240-245.
- [6] HASSAN M,KJOS M,NES I F,et al.Natural antimicrobial peptides from bacteria:characteristics and potential applications to fight against antibiotic resistance[J].Journal of Applied Microbiology,2012,113(4):723-736.
- [7] SCHNAPP D,KEMP G D,SMITH V J.Purification and characterization of a proline-rich antibacterial peptide,with sequence similarity to Bactenecin-7,from the haemocytes of the shore crab,Carcinus maenas[J].European Journal of Biochemistry,1996,240(3):532-539.
- [8] RELF J M,CHISHOLM J R S,KEMP G D,et al.Purification and characterization of a cysteine-rich 11.5-kDa antibacterial protein from the granular haemocytes of the shore crab,Carcinus maenas[J].European Journal of Biochemistry,1999,264(2):350-357.
- [9] SMITH V J,FERNANDES J M O,KEMP G D,et al.Crustins:enigmatic WAP domain-containing antibacterial proteins from crustaceans[J].Developmental & Comparative Immunology,2008,32(7):758-772.
- [10] CHEN J Y,CHUANG H,PAN C Y,et al.cDNA sequence encoding an antimicrobial peptide of chelonianin from the tiger shrimp Penaeus monodon[J].Fish & Shellfish Immunology,2005,18(2):179-183.
- [11] CHEN D D,HE N H,XU X.Mj-DWD,a double WAP domain-containing protein with antiviral relevance in Marsupenaeus japonicus[J].Fish & Shellfish Immunology,2008,25(6):775-781.
- [12] DU Z Q,REN Q,ZHAO X F,et al.A double WAP domain(DWD)-containing protein with proteinase inhibitory activity in Chinese white shrimp,Fenneropenaeus chinensis[J].Comparative Biochemistry & Physiology Part B:Biochemistry and Molecular Biology,2009,154(2):203-210.
- [13] CUI Z X,SONG C W,LIU Y,et al.Crustins from eyestalk cDNA library of swimming crab Portunus trituberculatus:molecular characterization,genomic organization and expression analysis[J].Fish & Shellfish Immunology,2012,33(4):937-945.
- [14] JIRAVANICHPAISAL P,LEE S Y,KIM Y A,et al.Antibacterial peptides in hemocytes and hematopoietic tissue from freshwater crayfish Pacifastacus leniusculus:characterization and expression pattern[J].Developmental & Comparative Immunology,2007,31(5):441-455.
- [15] CHRISTIE A E,RUS S,GOINEY C C,et al.Identification and characterization of a cDNA encoding a crustin-like,putative antibacterial protein from the American lobster Homaru samericanus[J].Molecular Immunology,2007,44(13):3333-3337.
- [16] JIA Y P,SUN Y D,WANG Z H,et al.A single whey acidic protein domain(SWD):containing peptide from fleshy prawn with antimicrobial and proteinase inhibitory activities[J].Aquaculture,2008,284(1/2/3/4):246-259.
- [17] ZHANG Z T,ZHU S Y.Comparative genomics analysis of five families of antimicrobial peptide-like genes in seven ant species[J].Developmental & Comparative Immunology,2012,38(2):262-274.
- [18] IMJONGJIRAK C,AMPARYUP P,TASSANAKAJON A,et al.Molecular cloning and characterization of crustin from mud crab Scylla paramamosain[J].Molecular Biology Reports,2009,36(5):841-850.
- [19] WANG H,ZHANG J X,WANG Y,et al.Newly identified type Ⅱ crustin(SpCrus2)in Scylla paramamosain contains a distinct cysteine distribution pattern exhibiting broad antimicrobial activity[J].Developmental & Comparative Immunology,2018,84:1-13.
- [20] WANG Y,ZHANG X W,WANG H,et al.SpCrus3 and SpCrus4 share high similarity in mud crab(Scylla paramamosain)exhibiting different antibacterial activities[J].Developmental & Comparative Immunology,2018,82:139-151.
- [21] WANG Y,ZHANG C,WANG H,et al.Involvement of a newly identified atypical type Ⅱ crustin(SpCrus5)in the antibacterial immunity of mud crab Scylla paramamosain[J].Fish & Shellfish Immunology,2018,75:346-356.
- [22] RATTANACHAI A,HIRONO I,OHIRA T,et al.Cloning of kuruma prawn Marsupenaeus japonicus crustin-like peptide cDNA and analysis of its expression[J].Fisheries Science,2004,70(5):765-771.
- [23] SPERSTAD S V,HAUG T,PAULSEN V,et al.Characterization of crustins from the hemocytes of the spider crab,Hyas araneus,and the red king crab,Paralithodes camtschaticus[J].Developmental & Comparative Immunology,2009,33(4):583-591.
- [24] YUE F,PAN L Q,MIAO J J,et al.Molecular cloning,characterization and mRNA expression of two antibacterial peptides:crustin and anti-lipopolysaccharide factor in swimming crab Portunus trituberculatus[J].Comparative Biochemistry and Physiology Part B:Biochemistry and Molecular Biology,2010,156(2):77-85.
- [25] JIANG H S,SUN C,WANG T,et al.A single whey acidic protein domain containing protein(SWD)inhibits bacteria invasion and dissemination in shrimp Marsupenaeus japonicus[J].Fish & Shellfish Immunology,2013,35(2):310-318.
- [26] LATHAM P W.Therapeutic peptides revisited[J].Nature Biotechnology,1999,17(8):755-757.
- [27] KRUSONG K,POOLPIPAT P,SUPUNGUL P,et al.A comparative study of antimicrobial properties of CrustinPm1 and CrustinPm7 from the black tiger shrimp Penaeus monodon[J].Developmental & Comparative Immunology,2012,36(1):208-215.