(厦门大学化学化工学院,福建 厦门 361005)
(College of Chemistry and Chemical Engineering,Xiamen University,Xiamen 361005,China)
DOI: 10.6043/j.issn.0438-0479.201803052
备注
光催化降解染料废水作为安全的、环境友好的技术越来越受世人关注,但目前研究制备的光催化剂仍存在性能不稳定且难以高效再生等亟待解决的难题.基于此,以聚合紫罗碱(polyviologens,PV)和磷钼酸(H3PMo12O40,HPMo)为原料合成了磷钼酸-聚合紫罗碱(PMo-PV)复合材料,并将其作为载体负载Ag/AgBr催化剂,用于光催化降解甲基橙染料.由该法制备的Ag/AgBr/PMo-PV催化剂具有较高的比表面积和丰富的介孔结构,在光催化降解甲基橙反应中活性优于Ag/AgBr催化剂和商业TiO2 P25催化剂,而且该催化剂在含有H2O2条件下多次重复反应后仍保持着很高的活性,其重复稳定性远大于Ag/AgBr催化剂.
Photocatalytic degradation of dyes wastewater as a safe and environmentally friendly technology has attracted worldwide attention.However,currently there is still lack of photocatalysts that can be efficiently regenerated with stable performance.In this study,the polyviologen(PV)and phosphomolybdic acid(HPMo)composite PMo-PV was designed and synthesized as the Ag/AgBr catalyst for photocatalytic degradation of methyl orange dyes.The prepared Ag/AgBr/PMo-PV with high surface area and abundant porous structure showed its high photocatalytic activity,better than the Ag/AgBr and commercial TiO2 P25 catalysts.Furthermore,in the presence of H2O2,Ag/AgBr/PMo-PV catalyst remained high catalytic activity after repeated catalytic reactions and also showed much better reproducibility than the Ag/AgBr catalyst.
引言
Ag/AgBr是一种较为常用的降解染料废水的光催化剂,其主要缺点是易被光腐蚀还原成Ag单质.目前解决Ag/AgBr光腐蚀问题主要有两种方法:一种方法是改变其本身的结构,利用不同于传统光催化的机理进行光催化[1-2]; 另一种方法则是将Ag/AgBr与其他材料复合,利用良好的电子传导材料将AgBr受到光激发而产生的表面电子捕获,以避免光腐蚀[3-4].
杂多酸(polyoxometalate,POM)是良好的接受和给予电子的载体[5],但是单独作为光催化剂时活性较差,这是因为POM本身易形成稳定还原态,而还原态POM的还原能力有限,较难活化氧化剂而导致其失去氧化活性.若POM与其他导带电位高于还原态POM的半导体材料复合,则可将半导体材料导带上的电子吸收并转移到自身的导带上,使得其进一步激发,进而还原O2,得到过氧自由基.同时,所复合的半导体材料若能及时提供所需的光生电子,就能形成一个完整的电子传导链,大大提高电子效率.如果将POM与Ag/AgBr复合,不仅能解决Ag/AgBr的光腐蚀问题,还弱化了POM在光催化领域的局限性; 但是由于Ag+和Br-的相互作用力强于和POM的作用,游离的POM很容易流失.因此,寻求一种可紧密结合并有效分散POM的阳离子聚合物,与POM结合形成稳定的复合材料[6]作为Ag/AgBr的载体,是制备性能稳定的高效光催化剂的关键.
聚合紫罗碱(polyviologens,PV)是一种有着良好接受电子能力和氧化还原活性的阳离子聚合物[7].Chen等[6]通过离子自组装方法,在水中利用磷钼酸(H3PMo12O40,HPMo)与直链PV制备了具有离子网络框架和介孔结构的磷钼酸-聚合紫罗碱(PMo-PV)复合材料.目前PMo-PV复合材料还未见用于光催化领域的报道,但该复合材料具有较高的比表面积,其多孔结构更易使光激发产生的电子和空穴到达光催化材料表面参与反应,提高量子转换效率[8].此外,若材料孔径与光的波长在同一数量级上,其孔道结构可以增加光散射,多次内部反射可能会产生级联效应,增强孔内活性位点的照明,从而提高光催化效率[9].
本研究以PV和HPMo为原料合成了PMo-PV复合材料,并将其作为载体负载Ag/AgBr催化剂,研究其光催化降解甲基橙染料废水的性能,并探讨该复合光催化剂的催化活性及稳定性.
1 实验部分
1.1 试 剂溴化钠(NaBr,纯度≥99.0%)、硝酸银(AgNO3,纯度≥99.8%)、HPMo(纯度≥99%)、无水乙醇(纯度≥99.7%)、异丙醇(纯度≥99.7%)、硝酸(HNO3,质量分数65%~68%)、溴化十六烷三甲基铵(CTAB,纯度≥99.7%)和甲基橙(纯度≥99%)购于国药集团化学试剂有限公司; 对二溴苄和4,4'-联吡啶购于上海阿达玛斯试剂有限公司; 过氧化氢(H2O2,质量分数30%)购于广东光华科技股份有限公司; TiO2 P25纳米催化剂(纯度≥99.5%)购于Evonik Degussa公司.
1.2 仪器设备氮气吸附-脱附测试采用美国Micromeritics ASAP2020全自动物理吸附仪; 孔径分布计算采用BJH(Barrett-Joyner-Halenda)法; X射线小角衍射测试采用日本Rigaku Ultima Ⅳ X射线衍射(XRD)仪:测试角度20°~80°,扫描速度10(°)/min; 产物形貌采用Zeiss Sigma扫描电镜(SEM)表征; 光源采用北京中教金源科技有限公司的CEL-HXF300氙灯光源系统.
1.3 催化剂的制备1.3.1 PMo-PV的制备[6]
将一定量的4,4'-联吡啶、对二溴苄和乙醇混合溶解,在85 ℃下加热回流24 h后,离心除去上清液; 再用乙醇多次洗涤至上清液透明; 最终除去上清液得到固体沉淀,在80 ℃下真空干燥12 h得到PV.
将一定量的PV和HPMo分别溶于10和30 mL pH 1.0的HNO3溶液中; 然后将30 mL HPMo溶液缓慢滴加入10 mL PV溶液中,搅拌20 h后离心除去上清液; 再用pH 1.0的HNO3溶液多次洗涤,直至上清液中滴加AgNO3溶液无沉淀产生为止; 最后将所得固体沉淀在80 ℃下真空干燥12 h,得到PMo-PV复合材料颗粒.
1.3.2 Ag/AgBr/PMo-PV的制备将一定量的PMo-PV、AgNO3和NaBr分别溶于40,10和1 mL水中,然后将10 mL AgNO3溶液缓慢滴加到40 mL PMo-PV溶液中搅拌1 h,再缓慢滴加入1 mL NaBr溶液搅拌2 h; 再滴加1 mL异丙醇,用氙灯(I=20 mA)光照0.5 h,离心除去上清液,用乙醇多次洗涤; 除去上清液后,将所得固体沉淀在80 ℃下真空干燥0.5 h得到Ag/AgBr/PMo-PV固体颗粒.
1.3.3 Ag/AgBr的制备将一定量的AgNO3和CTAB分别溶于20和30 mL水中,然后将30 mL CTAB溶液缓慢滴加入20 mL AgNO3溶液中搅拌2 h; 再往混合溶液中滴加1 mL异丙醇,接着用氙灯(I=20 mA)光照0.5 h后,离心除去上清液,用乙醇多次洗涤; 除去上清液后,将所得固体沉淀在80 ℃下真空干燥0.5 h得到Ag/AgBr固体颗粒.
本实验还以同样的方法制备了以NaBr为溴源的Ag/AgBr催化剂(记为Ag/AgBr-NaBr).相较于以CTAB为溴源的Ag/AgBr催化剂,Ag/AgBr-NaBr催化剂的颗粒较大,分散性也较差.
1.4 染料光催化反应空气条件下的光催化反应:1)取0.025 g 催化剂固体于100 mL烧杯中,加入49.5 mL pH 2.3的HNO3溶液,再滴加0.5 mL 1 g/L的甲基橙溶液,用锡箔纸将烧杯整体包住,遮光条件下暗平衡吸附15 min; 2)打开氙灯光源进行预热,调整I=20 mA,装上滤光片(使λ > 400 nm的光可以透过),同时打开程控型加热制冷循环器,将温度设定为20 ℃; 3)将暗平衡好的样品去掉锡箔纸放置在灯片下,打开搅拌器并按下光照按钮,开始反应,分别于0,5,10,15,20,25,30 min时吸取2 mL溶液于2 mL离心管中,置于不透光的盒子里,反应30 min后离心,保留底部固体颗粒,用紫外-可见光分光光度计测定上清液的吸光度; 4)继续光照,直至烧杯中残留的染料完全降解,接着将离心得到的固体颗粒用13.5 mL pH 2.3的HNO3溶液洗到烧杯中,并加入0.5 mL 1 g/L的甲基橙溶液,用锡箔纸将烧杯整体包住,遮光条件下暗平衡吸附15 min,重复步骤2)~4).
H2O2条件下的光催化反应:往反应溶液中加入0.01 mL 30% H2O2,其他实验操作与空气条件下的光催化反应相同.
2 结果与讨论
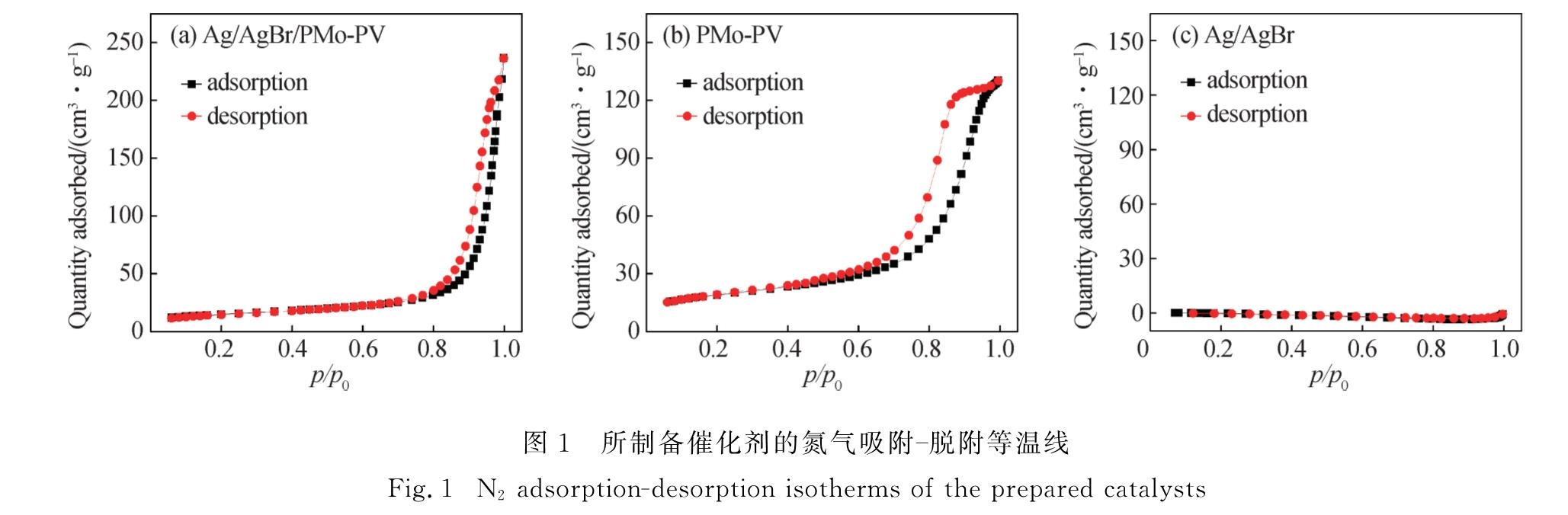
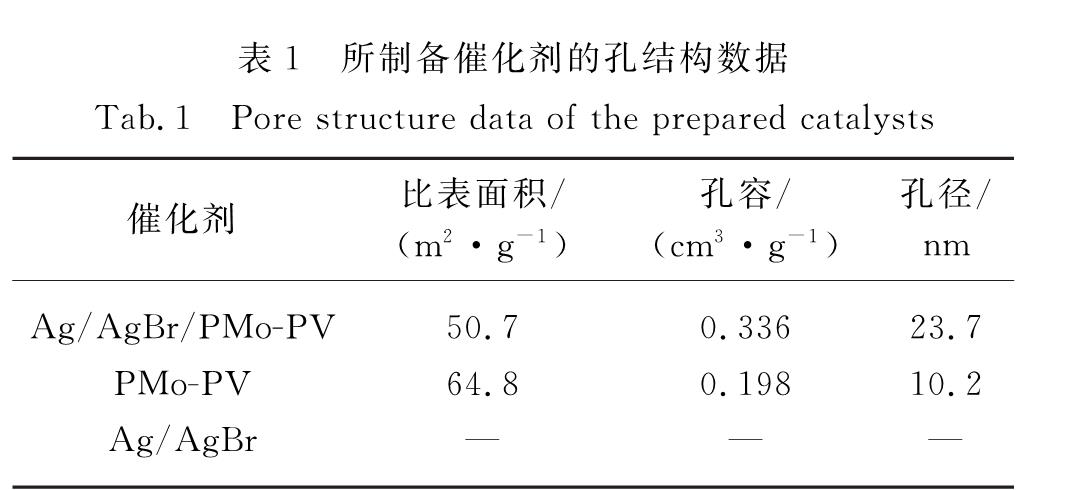
2.1 催化剂的表征图1和2分别为制备的3种催化剂的低温氮气吸附-脱附等温线和SEM图.由图1可知:当气压比较低(p/p0<0.8)时,Ag/AgBr/PMo-PV和PMo-PV的吸附量随气压比升高增长缓慢; 当气压比较高(p/p0≥0.8)时二者的吸附量则随之陡增,均呈现出Ⅴ型吸附等温线,表明二者均具有微孔少、介孔多的结构特点; 而且它们的吸附-脱附曲线中均存在类似H1型的迟滞回线.此外,从图2(a)和(b)可以看出Ag/AgBr/PMo-PV和PMo-PV都含有丰富的不规则孔道,孔道骨架由微小颗粒相互黏连堆砌而成,表明二者均具有孔径分布相对较窄的结构特征[10].Ag/AgBr/PMo-PV和PMo-PV的孔结构数据如表1所示,负载Ag/AgBr后导致催化剂的比表面积下降,孔容增大,孔径提高.其原因在于负载Ag/AgBr的过程中部分PMo-PV溶解在溶液中,并重新组装形成了新的孔结构[7].而由图1(c)和2(c)可知,Ag/AgBr催化剂为粒径分布不均匀的微米级不规则颗粒,几乎没有介孔和微孔结构,在氮气吸附-脱附测试中也未测得其比表面积和孔容数据.
图1 所制备催化剂的氮气吸附-脱附等温线
Fig.1 N2 adsorption-desorption isotherms of the prepared catalysts图2 催化剂Ag/AgBr/PMo-PV(a)、PMo-PV(b)和Ag/AgBr(c)的SEM图
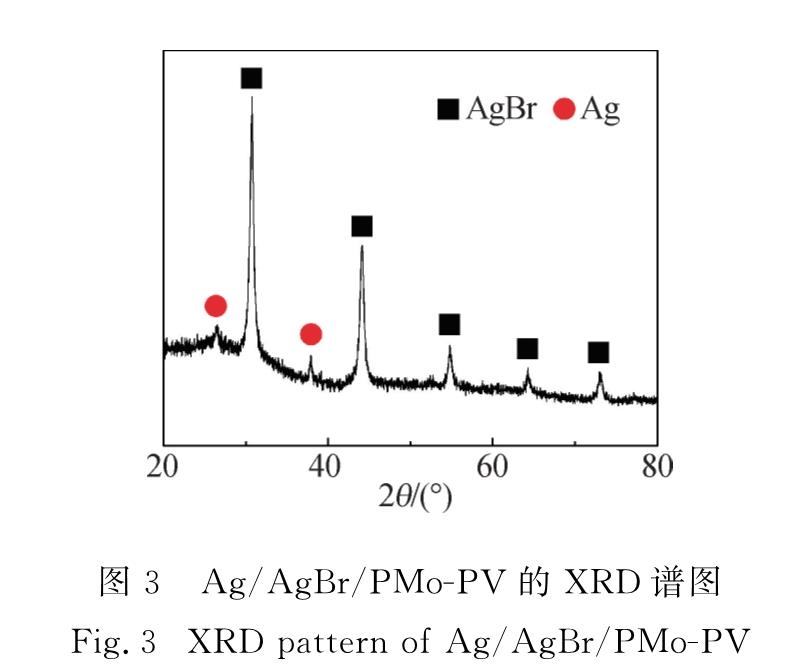
Fig.2 SEM images of Ag/AgBr/PMo-PV(a), PMo-PV(b)and Ag/AgBr(c)catalysts图3为Ag/AgBr/PMo-PV的XRD谱图,可以看出Ag/AgBr/PMo-PV具有明显的峰型,说明其具有明显的晶体结构.其中,大部分为AgBr,少量为Ag单质.含少量Ag单质的原因可能是在制备过程中,样品液在0.5 h的光照期间有一小部分AgBr发生光腐蚀生成Ag单质.
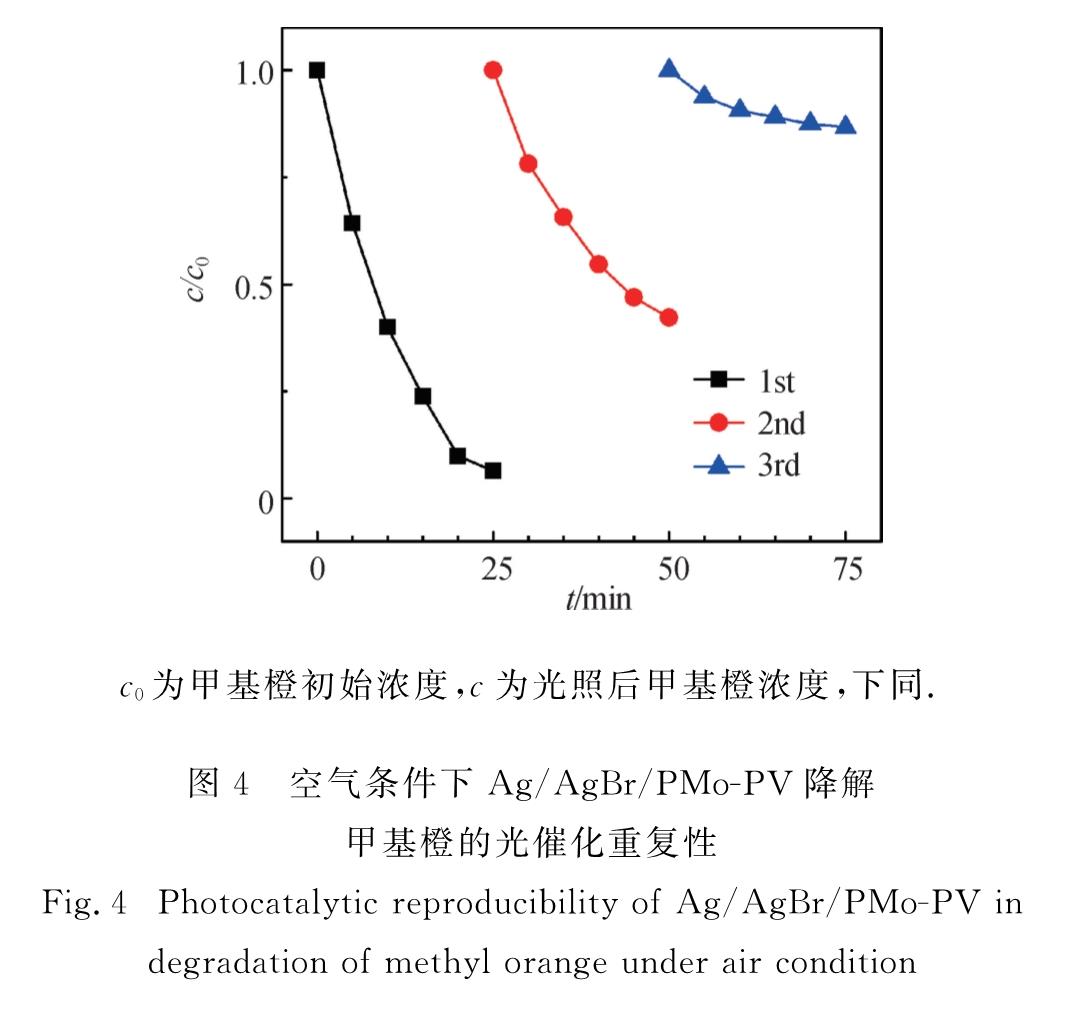
2.2 光催化反应降解甲基橙在空气条件下,采用制备的Ag/AgBr/PMo-PV催化剂进行了3次降解甲基橙的光催化反应重复性实验,结果如图4所示.在第1次光催化反应中甲基橙经25 min后几乎完全降解,而目前商业化TiO2 P25纳米催化剂在同等条件下完全降解甲基橙则需2 h,证明本文中制备的Ag/AgBr/PMo-PV催化剂的催化活性更高; 而在第2次和第3次重复使用该催化剂的实验中,其催化降解甲基橙的速率显著下降,表明该催化剂的重复稳定性较差.这可能是由于POM与O2的结合能力差,导致电子难以从POM传递给O2,使得大量积聚在POM上的电子只能回传给AgBr,进而导致AgBr被光腐蚀还原成Ag单质,失去了光催化活性.
c0为甲基橙初始浓度,c为光照后甲基橙浓度,下同.
图4 空气条件下Ag/AgBr/PMo-PV降解甲基橙的光催化重复性
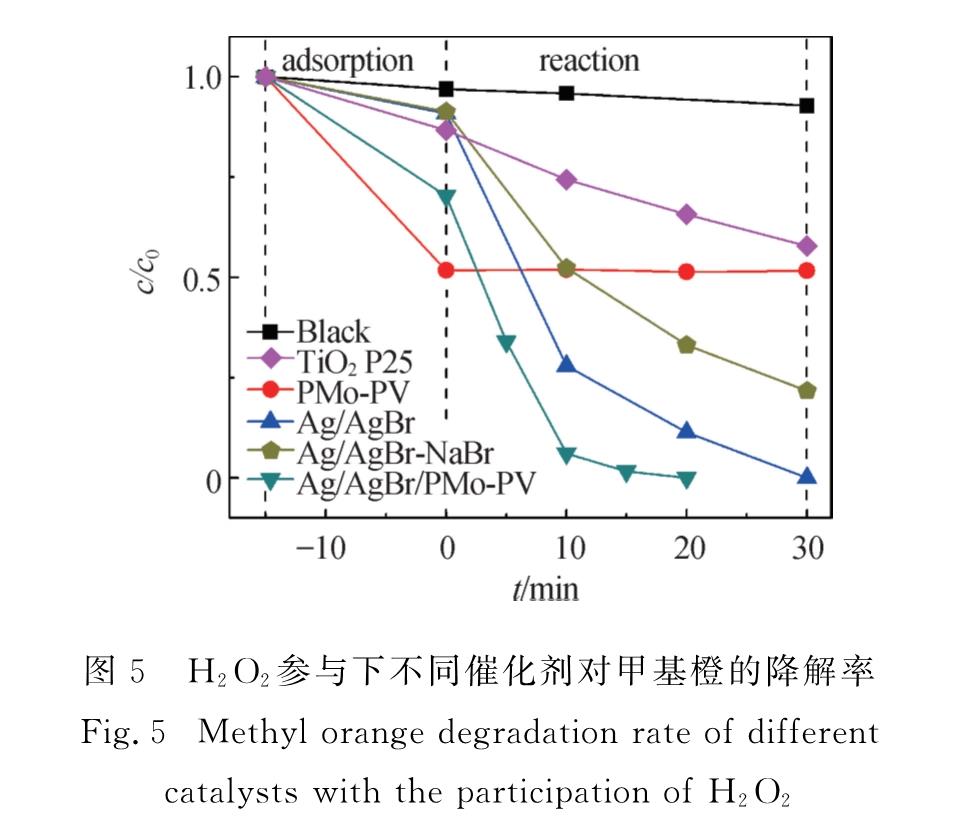
Fig.4 Photocatalytic reproducibility of Ag/AgBr/PMo-PV in degradation of methyl orange under air condition针对上述催化剂的光腐蚀问题,引入了更容易与POM结合的H2O2,使POM上的电子更容易传导出来.所制备的不同催化剂对甲基橙的光催化降解实验结果如图5所示.可以看出:虽然H2O2对甲基橙有一定的降解能力,但由于本实验中甲基橙浓度较大,H2O2添加量很少,所以在30 min的反应时间内H2O2几乎无法单独降解甲基橙; PMo-PV对甲基橙的吸附能力较强,但对甲基橙不具备降解能力; Ag/AgBr由于比表面积低,所以对甲基橙的吸附能力较差,但表现出较高的光催化活性,反应
图5 H2O2参与下不同催化剂对甲基橙的降解率
Fig.5 Methyl orange degradation rate of different catalysts with the participation of H2O230min后甲基橙即完全降解; 以NaBr为溴源的Ag/AgBr-NaBr由于颗粒大,分散性差,其催化活性不如以CTAB为溴源的Ag/AgBr; 与Ag/AgBr相比,Ag/AgBr/PMo-PV对甲基橙的吸附能力有了很大的提高,且表现出更高的光催化活性,反应20 min后即可完全降解甲基橙.
虽然Ag/AgBr和Ag/AgBr/PMo-PV都表现出了优良的降解甲基橙的光催化活性,但是Ag/AgBr自身容易因光生电子的还原而受到腐蚀,所以稳定性一直是该类型催化剂有待提高的重要指标.为了进一步探讨PMo-PV载体对Ag/AgBr稳定性的影响,本研究分别对Ag/AgBr和Ag/AgBr/PMo-PV催化剂进行重复性实验,结果如图6所示.
图6 H2O2参与下Ag/AgBr和Ag/AgBr/PMo-PV降解甲基橙的光催化重复性
Fig.6 Photocatalytic reproducibility of Ag/AgBr and Ag/AgBr/PMo-PV in degradation of methyl orange with the participation of H2O2从图中可以看出,经过连续4次30 min的光催化反应,Ag/AgBr对甲基橙的降解率分别为100%,77%,58%和47%,其催化活性随着重复次数的增加而明显降低,说明Ag/AgBr催化剂在降解甲基橙的过程中容易被腐蚀,稳定性较差; 而Ag/AgBr/PMo-PV经过连续4次光催化反应,在每次反应20 min后其对甲基橙的降解率都接近100%,表明Ag/AgBr/PMo-PV催化剂在降解甲基橙的过程中具有催化活性高、稳定性好的特点.
3 结 论
针对目前染料废水污染的严重性及传统染料废水处理方法的局限性,本文中设计合成了一种PMo-PV复合材料,并将其作为载体负载Ag/AgBr催化剂,用于光催化降解甲基橙染料.制备的Ag/AgBr/PMo-PV催化剂含有丰富的不规则孔道,且具有微孔少、介孔多的晶体结构.在含有H2O2 条件下,Ag/AgBr/PMo-PV光催化降解甲基橙的重复稳定性明显优于空气条件下,并且远优于Ag/AgBr催化剂; 在含有H2O2条件下,Ag/AgBr/PMo-PV催化剂对甲基橙的降解率在20 min内即可接近100%,活性优于Ag/AgBr催化剂和商业TiO2 P25纳米催化剂.
- [1] WANG P,HUANG B B,ZHANG X Y,et al.Highly efficient visible-light plasmonic photocatalyst Ag@AgBr[J].Chemistry:A European Journal,2009,15(8):1821-1824.
- [2] KUAI L,GENG B Y,CHEN X T,et al.Facile subsequently light-induced route to highly efficient and stable sunlight-driven Ag-AgBr plasmonic photocatalyst[J].Langmuir,2010,26(24):18723-18727.
- [3] CHENG H F,HUANG B B,WANG P,et al.In situ ion exchange synthesis of the novel Ag/AgBr/BiOBr hybrid with highly efficient decontamination of pollutants[J].Chemical Communications,2011,47(25):7054-7056.
- [4] WANG P,HUANG B B,QIN X Y,et al.Ag/AgBr/WO3·H2O:visible-light photocatalyst for bacteria destruction[J].Inorganic Chemistry,2009,48(22):10697-10702.
- [5] TACHIKAWA T,TOIO S,FUJITSUKA M,et al.One-electron redox processes during polyoxometalate-mediated photocatalytic reactions of TiO2 studied by two-color two-laser flash photolysis[J].Chemistry:A European Journal,2006,12(11):3124-3131.
- [6] CHEN G J,HOU W,LI J,et al.Ionic self-assembly affords mesoporous ionic networks by crosslinking linear polyviologens with polyoxometalate clusters[J].Dalton Transactions,2016,45(11):4504-4508.
- [7] SUN J K,ZHANG J.Functional metal-bipyridinium frameworks:self-assembly and applications[J].Dalton Transactions,2015,44(44):19041-19055.
- [8] 范晓星,于涛,邹志刚.介孔TiO2的材料合成及其在光催化领域的应用[J].功能材料,2006,37(1):6-9.
- [9] PARLETT C M A,WILSON K,LEE A F.Hierarchical porous materials:catalytic applications[J].Chemical Society Reviews,2013,42(9):3876-3893.
- [10] SING K S W,EVERETT D H,HAUL R A W,et al.Reporting physisorption data for gas solid systems with special reference to the determination of surface area and porosity[J].Pure and Applied Chemistry,1985,57(4):603-619.