(厦门大学化学化工学院,固体表面物理化学国家重点实验室,福建 厦门 361005)
(State Key Laboratory of Physical Chemistry of Solid Surfaces,College of Chemistry and Chemical Engineering,Xiamen University,Xiamen 361005,China)
fullerenes; arc discharge; crystallographic structure; isolated pentagon rule; formation mechanism
DOI: 10.6043/j.issn.0438-0479.201807016
备注
碳电弧放电法是合成富勒烯及其衍生物的最重要方法之一,但电弧反应过程复杂,涉及的衍生化机制尚不明确.采用电弧法合成含有氯化富勒烯的碳灰,借助高效液相色谱法对其进行分离、纯化,得到了符合独立五元环规则的氯化富勒烯#24106C78Cl6,结合X-射线单晶衍射、质谱、紫外-可见吸收光谱对其进行结构表征,证明#24106C78Cl6与已有的氯化物#24106C78Cl18、#24106C78Cl30在六并苯片段具有相同的氯原子加成[5,6,6]位点,同时也证明了在氯参与的碳电弧中,富勒烯在靠近电弧中心的较高温区发生氯化反应,而氯化碳簇的加成反应发生于更低的温区.
Arc discharge of carbon was one of the most important methods for the synthesis of fullerenes and their chlorinated derivatives.However,the arc reaction process was complicated and the involved derivatization mechanism was still unclear.Herein the carbon ash containing chlorinated fullerenes was synthesized using the carbon arc.Separated and purified with high performance liquid chromatography,the chlorinated fullerene #24106C78Cl6 conformed to the isolated pentagon rule was obtained.With X-ray single crystal diffraction,mass spectrometry and spectroscopy,#24106C78Cl6 was confirmed to have the same chlorine atom addition pattern as those of high chloride #24106C78Cl18 and #24106C78Cl30 at the [5,6,6] sites of the coronene segment.The capture of #24106C78Cl6 supported that the chlorination reaction occurred in the higher temperature zone near the center of the arc,whereas the addition reaction of the chlorinated carbon cluster occurred in the lower temperature zone in the complex chlorine-involving carbon arc.
引言
电弧放电法是合成富勒烯的重要手段[1],近20多年来,经多次改进后,内嵌富勒烯和外接富勒烯等新型富勒烯已可宏量合成[2-3].但电弧放电是一个复杂且激烈的过程,反应温度可达4 000 ℃以上,现有技术很难用于原位跟踪反应中间体,因此,研究碳电弧中富勒烯形成与衍生反应机制的难度很大.科学家们基于理论计算并结合气相实验来验证富勒烯C2插入的生长机制及C2丢失的收缩机制[4-10],然而,由于缺乏富勒烯形成过程及其衍生反应中间体的明确结构,富勒烯的形成机制尚不明确,所以通过富勒烯中间体的捕获从而更好地理解富勒烯的反应机制是十分必要的.
本课题组将四氯化碳引入到碳电弧中[11],合成并表征了数十种氯化富勒烯[2,12-22],这些结构的表征在一定程度上反映出电弧放电法合成富勒烯的反应中系列碳簇的生长过程,但是在这样复杂又激烈的体系中,很难得到直接的、原位的实验证据来证明富勒烯的形成与衍生化.最近,本课题组在碳电弧的碳灰产物中分离并表征了一例双重衍生化的#24106C78Cl6(C5Cl6)[23],该衍生物是迄今在碳电弧中捕获得到的唯一一例双功能化富勒烯,其结构的表征在实验上证明了全氯代环戊二烯(C5Cl6)这类全氯代碳簇确实存在于电弧放电的低温区; 结合理论计算,进而研究了氯代碳簇、氯原子与富勒烯之间的衍生化顺序,推进了对极端条件下富勒烯衍生化反应机制的理解,以C78作为代表性富勒烯用于研究复杂碳电弧反应过程的范例也因此彰显.
从拓扑学上来说,仅由五元环和六元环组成的高富勒烯C78家族中含有5个满足独立五元环规则(isolated pentagon rule,IPR)的异构体[24],包括D3-#24105C78、C2v-#24106C78、C2v-#24107C78、D3h-#24108C78和D3h-#24109C78[25].到目前为止,D3-#24105C78、C2v-#24106C78、C2v- #24107C78和D3h-#24109C78(其命名规则参见文献[25])这4个IPR-C78异构体已获得明确的结构表征,其中前3个异构体相对比较稳定,能够以空笼的形式通过高效液相色谱法直接分离,此外还可以不同的衍生物形式被分离和表征[26-29]; 而D3h-#24108C78由于溶解度非常差,到目前为止还没有被表征出来.对于富勒烯的分离,最常用、最有效的方法还是高效液相色谱法,但有时也可以根据异构体之间性质的差异,达到快速分离的目的.例如,根据D3-#24105C78与C2v-#24106C78这2个异构体在光化学反应活性上的差异[30],与1,1,2,2-四苯基-1,2-二硅烷在光照下进行环加成反应,只有C2v-#24106C78能够发生环加成反应,之后再用高氯酸盐脱去硅烷,从而达到分离这2个异构体的目的.
除了电弧放电法之外,还可以采用传统的化学方法来合成氯化富勒烯及其中间体.关于富勒烯C78在化学反应方面的研究,主要进行环丙烷化、卤化、三氟甲基化及其他的相关反应,并用1H、13C和19F核磁共振波谱(NMR)和单晶结构进行C78衍生物的表征.高富勒烯C78进行溴代反应可得到#24106C78Br18和#24107C78Br18[31],氯代反应可得到#24106C78Cl18、#24107C78Cl18、#24109C78Cl18、#24105C78Cl30和#24107C78Cl30 [27,32],三氟甲基化可得到#24105C78(CF3)10-18[33]、#24106C78(CF3)10,12[26]、#24107C78(CF3)8,12,14[26]和#24109C78(CF3)12 [28]以及五氟乙烷化的产物#24106C78(C2F5)10[34].其中由于#24109C78的带隙比较小,导致溶解度比较低,很难从碳灰的混合物中直接分离,但可以通过三氟甲基化增加溶解度,从而被成功地表征.
另外,IPR-C78异构体除了外接衍生化,还可以内嵌金属富勒烯的形式被表征.Olmstead等[35]成功合成并分离出Sc3N@#24109C78,并且该结构与八乙基卟啉镍以共晶的形式通过X-射线单晶衍射被明确表征.Cao等[36]通过紫外及13C-NMR,并结合理论计算,分离并表征了La2@#24109C78.Zhao等[37]结合密度泛函理论对Sc2O@C78进行系统研究,发现Sc2O@#24106C78与Sc2O@#24109C78通过一步Stone-Wales转化可以实现相互转换.
本研究在四氯化碳的碳电弧中捕获了#24106C78Cl6,结合X-射线单晶衍射、多级质谱、紫外-可见吸收光谱等技术对其进行了结构表征,明确了6个氯原子加成在六并苯[5,6,6]位点的C2v对称性分子结构,这一化合物的捕获为氯原子是先于氯化碳簇加成至裸露的碳笼上这一理论预测[23]提供了有力支持.
1 实验部分
2 结果与讨论
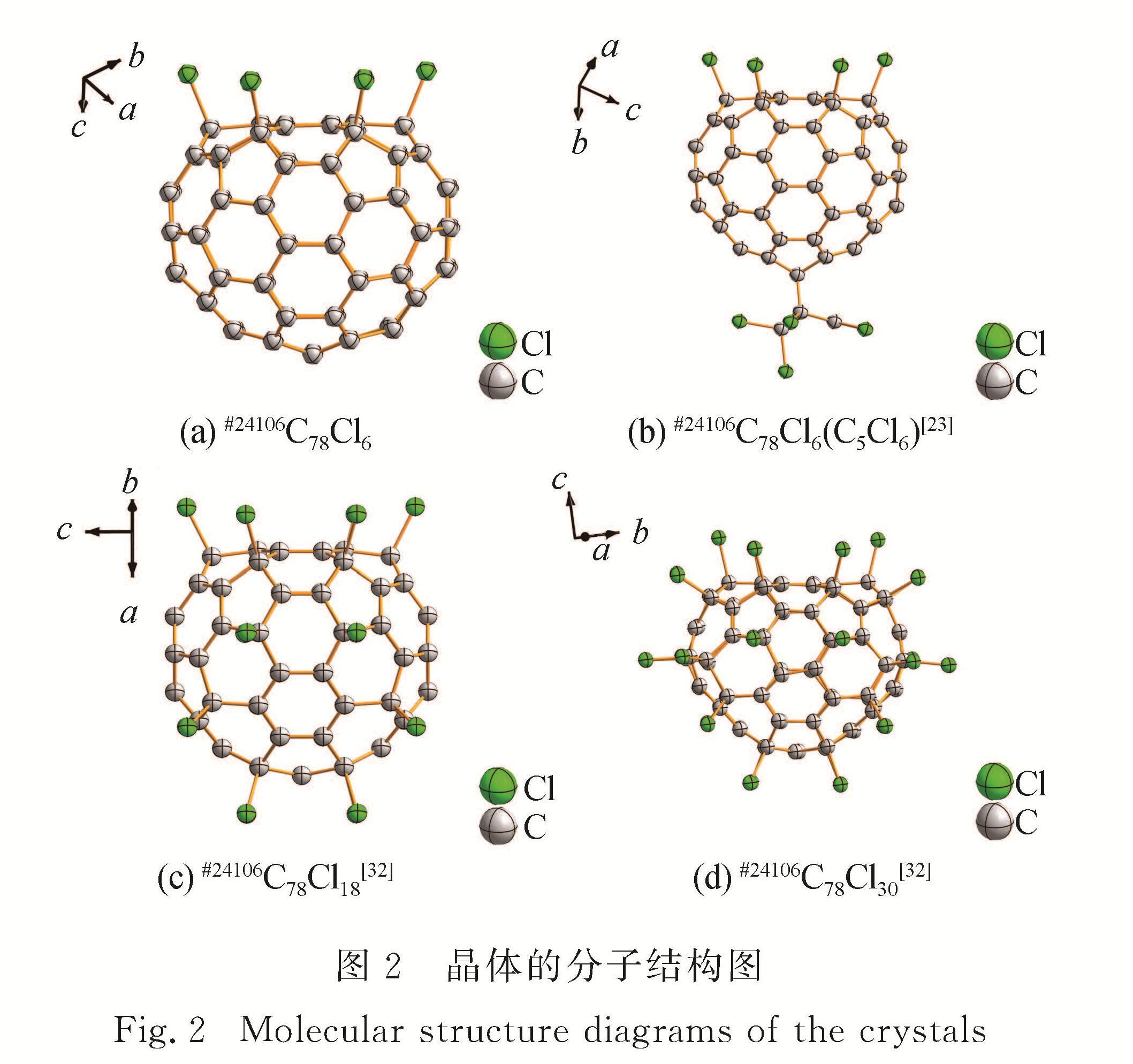
2.1 #24106C78Cl6的晶体结构分析#24106C78Cl6是从四氯化碳参与的电弧放电的碳灰的甲苯提取液中,通过高效液相色谱的多级分离得到的.缓慢挥发分离纯化后的#24106C78Cl6的甲苯溶液,得到晶型完整可表征的晶体.#24106C78Cl6的晶体数据如表1所示,该分子属于正交晶系,Pnma空间群,晶胞参数a=2.260 75 nm,b=1.557 33 nm,c=1.146 04 nm,α=90°,β=90°,γ=90°.由分子结构(图2)可得,#24106C78Cl6的对称性与其母笼#24106C78的对称性一致,都为C2v,6个氯原子依次键合在六并苯片段[5,6,6]位的碳原子上,形成一条sp3杂化的碳链,将母笼分割成一个具有芳香性苯型分子的片段和一个具有单双键交替的C66片段.这种加成模式很好地满足了局域芳香性的原理[24].
通过X-射线单晶衍射明确表征了#24106C78Cl6的单晶结构,该结构满足IPR,含有12个五元环和29个六元环,并且所有五元环都被六元环隔开.最近,本课题组通过X-射线单晶衍射确切表征出了双重衍生化#24106C78Cl6(C5Cl6)的几何结构[23],并结合密度泛函理论对其双重衍生化的加成顺序进行了推断,结果表明6个氯原子先键合至裸碳笼上,之后再进行全氯
表1 #24106C78Cl6的晶体参数
Tab.1 Crystallographic data of #24106C78Cl6代碳簇的环加成反应.#24106C78Cl6中间体的捕获恰好从实验的角度验证了之前理论计算推断的双重衍生化#24106C78Cl6(C5Cl6)的加成顺序,从而进一步支持了理论计算结果的准确性.#24106C78Cl6中6个氯原子键合顺序的相关理论计算部分之前已有报道[23],这里就不再赘述.
目前,#24106C78外接衍生物包括#24106C78(CF3)10,12[26]、#24106C78Br18[31]、#24106C78Cl18[29]和#24106C78Cl30[27,32],通过外接衍生化获得#24106C78的最高氯化物为#24106C78Cl30,并且推测氯化物#24106C78Cl18可能是高氯化物#24106C78Cl30的前驱体[32].由于#24106C78Cl6的氯原子键合位点和#24106C78Cl18、#24106C78Cl30都一样,所以捕获到的#24106C78Cl6极有可能是#24106C78Cl18和#24106C78Cl30的前驱体.
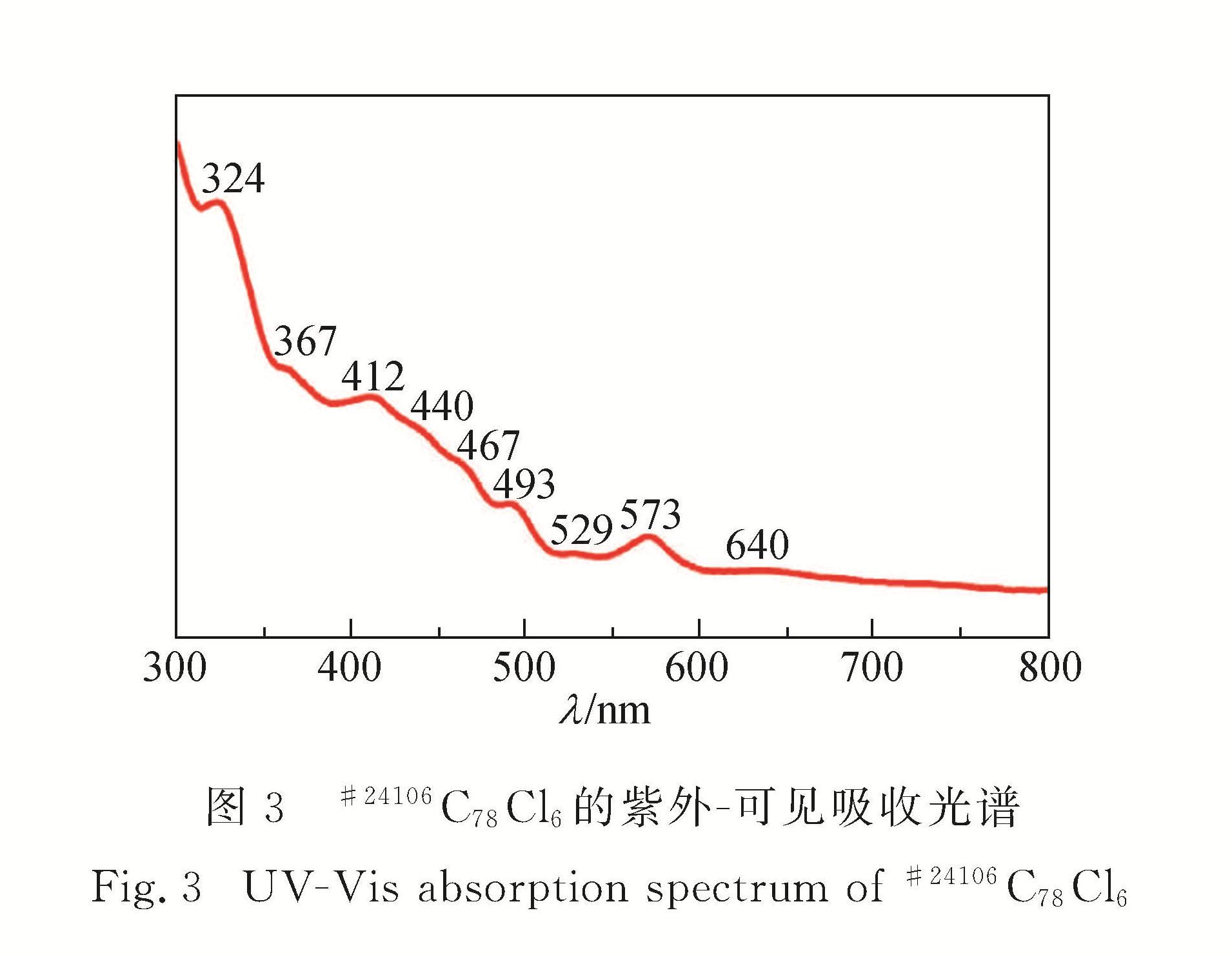
2.2 #24106C78Cl6的紫外-可见吸收光谱和质谱表征图3为高纯#24106C78Cl6的甲苯溶液的紫外-可见吸收光谱,可以看出,#24106C78Cl6的光谱呈现出比较宽的吸收范围,其主要吸收峰有324,367,412,440,467,493,529,573和640 nm,起始吸收波长为785 nm.
图3 #24106C78Cl6的紫外-可见吸收光谱
Fig.3 UV-Vis absorption spectrum of #24106C78Cl6对分离纯化后得到的#24106C78Cl6进行质谱表征.如图4中的插图所示,#24106C78Cl6质谱峰的同位素分布与理论计算模拟峰的同位素分布基本一致.此外,该质谱图中除了在m/z为1 146.2处有明显的信号峰之外,并无其他信号峰,表明样品#24106C78Cl6具有较高的纯度,获得了有效的分离.
图4 #24106C78Cl6的质谱图
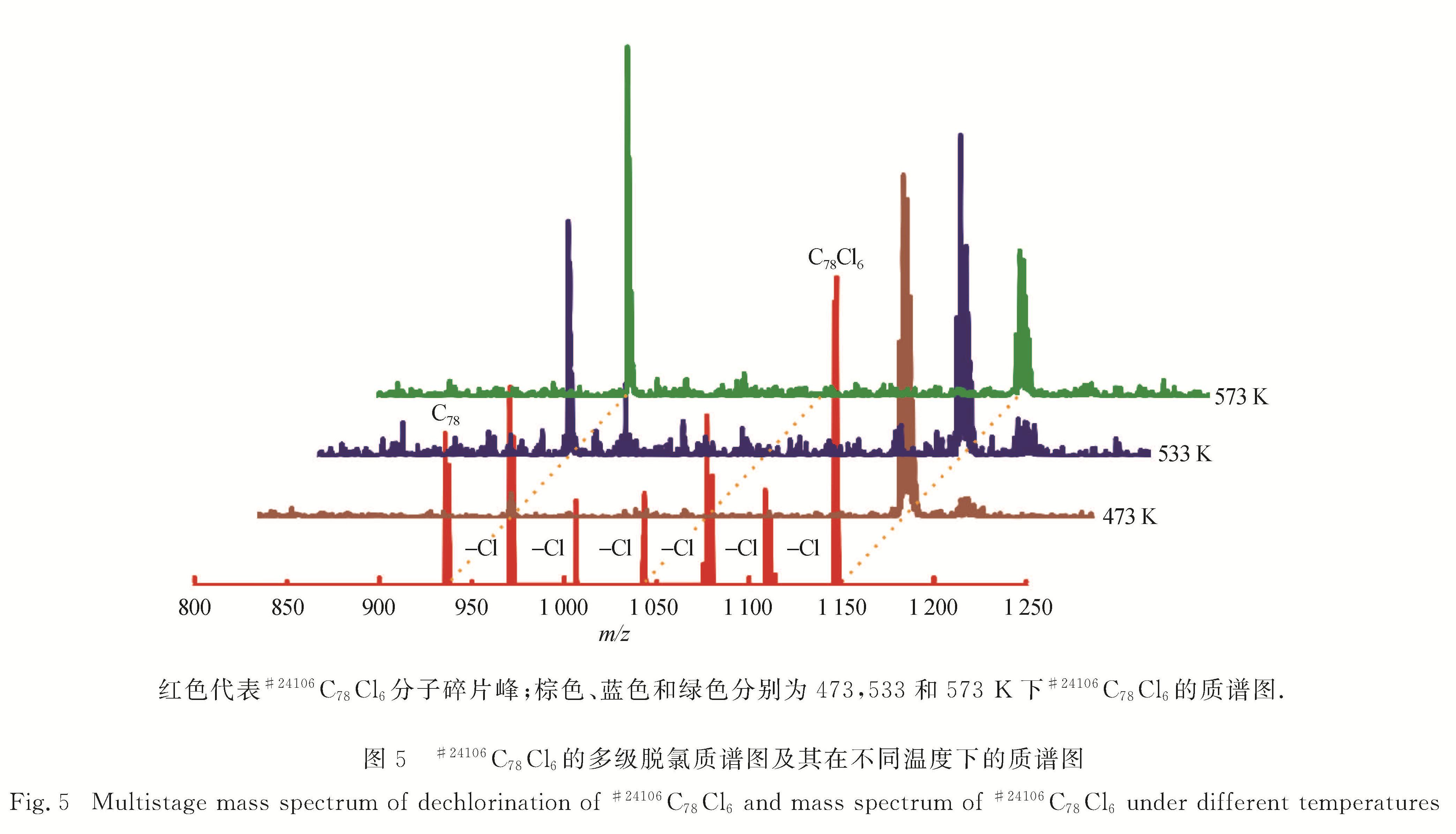
Fig.4 Mass spectrum of #24106C78Cl6富勒烯#24106C78由于满足IPR所以碳笼无需修饰就可以稳定存在,从其质谱表征结果(图5)来看,当离子化温度和蒸发温度都设置为473 K时,只出现m/z为1 146.2的信号峰,该质谱峰对应的分子式为#24106C78Cl6; 当离子化温度和蒸发温度增加到533 K时,出现的质谱峰信号m/z分别为1 146.2和936.4,对应的分子式分别为#24106C78Cl6和#24106C78,并且1 146.2 的信号强度要稍微强于936.4的信号强度; 当离子化温度和蒸发温度继续增加至573 K时,母笼#24106C78的信号强度反而要高于#24106C78Cl6.该结果表明温度时,#24106C78Cl6的信号占据主导地位,而在较高温度下,#24106C78Cl6中的6个氯原子容易离去,获得稳定的IPR-#24106C78母笼.
2.3 电弧反应中富勒烯的形成与衍生化机制碳电弧法是合成富勒烯及其氯化衍生物的最重要方法之一,但由于电弧反应过程复杂,涉及的衍生化机制尚不明确,通过富勒烯及其氯化衍生物中间体的捕获来研究富勒烯的形成机制就显得尤为重要.2011年,本课题组根据13C标记实验的质谱结果及电弧放电装置的温度红色代表#24106C78Cl6分子碎片峰; 棕色、蓝色和绿色分别为473,533和573 K下#24106C78Cl6的质谱图.
图5 #24106C78Cl6的多级脱氯质谱图及其在不同温度下的质谱图
Fig.5 Multistage mass spectrum of dechlorination of#24106C78Cl6 and mass spectrum of #24106C78Cl6 under different temperatures
分布模拟曲线[18],推断出富勒烯C68和其他富勒烯是在离电弧中心2~3 mm的高温区形成,而氯化碳簇则是在离电弧中心30~33 mm700~730 K的温度区间形成.最近,本课题组又捕获到双重衍生化的富勒烯#24106C78Cl6(C5Cl6)并对其形成过程进行了理论研究[23],结果表明氯原子是先加成到富勒烯C78六并苯的片段上,同时由于富勒烯具有亲二烯体的性质,生成的#24106C78Cl6与C5Cl6进一步发生Diels-Alder环加成反应; 此外,从分子动力学的角度分析表明,#24106C78Cl6(C5Cl6)结构中的C5Cl6基团在高温区(800~1 000 K)要比#24106C78Cl6中的氯原子更容易离去,即C—(C5Cl6)键弱于C—Cl键.这些研究结果从理论上推测6个氯原子在#24106C78上的加成反应发生在C5Cl6的环加成反应之前,不同温度下的质谱实验数据也验证了这一理论预测.然而,这些关于#24106C78Cl6(C5Cl6)加成顺序的研究仅局限于理论计算而缺乏实验数据的支持,若能够获得中间体#24106C78Cl6的确切结构将会使得双重衍生化的反应机制更具说服力.本研究成功表征了富勒烯氯化中间体#24106C78Cl6,该结构的表征不仅从实验上证实了氯原子是先于C5Cl6加成至碳笼上,同时也表明了氯化反应发生在靠近电弧中心的较高温区,而氯化碳簇官能团的加成反应发生于较低温区.随着越来越多的富勒烯中间体被表征,碳电弧放电法合成富勒烯及其氯化衍生物的机制有望被逐渐揭开.
3 结 论
本研究通过高效液相色谱法分离并结合X-射线单晶衍射、质谱和紫外-可见吸收光谱,明确表征了碳电弧放电合成的碳灰中#24106C78Cl6的几何结构,该结构中氯原子的加成模式符合局域芳香性原理.该结构的表征可从实验上验证#24106C78Cl6(C5Cl6)双重衍生化的加成过程,支持氯原子是先于C5Cl6加成到碳笼上的理论研究结果.此外,#24106C78Cl6中6个氯原子的加成位点与富勒烯氯化物#24106C78Cl18、#24106C78Cl30相似,都是加成在六并苯片段[5,6,6]位的碳原子上,因此,该结构也可能是#24106C78更高氯化物的前驱体.总之,本研究对#24106C78Cl6的捕获与结构表征有利于理解复杂的碳电弧反应中富勒烯的衍生化过程,例证了在氯参与的碳电弧反应过程中,富勒烯首先在靠近电弧中心的较高温区发生氯化反应,而C5Cl6等氯化碳簇的加成反应发生于较低温区.
1.1 试剂和仪器甲苯和二硫化碳均为分析纯,购自厦门绿茵试剂玻仪有限公司.
LC908W-C60型可循环高效液相色谱仪,Bruker HCT 液相质谱仪,Bruker Smart APEX CCD单晶X-射线衍射仪,EYELA OSB-2100旋转蒸发仪,Shimadzu 2550型紫外可见-近红外吸收光谱仪.
Cosmosil色谱柱:Buckyprep[10 mm(i.d.)×250 mm], Buckyprep-M[10 mm(i.d.)×250 mm], 5-PBB[10 mm(i.d.)×250 mm].
1.2 合成与分离1.2.1 氯化富勒烯碳灰的合成和提取首先,参照文献[11-12]中的方法合成氯化富勒烯碳灰,再以甲苯为溶剂进行多次超声提取,直至提取液接近无色为止,合并提取液并浓缩,待纯化.
1.2.2 #24106C78Cl6的高效液相色谱分离采用高效液相色谱法对上述浓缩样品进行分离、纯化,具体步骤(图1)如下:1)在常温下以甲苯为流动相,流速为4 mL/min,用Buckyprep-M色谱柱分离,收集保留时间为11.9~16.7 min之间的组分,富集、浓缩; 2)采用5-PBB色谱柱,将流速调至6 mL/min,除去大部分的C60和C70,收集保留时间为6.3~9.0 min之间的组分,富集、浓缩; 3)采用Buckyprep-M色谱柱,将流速调至4 mL/min,收集保留时间为45.0~49.1 min之间的组分,富集、浓缩; 4)采用5-PBB色谱柱,通过4次循环分离,收集图1(d)阴影部分的样品; 5)用Buckyprep色谱柱进行13次循环分离,最终获得高纯的#24106C78Cl6样品.
1.2.3 挥发法培养#24106C78Cl6晶体将分离纯化后的#24106C78Cl6样品溶解在甲苯中,由于该样品在甲苯中的溶解度较低,浓缩至样品溶液颜色由浅绿色至绿色即可,以免样品析出影响晶体结晶; 再将其转移至洁净的小试管中用封口膜封好,将其静置于柜子中约一个月; 待#24106C78Cl6的甲苯溶液缓慢挥发干后,在小试管管壁及底部有晶体析出,得到#24106C78Cl6单晶.
色谱图中阴影标注的区域为需收集的色谱组分.
图1 #24106C78Cl6的多级循环高效液相色谱分离流程图
Fig.1 Flow diagram of multistage cycle HPLC chromatograms for the separation of #24106C78Cl61.3 样品的表征晶体结构表征:在光学显微镜下挑选合适尺寸的晶体放在Loop环上,采用Bruker Smart APEX CCD单晶X-射线衍射仪于100 K温度下测试.该仪器采用镜面单色器单色化的Cu Kα(λ=0.154 84 nm)作为入射光源,以ω-2θ扫描方式收集衍射点.收集得到的衍射数据采用CrysAlisPro(multi-scan)软件吸收校正,结构解析和精修采用OLEX2软件中SHELXS-2015和SHELXL-2015程序.
质谱表征:采用Bruker HCT液相质谱仪,大气压化学电离源(APCI),雾化气体压力275.8 kPa,干燥气体流速4 L/min,干燥气体温度250 ℃,APCI气化温度300 ℃,检测模式为负离子,优化检测离子质量数为1 000.
紫外-可见吸收光谱表征:采用Shimadzu 2550型紫外可见-近红外吸收光谱仪,扫描范围200~1 000 nm.
- [1] KRÄTSCHMER W,LAMB L D,FOSTIROPOULOS K,et al.Solid C60:a new form of carbon[J].Nature,1990,347(6291):354-358.
- [2] TAN Y Z,XIE S Y,HUANG R B,et al.The stabilization of fused-pentagon fullerene molecules[J].Nat Chem,2009,1(6):450-460.
- [3] POPOV A A,YANG S,DUNSCH L.Endohedral fullerenes[J].Chem Rev,2013,113(8):5989-6113.
- [4] HEATH J R.Synthesis of C60 from small carbon clusters[J].ACS Symp Ser,1992,481:1-23.
- [5] HUA X,CAGIN T,CHE J,et al.QM(DFT)and MD studies on formation mechanisms of C60 fullerenes[J].Nanotechnology,2000,11(2):85-88.
- [6] KHAN S D,AHMAD S.Modelling of C2 addition route to the formation of C60[J].Nanotechnology,2006,17(18):4654-4658.
- [7] CURL R F,LEE M K,SCUSERIA G E.C60 buckminster fullerene high yields unraveled[J].J Phys Chem A,2008,112(46):11951-11955.
- [8] SAHA B,IRLE S,MOROKUMA K.Hot giant fullerenes eject and capture C2 molecules:QM/MD simulations with constant density[J].J Phys Chem C,2011,115(46):22707-22716.
- [9] DUNK P W,MULET-GAS M,NAKANISHI Y,et al.Bottom-up formation of endohedral mono-metallofullerenes is directed by charge transfer[J].Nat Commun,2014,5:5844.
- [10] MULET-GAS M,ABELLA L,DUNK P W,et al.Small endohedral metallofullerenes:exploration of the structure and growth mechanism in the Ti@C2n(2n=26-50)family[J].Chem Sci,2015,6(1):675-686.
- [11] GAO F,XIE S Y,HUANG R B,et al.Significant promotional effect of CCl4 on fullerene yield in the graphite arc-discharge reaction[J].Chem Commun,2003(21):2676-2677.
- [12] XIE S Y,GAO F,LU X,et al.Capturing the labile fullerene[50] as C50Cl10[J].Science,2004,304(5671):699.
- [13] HAN X,ZHOU S J,TAN Y Z,et al.Crystal structures of saturn-like C50Cl10 and pineapple-shaped C64Cl4:geometric implications of double- and triple-pentagon-fused chlorofullerenes[J].Angew Chem Int Ed,2008,47(29):5340-5343.
- [14] TAN Y Z,HAN X,WU X,et al.An entrant of smaller fullerene:C56 captured by chlorines and aligned in linear chains[J].J Am Chem Soc,2008,130(46):15240-15241.
- [15] TAN Y Z,LIAO Z J,QIAO Z Z,et al.Two Ih-symmetry-breaking C60 isomers stabilized by chlorination[J].Nat Mater,2008,7(10):790-794.
- [16] TAN Y Z,LI J,ZHU F,et al.Chlorofullerenes featuring triple sequentially fused pentagons[J].Nat Chem,2010,2(4):269-273.
- [17] TAN Y Z,ZHOU T,BAO J,et al.C72Cl4:a pristine fullerene with favorable pentagon-adjacent structure[J].J Am Chem Soc,2010,132(48):17102-17104.
- [18] TAN Y Z,CHEN R T,LIAO Z J,et al.Carbon arc production of heptagon-containing fullerene[68][J].Nat Commun,2011,2:420.
- [19] ZHOU T,TAN Y Z,SHAN G J,et al.Retrieving the most prevalent small fullerene C56[J].Chemistry,2011,17(31):8529-8532.
- [20] SHAN G J,TAN Y Z,ZHOU T,et al.C64Cl8:a strain-relief pattern to stabilize fullerenes containing triple directly fused pentagons[J].Chem Asian J,2012,7(9):2036-2039.
- [21] TAN Y Z,LI J,DU M Y,et al.Exohedrally stabilized C70 isomer with adjacent pentagons characterized by crystallography[J].Chem Sci,2013,4(7):2967-2970.
- [22] GAO C L,LI X,TAN Y Z,et al.Synthesis of long-sought C66 with exohedral stabilization[J].Angew Chem Int Ed,2014,53(30):7853-7855.
- [23] GAO C L,ABELLA L,TIAN H R,et al.Double functio-nalization of a fullerene in drastic arc-discharge conditions:synthesis and formation mechanism of C2v(2)-C78Cl6(C5Cl6)[J].Carbon,2018,129:286-292.
- [24] KROTO H W.The stability of the fullerenes Cn,with n=24,28,32,36,50,60 and 70[J].Nature,1987,329(6139):529-531.
- [25] FOWLER P W,MANOLOPOULOS D E.An atlas of fullerenes[J].Fullerene Science and Technology,1996,4(3):623-624.
- [26] TAMM N B,KOSAYA M P,FRITZ M A,et al.Synthesis,isolation,and X-ray structural characterization of trifluoromethylated C78 fullerenes:C78(2)(CF3)10/12 and C78(3)(CF3)12/14[J].Nanosystems:Physics,Chemistry,Mathematics,2016:111-117.doi:10.17586/2220-8054-2016-7-1-111-117.
- [27] KEMNITZ E,TROYANOV S I.Chlorides of isomeric C78 fullerenes:C78(1)Cl30,C78(2)Cl30,and C78(2)Cl18[J].Mendeleev Communications,2010,20(2):74-76.
- [28] SHUSTOVA N B,NEWELL B S,MILLER S M,et al.Discovering and verifying elusive fullerene cage isomers:structures of C2-p11-(C74-D3h)(CF3)12 and C2-p11-(C78-D3h(5))(CF3)12[J].Angew Chem Int Ed,2007,46(22):4111-4114.
- [29] SIMEONOV K S,AMSHAROV K Y,JANSEN M.Chlorinated derivatives of C78-fullerene isomers with unusually short intermolecular halogen-halogen contacts[J].Chemistry,2008,14(31):9585-9590.
- [30] HAN A H,WAKAHARA T,MAEDA Y,et al.A new method for separating the D3 and C2v isomers of C78[J].New J Chem,2009,33(3):497-500.
- [31] TROYANOV S I,KEMNITZ E.The first crystal structure of a halogenated higher fullerene,C78Br18,obtained by bromination of a fullerene mixture[J].Eur J Org Chem,2003,2003(20):3916-3919.
- [32] TROYANOV S I,TAMM N B,CHEN C,et al.Synthesis and structure of a highly chlorinated C78:C78(2)Cl30[J].Z Anorg Allg Chem,2009,635(12):1783-1786.
- [33] KOSAYA M P,FRITZ M A,BROTSMAN V A,et al.Synthesis,isolation and structure of trifluoromethylated fullerene D3-C78,C78(1)(CF3)10-18[J].Chem Asian J,2016,11(7):1000-1003.
- [34] TAMM N B,TROYANOV S I.Isomer C78(2)captured as the perfluoroethyl derivative C78(C2F5)10[J].Mendeleev Commun,2009,19(4):198-199.
- [35] OLMSTEAD M M,DE BETTENCOURT-DIAS A,DUCHAMP J C,et al.Isolation and structural chara-cterization of the endohedral fullerene Sc3N@C78[J].Angew Chem Int Ed,2001,40(7):1223-1225.
- [36] CAO B P,WAKAHARA T,TSUCHIYA T,et al.Isolation,characterization,and theoretical study of La2@C78[J].J Am Chem Soc,2004,126(30):9164-9165.
- [37] ZHAO P,LI M Y,GUO Y J,et al.Single step Stone-Wales transformation linking two thermodynamically stable Sc2O@C78 isomers[J].Inorg Chem,2016,55(5):2220-2226.