(厦门大学 生命科学学院,滨海湿地生态系统教育部重点实验室,福建 厦门 361102)
(Key Laboratory of the Coastal and Wetland Ecosystems,Ministry of Education,School of Life Sciences,Xiamen University,Xiamen 361102,China)
α-bromocinnamaldehyde; tyrosinase; Helicoverpa armigera
DOI: 10.6043/j.issn.0438-0479.201607025
备注
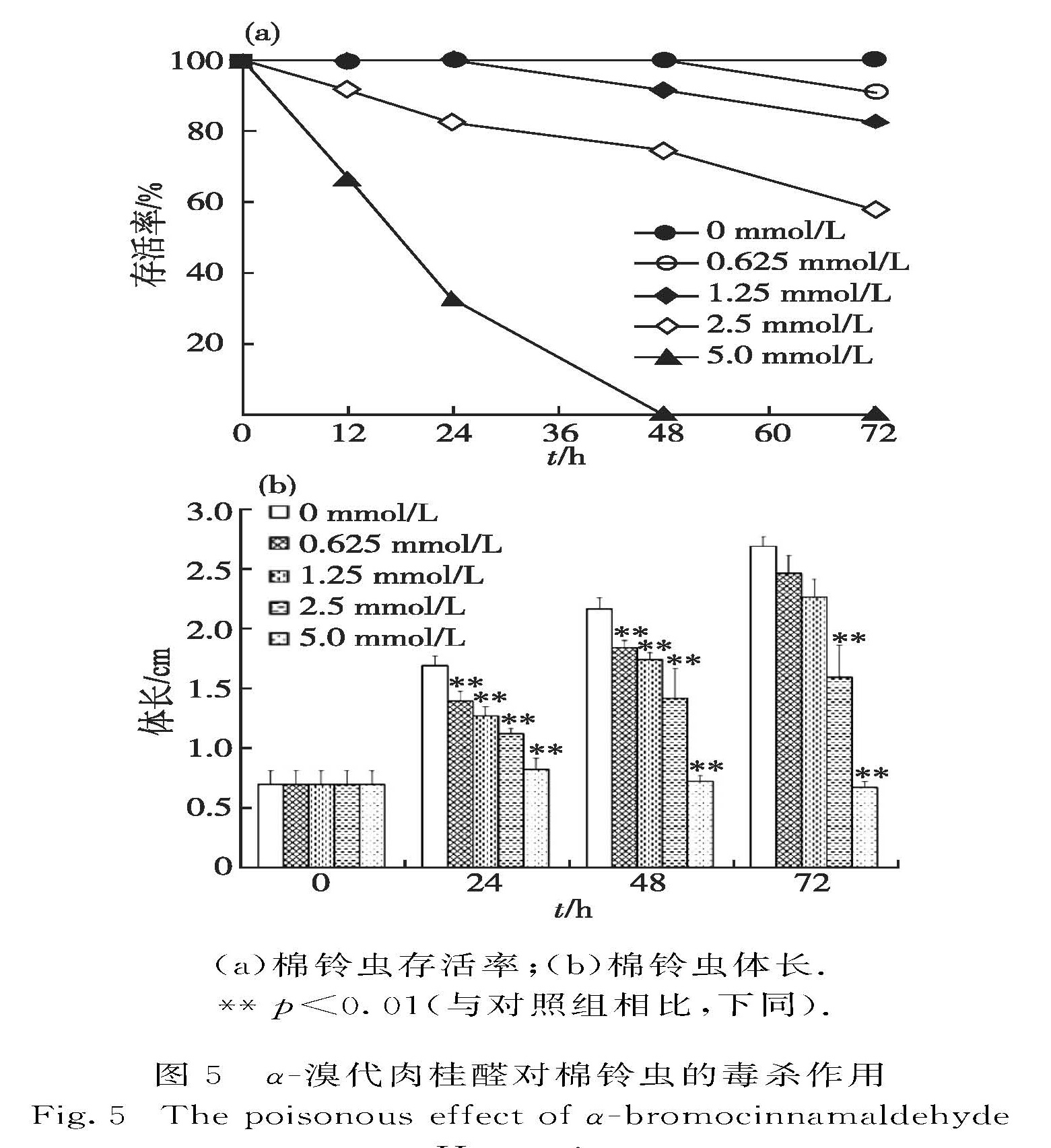
运用酶活性染色和酶抑制动力学方法分析了α-溴代肉桂醛对蘑菇酪氨酸酶的抑制作用,测得酶的正向和逆向速率常数分别为2.793 L/(mmol·min)和1.98×10-3 s-1.在此基础上探讨了α-溴代肉桂醛对棉铃虫(Helicoverpa armigera)的毒杀作用,发现经0.625 mmol/L α-溴代肉桂醛处理后,棉铃虫3龄幼虫的生长发育受到一定程度限制,当α-溴代肉桂醛浓度达5.0 mmol/L时,在作用48 h后致死.此外,经5.0 mmol/L α-溴代肉桂醛处理后,棉铃虫3龄幼虫的活体和离体多酚氧化酶(PPO)活力受到了显著抑制.上述结果为今后α-溴代肉桂醛在食品、农业、医药等方面的应用提供了理论和实践基础.
The inhibitory effect of α-bromocinnamaldehyde on mushroom tyrosinase was investigated in this study using enzyme activity staining and enzyme inhibitory kinetics.The rate constants of the forward(k+0)and reverse(k-0)reactions were determined to be 2.793 L/(mmol·min)and 1.98×10-3 s-1,respectively.Moreover,the insecticidal efficacy of α-bromocinnamaldehyde was determined.As expected,the larval growth and survival rate of Helicoverpa armigera were found to be reduced after supplemented with 0.625 mmol/L α-bromocinnamaldehyde as compared to the control larvae,and the larvae were totally dead after 48 h treatment with 5.0 mmol/L α-bromocinnamaldehyde.The polyphenol oxidase(PPO)activities were inhibited by 5.0 mmol/L α-bromocinnamaldehyde both in vivo and in vitro.These results may provide theoretical and practical basis in the application of α-bromocinnamaldehyde in food,agriculture and medicine.
引言
酪氨酸酶(EC 1.14.18.1)作为黑色素合成的限速酶,其活性与黑色素的合成量成正相关[1],当其在人体中异常表达时能引起雀斑和黑色素沉积等皮肤病.对昆虫而言,酪氨酸酶参与其表皮黑化、骨针形成、伤口愈合以及对外源病原体的包被吞噬等重要生命活动[2].对细菌而言,酪氨酸酶也具有举足轻重的作用,在其催化下形成的黑色素能保护细菌的孢子免受紫外线的伤害,同时还能螯合重金属离子以消除其对细菌细胞的伤害[3].酪氨酸酶众多的生理功能使得酪氨酸酶抑制剂成为国内外研究的热点.
肉桂醛已被广泛地应用于香精香料、化工生产、食品工程、粮食生产、果蔬保鲜、牲畜饲料等领域[4].近年来,其衍生物也不断被合成和开发.Andreeva等[5]报道了邻羟基肉桂醛的衍生物具有抗菌、抗炎、抑制癌细胞增殖等多种活性.张园园[6]发现α-溴代肉桂醛对淡紫拟青霉(Paecilomyces lilacinus)、黑曲霉(Aspergillus niger)和宛氏拟青霉(P. varioti)有抑制作用.
本课题组近期一项研究报道了α-溴代肉桂醛对蘑菇酪氨酸酶具有良好的抑制效应[7].在此基础上,本研究进一步分析了α-溴代肉桂醛对酪氨酸酶活力的抑制动力学,以阐明其相关酶学机制,同时还探究了其对棉铃虫(Helicoverpa armigera)的影响,以期为α-溴代肉桂醛在生物农药及果蔬保鲜剂等方面的开发利用奠定理论基础.
1 材料与方法
2 结果与分析
3 讨 论
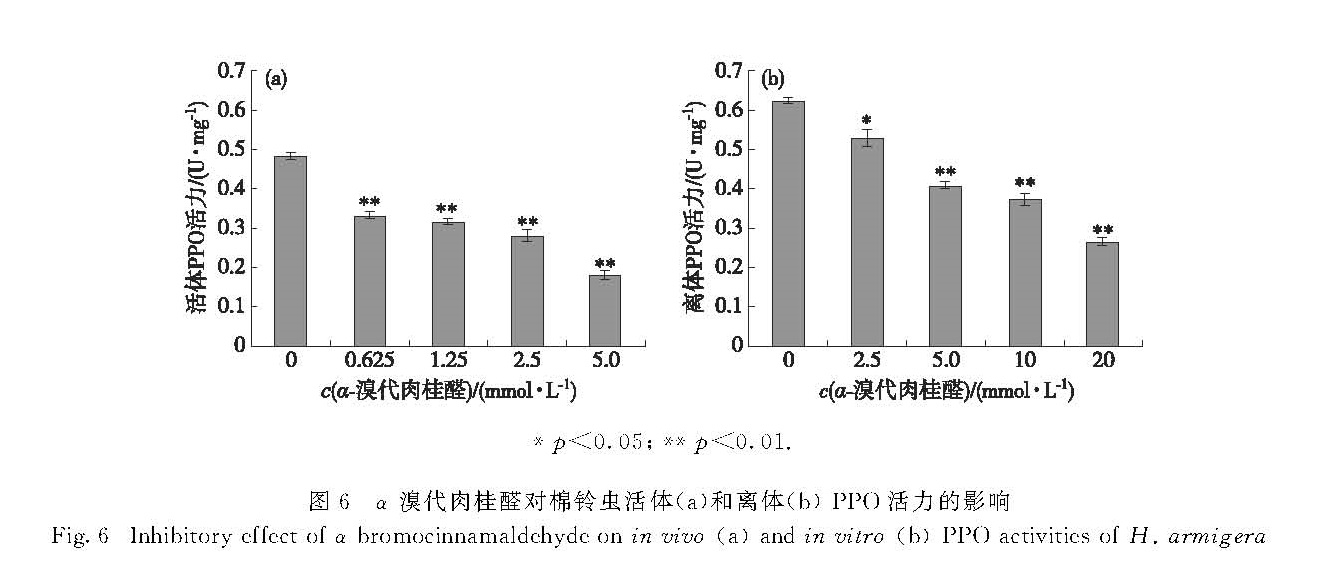
*p<0.05; **p<0.01.
图6 α-溴代肉桂醛对棉铃虫活体(a)和离体(b)PPO活力的影响
Fig.6 Inhibitory effect of α-bromocinnamaldehyde on in vivo(a)and in vitro(b)PPO activities of H. armigera本研究构建了混合竞争型动力学模型来探讨酶与底物以及酶与抑制剂的结合.结果显示,α-溴代肉桂醛对游离酶、酶-底物复合物的正向失活速率常数k+0和k'+0分别为2.793和1.441 L/(mmol·min),可以看出k+0>k'+0,这表明游离酶比酶-底物复合物更具有柔性,即α-溴代肉桂醛更易与游离酶相互作用,也说明了底物L-DOPA的存在能在一定程度上保护酶,阻止α-溴代肉桂醛的抑制作用.
α-溴代肉桂醛对棉铃虫的毒杀作用极有可能与PPO有关.酚氧化酶是昆虫体内黑色素合成的关键酶,通常以酶原的形式存在于昆虫血淋巴中,通过特异性丝氨酸蛋白酶级联反应被激活并水解生成有活性的PPO,在昆虫免疫反应中起关键性的作用,该酶系已逐渐成为探索新杀虫药剂的关键靶标之一[18].谢桂英等[19]研究发现天然源化合物曲酸对小菜蛾(Plutella xylostella)的毒杀作用也与酚氧化酶抑制有关.马志卿等[20]报道了松油烯-4-醇对粘虫(Mythimna separata)的PPO活力有明显的抑制作用.本研究中α-溴代肉桂醛处理棉铃虫后,对虫体的生长发育有显著的抑制效果,同时虫体PPO活力也受到显著的抑制,推测α-溴代肉桂醛可能是通过抑制黑色素的形成而破坏棉铃虫的免疫系统,导致其死亡.
综上,α-溴代肉桂醛能有效地抑制酪氨酸酶活力的同时,又能对棉铃虫产生抑制效应,该研究结果将为α-溴代肉桂醛在食品、农业、医药等方面的应用提供理论和实践基础.
2.1 Native-PAGE法分析α-溴代肉桂醛对酪氨酸酶的抑制作用
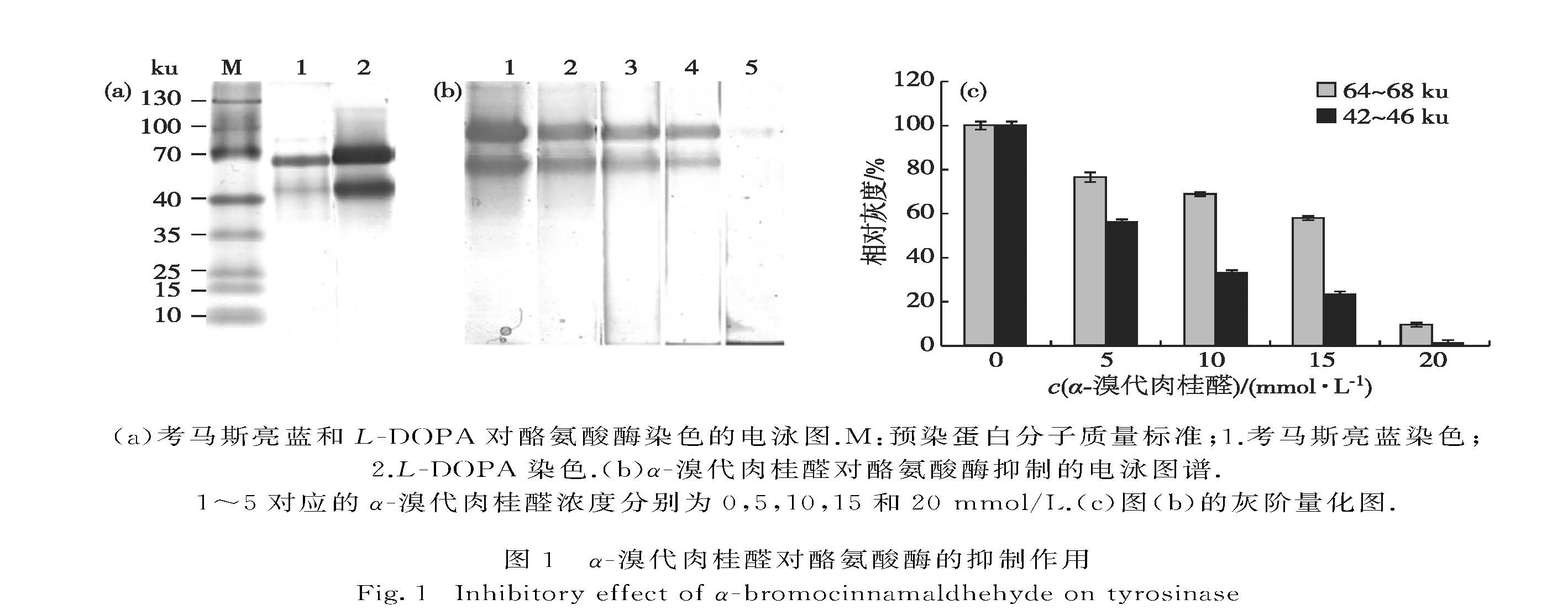
蘑菇酪氨酸酶由多家族基因编码,分子质量范围为42~46 ku和64~68 ku[14-16].由图1(a)可知,样品中存在2种分子质量的酪氨酸酶且均具活性.由图1(b)可见,随着α-溴代肉桂醛浓度增加,酪氨酸酶的活性条带颜色深度递减.当α-溴代肉桂醛浓度为20 mmol/L时,42~46 ku的酪氨酸酶条带完全消失,用ImageJ 1.48软件量化处理后的灰度值为对照组的0.9%; 64~68 ku的酪氨酸酶条带也几乎完全消失,灰度值为对照组的8.96%(图1(b)和(c)).上述结果说明α-溴代肉桂醛对酪氨酸酶有明显的抑制作用且呈现出浓度效应.
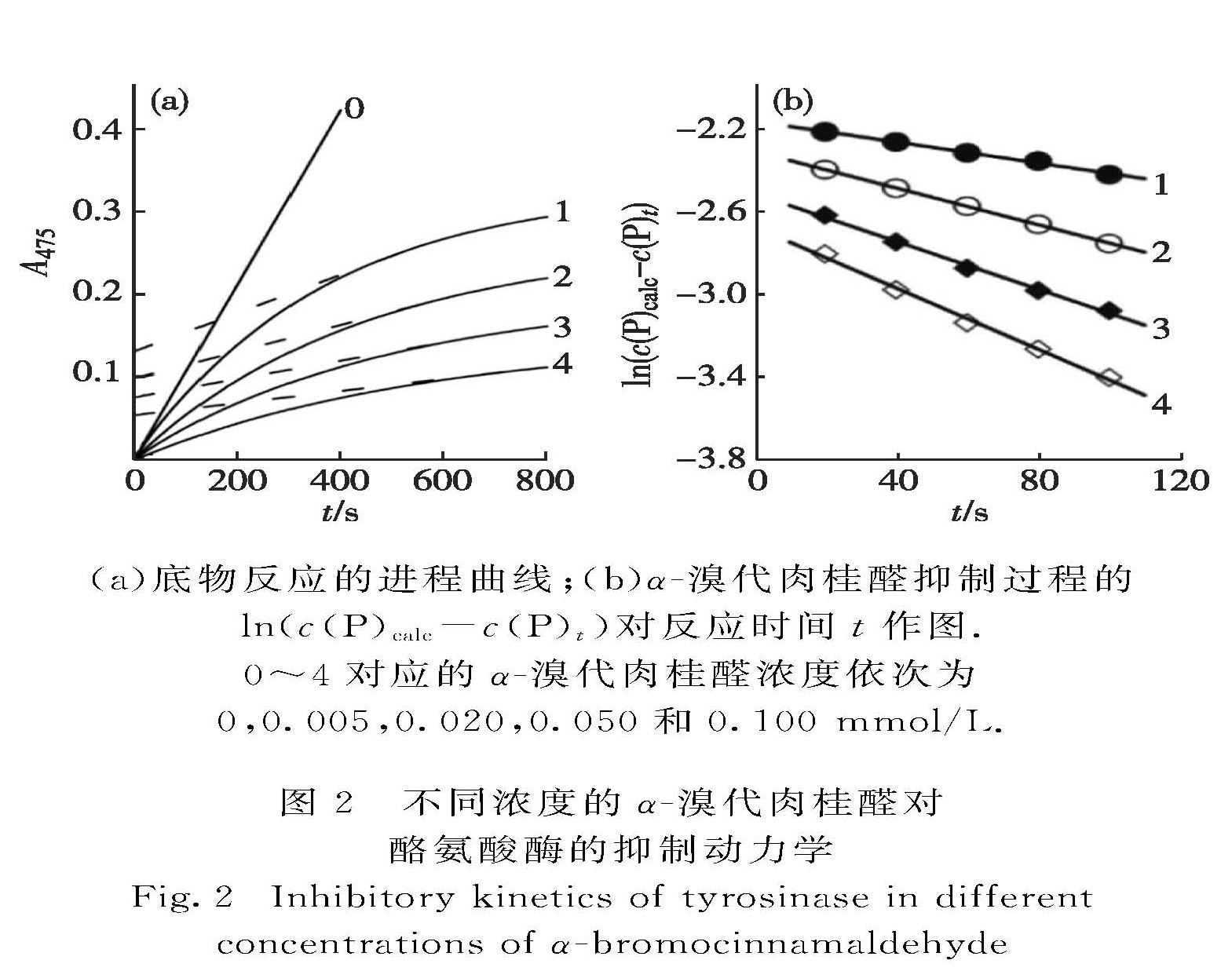
2.2 α-溴代肉桂醛对酪氨酸酶的抑制动力学2.2.1 抑制动力学模型在30 ℃下监测不同浓度的α-溴代肉桂醛存在时产物形成量随反应时间的进行过程,结果如图2(a)所示:在考察的浓度范围内,α-溴代肉桂醛对酶表现为慢可逆抑制作用.虽然酶和抑制剂结合后成为无活性的络合物,但是由于抑制过程达到终态时仍有部分未与抑制剂结合的天然酶存在,因而表现出有部分剩余活力.以ln(c(P)calc-c(P)t)(c(P)calc表示理论计算得出的产物浓度,c(P)t表示反应时间为t时的产物浓度)对反应时间t作图(图2(b)),得到一组直线,其负斜率(-slope)为Ac(I)+B.
图2 不同浓度的α-溴代肉桂醛对酪氨酸酶的抑制动力学
Fig.2 Inhibitory kinetics of tyrosinase in different concentrations of α-bromocinnamaldehyde在本课题组前期的研究中发现α-溴代肉桂醛对酶是混合型抑制[7],因此酶在α-溴代肉桂醛的慢可逆抑制作用过程中催化底物反应的动力学模型可以表示如下[17]:
式中:S、P、I和E分别表示底物(L-DOPA)、产物、效应物(α-溴代肉桂醛)和天然酶; ES、EI和EIS为相应的复合物; k+1、k'+1、k+2为正向反应速率常数; k-1、k'-1为逆向反应速率常数.在底物和效应物浓度远大于酶的初始浓度时,根据Cabanes等[18]提出的效应物存在下的酶催化底物反应的动力学方程,可计算出游离酶的正向速率常数(k+0)、酶-底物复合物的正向速率常数(k'+0)、游离酶的逆向速率常数(k-0)和酶-底物复合物的逆向速率常数(k'-0).
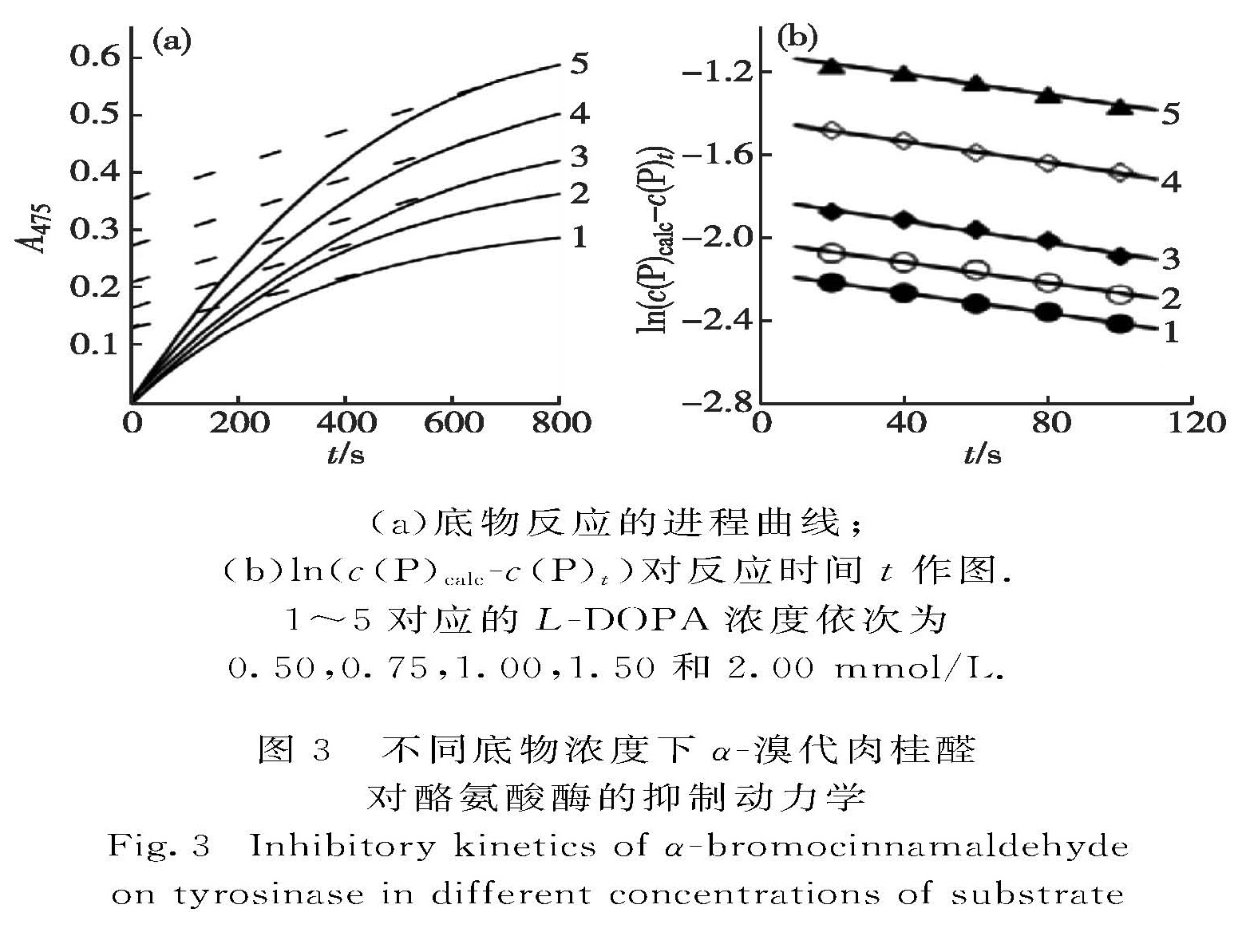
2.2.2 微观速率常数测定固定α-溴代肉桂醛浓度,改变底物浓度,监测酶催化底物反应的动力学过程.图3(a)为在含0.005 mmol/L α-溴代肉桂醛及不同浓度L-DOPA的测活体系中酶促反应的进程曲线.以ln(c(P)calc-c(P)t)对反应时间t作图(图3(b)),得到一组直线,其负斜率为Ac(I)+B.
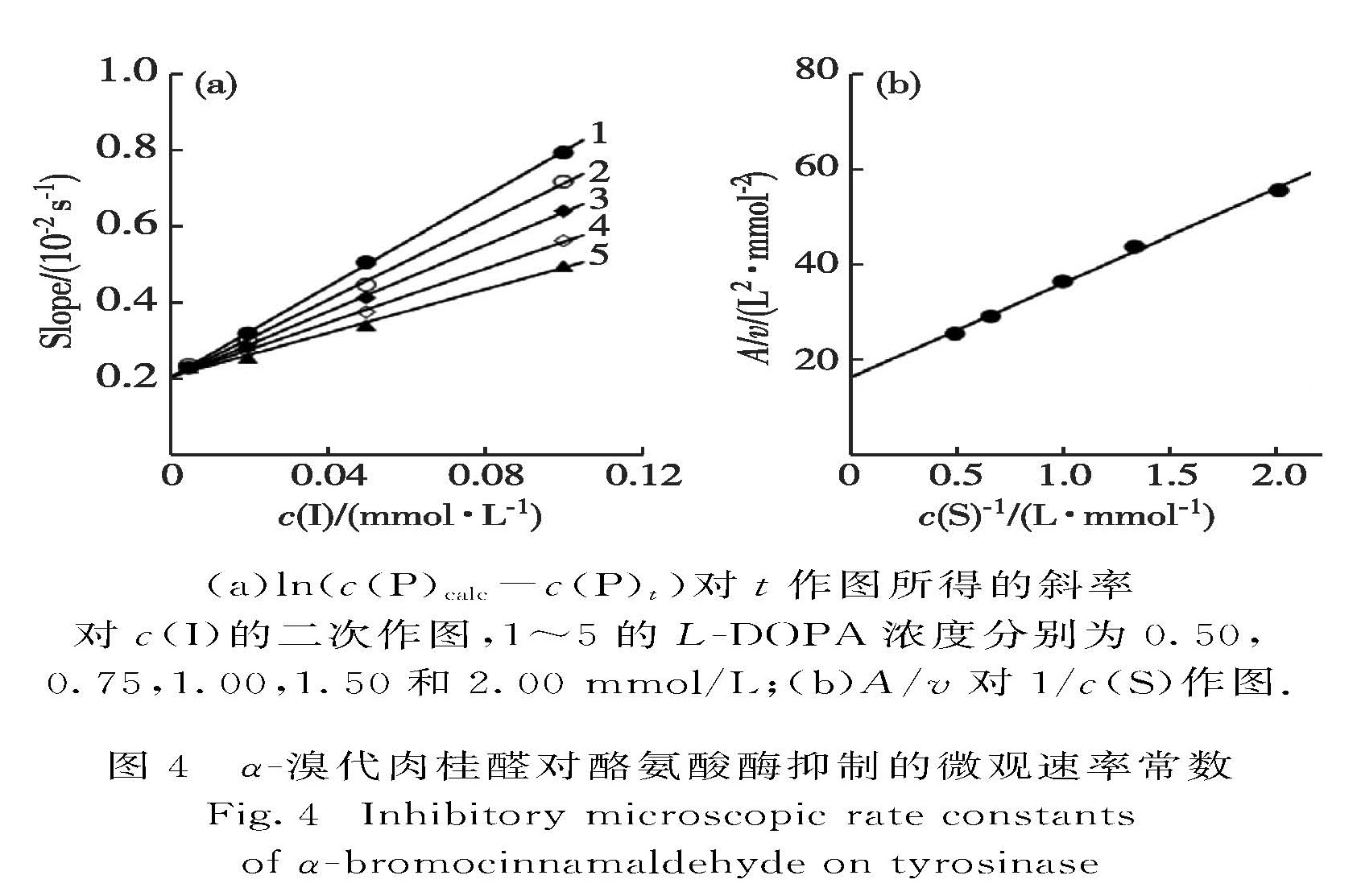
再以斜率对c(I)作图,得到一组直线,从直线的斜率和截距分别可求得A和B的值.由图4(a)可见:不同底物浓度下,ln(c(P)calc-c(P)t)对反应时间t作图所得的斜率再对c(I)二次作图的一组直线的截距不变,即在不同的底物浓度下,逆向反应的表观速率常数B的值不变,说明逆向反应的速率常数k-0和k'-0相等,且等于B的值.由此求得逆向反应的微观速率常数k-0和k'-0均为1.98×10-3 s-1.
以A/v对1/c(S)作图,得到一条直线(图4(b)),该直线的斜率为Km·k+0/Vm,截距为k'+0/Vm.其中Km和Vm可从无抑制剂存在下的酶促反应动力学求得,在该条件下测得酶促反应的Km值为0.62 mmol/L,Vm值为89.4 μmol/(L·min).因此,从直线的斜率和截距可求得酶被α-溴代肉桂醛抑制的失活反应的微观速率常数k+0和k'+0分别为2.793和1.441 L/(mmol·min).
- [1] CHAKRABORTY A K,FUNASAKA Y,KOMOTO M,et al.Effect of arbutin on melanogenic proteins in human melanocytes [J].Pigment Cell Research,1998,11(4):206-212.
- [2] SUGUMARAN M.Molecular mechanisms for cuticular sclerotization in Drosophila melanogaster[J].Journal of Cellular Biochemistry,1987,S(11 part C):27.
- [3] FACCIO G,KRUUS K,SALOHEIMO M,et al.Bacterial tyrosinases and their applications [J].Process Biochemistry,2012,47(12):1749-1760.
- [4] 阮海燕.肉桂醛在香料工业及日用化工行业中的应用 [J].香料香精化妆品,2005,2(1):37-38.
- [5] ANDREEVA I M,BABESHKO O M,BONDARENKO E M,et al.Structure and antimicrobial activity of 2-hydroxy-cinnamaldehyde derivatives [J].Pharmaceutical Chemistry Journal,1985,19(3):191-193.
- [6] 张园园.肉桂醛抑菌衍生物的合成及其定量构效关系 [D].哈尔滨:东北林业大学,2013:11.
- [7] CUI Y,LIANG G,HU Y H,et al.α-substituted derivatives of cinnamaldehyde as tyrosinase inhibitors:inhibitory mechanism and molecular analysis [J].Journal of Agricultural and Food Chemistry,2015,63(2):716-722.
- [8] XING R,ZHENG A P,WANG F,et al.Functionality study of Na6PMo11FeO40 as a mushroom tyrosinase inhibitor [J].Food Chemistry,2015,175:292-299.
- [9] TSOU C L.Kinetics of substrate reaction during irreversible modification of enzyme activity [J].Advances in Enzymology and Related Areas of Molecular Biology,1988,61:381-436.
- [10] 刘轩.芳香族香料化合物及其衍生物的生物学效应研究 [D].厦门:厦门大学,2013:22.
- [11] 李凤舞,叶炳辉,钟维列.顺式氯氰菊酯对蚊幼虫脱氧核糖核酸酶、核糖核酸酶和多酚氧化酶的影响 [J].寄生虫与医学昆虫学报,1998,5(1):37-42.
- [12] BRADFORD M M.A rapid and sensitive method for the quantitation of microgram quantities of protein utilizing the principle of protein-dye binding [J].Anal Biochem,1976,72(1):248-254.
- [13] 马燕,刘瑞瑞,马志卿,等.斑蝥素对粘虫几种代谢酶及多酚氧化酶的影响 [J].昆虫学报,2010,53(8):870-875.
- [14] GERDEMANN C,EICKEN C,KREBS B.The crystal structure of catechol oxidase:new insight into the function of type-3 copper proteins [J].Accounts of Chemical Research,2002,35(3):183-191.
- [15] WICHERS H J,RECOURT K,HENDRIKS M,et al.Cloning,expression and characterisation of two tyrosinase cDNAs from Agaricus bisporus[J].Applied Microbiology and Biotechnology,2003,61(4):336-341.
- [16] WU J J,CHEN H B,GAO J Y,et al.Cloning,characterization and expression of two new polyphenol oxidase cDNAs from Agaricus bisporus[J].Biotechnology Letters,2010,32(10):1439-1447.
- [17] JIANG H B,WANG Y,KANOST M R.Pro-phenol oxidase activating proteinase from an insect,Manduca sexta:a bacteria-inducible protein similar to Drosophila easter [J].Proceedings of the National Academy of Sciences of the United States of America,1998,95(21):12220-12225.
- [18] CABANES J,GARCIA-CANOVAS F,TUDELA J,et al.L-mimosine,a slow-binding inhibitor of mushroom tyrosinase [J].Phytochemistry,1987,26(4):917-919.
- [19] 谢桂英,罗万春,马琛.天然源化合物曲酸对小菜蛾酚氧化酶抑制作用研究初报 [J].农药学学报,2003,5(1):68-72.
- [20] 马志卿,韩秀玲,冯俊涛.松油烯-4-醇对粘虫几种代谢酶及酚氧化酶的影响 [J].中国农业科学,2008,41(2):437-442.
1.1 材 料供试的棉铃虫及其无菌饲料均来自湖北省生物农药工程研究中心,培养温度控制在(30±2)℃,相对湿度为70%,光周期与自然光周期同步.
α-溴代肉桂醛为Aladdin公司产品; 蘑菇酪氨酸酶(酶活力为1 000 U/mg)和L-3,4-二羟基苯丙氨酸(L-DOPA)为Sigma-Aldrich公司产品; 其他试剂均为国产分析纯; 使用的水为去离子重蒸水(ddH2O).
1.2 方 法1.2.1 非变性聚丙烯酰胺凝胶电泳(native-PAGE)检测参照Xing等[8]的方法操作.除了考马斯亮蓝染色的蘑菇酪氨酸酶样品外,其他样品均不加热.上样酶液中蘑菇酪氨酸酶活力为1 000 U/mL(用50 mmol/L,pH 6.8的磷酸盐缓冲液(PBS)配制),每孔上样量为20 μL.电泳结束后,每一泳道切割为一片胶片,并将胶片按原泳道顺序依次浸泡在浓度为0,5,10,15,20 mmol/L的α-溴代肉桂醛溶液中,在摇床上旋转振摇45 min后取出,用10 mg/mL L-DOPA在37 ℃下孵育1 min,进行活性染色.除活性染色操作外,上述过程均在4 ℃下进行.
1.2.2 α-溴代肉桂醛对酪氨酸酶抑制动力学常数的测定根据Tsou[9]的方法测定.以0.50 mmol/L L-DOPA为底物,用不同浓度的α-溴代肉桂醛与终质量浓度为3.33 μg/mL的蘑菇酪氨酸酶反应,监测反应进程曲线.L-DOPA经酶催化形成的产物在475 nm处的吸光度(A475)最强,在Beckman DU800型分光光度计下测定A475以反映产物形成量,产物在475 nm处的克分子消光系数ε按3 700(L·cm)/mol计算.研究不同底物浓度下的酶失活动力学,根据合适的作图方法测定酶的失活微观速率常数.固定底物L-DOPA浓度为0.5 mmol/L,改变抑制剂α-溴代肉桂醛浓度(0,0.005,0.020,0.050,0.100 mmol/L); 固定α-溴代肉桂醛浓度为0.005 mmol/L,改变底物浓度(0.50,0.75,1.00,1.50和2.00 mmol/L); 实时跟踪测定800 s,以产物形成量对时间作图.
1.2.3 α-溴代肉桂醛对棉铃虫毒力的测定采用平板喂食法[10]进行测定.以乙酸乙酯为溶剂,采用倍比稀释法配制浓度分别为0,12.5,25,50和100 mmol/L的α-溴代肉桂醛母液.吸取3 mL饲料分装于24孔板,每孔中再加入150 μL不同浓度的α-溴代肉桂醛母液混于饲料中,使其均匀分布,每孔中α-溴代肉桂醛的终浓度分别为0,0.625,1.25,2.5和5.0 mmol/L,每个浓度4个孔,平行重复3块板.待乙酸乙酯挥发完全后,用毛笔转移棉铃虫3龄幼虫,每孔1只,每个浓度共计12只.每隔24 h拍照观察并测量棉铃虫体长,调查死亡虫数(虫的死亡以毛笔轻触不动为准),计算死亡率.
1.2.4 棉铃虫多酚氧化酶(PPO)活力的测定取经α-溴代肉桂醛处理后的供试棉铃虫,称量后按1 g:10 mL加入预冷的0.1 mol/L PBS(pH 7.0),冰浴匀浆后置于冷冻离心机4 000 r/min离心20 min,上清液即为待测酶液.酶活力测定参考李凤舞等[11]的方法,略有改动.以150 μL 0.5 mmol/L的L-DOPA作底物,取50 μL酶液加入反应体系,在30 ℃下反应30 min,在96孔板中测定A475.蛋白浓度采用考马斯亮蓝G-250法[12]测定.以每毫克蛋白每30 min的A475变化量来表示酶活力.每组处理重复3次.
离体酶活力测定参照马燕等[13]的方法.选择未经处理的适龄棉铃虫,以1 g:10 mL加入预冷的0.1 mol/L PBS(pH 7.0),冰浴下高速匀浆后于4 ℃静置1 h,12 000 r/min冷冻离心30 min,上清液即为棉铃虫PPO粗提液.用二甲基亚砜(DMSO)配制不同浓度的α-溴代肉桂醛溶液.在含50 μL 0.05 mol/L PBS(pH 6.8)的300 μL反应体系中,先加入50 μL不同浓度的α-溴代肉桂醛,再加入50 μL 0.5 mmol/L L-DOPA和ddH2O,最后加入100 μL棉铃虫PPO粗提液,立刻混匀,30 ℃恒温水浴30 min后,吸取200 μL反应液于酶标板,用多功能酶标仪测定A475.各浓度3个重复孔,取平均值.