(厦门大学附属第一医院神经外科,福建 厦门 361003)
(Department of Neurosurgery,The First Affiliated Hospital of Xiamen University,Xiamen 361003,China)
DOI: 10.6043/j.issn.0438-0479.201608009
备注
为探讨miR-193b对人胶质瘤U251细胞的迁移和侵袭能力的影响,利用HiPerFect转染试剂瞬时转染miR-193b模拟物(mimics)上调U251细胞中miR-193b的表达,通过实时荧光定量PCR(qRT-PCR)检测其转染效率,然后进行细胞划痕实验及侵袭实验,分别检测miR-193b对U251细胞迁移及侵袭能力的影响.结果显示过表达miR-193b可抑制U251细胞迁移和侵袭的能力.应用生物信息学软件预测,提示单羧酸转运蛋白7(MCT7)基因可能是miR-193b的潜在靶基因.进而构建双荧光素酶报告基因系统从转录水平上证明MCT7为miR-193b调控的靶基因; qRT-PCR及蛋白质免疫印记(Western blot)分别在mRNA和蛋白水平上进一步证明MCT7基因的表达受miR-193b的负调控.由此可见,miR-193b很可能通过负向调控MCT7基因的表达来抑制U251细胞的迁移与侵袭.
To investigate the effect of miR-193b on the migration and invasion of human glioma cell line U251,upregulated expression level of miR-193b in glioma U251 cells was achieved through transfecting with miR-193b mimics using HiPerFect transfection reagent.The transfection efficiency of miR-193b was detected using qRT-PCR,and cell scratch assay and invasive experiments were used to detect the abilities of miR-193b on migration and invasion of glioma cells.Results showed that the over-expression of miR-193b can inhibit the ability of U251 cells in migration and invasion.Meanwhile,bioinformatic software was used to predict the potential miR-193b target genes,and we found that MCT7 was the potential target gene of miR-193b.Subsequently,the dual luciferase report gene system,qRT-PCR and Western blot all revealed that miR-193b negatively regulated the expression of MCT7 gene.It is suggested that miR-193b propably inhibits the migration and invasion of U251 glioma cells by negatively regulating the expression of MCT7 gene.
引言
胶质瘤发生于神经上皮,是发病率、致残率、术后复发率和死亡率最高的颅内肿瘤,成人发病率可达0.006%,5年存活率仅20%~30%[1-2].手术治疗是胶质瘤最直接、最基本的首选治疗方法,但由于胶质瘤呈浸润性生长且和周围正常脑组织没有明显界限,故通过手术难以完全切除且容易复发,其中患有高度恶性的多形性胶质母细胞瘤患者的中位生存期仍然少于15个月[3].为了攻克胶质瘤治疗这一世界性难题,延长胶质瘤病人的生存期,一些创新的治疗技术如光动力学治疗、免疫治疗、基因治疗等不断应用于胶质瘤的治疗中,并取得了一定的疗效.
随着对胶质瘤发病机制的不断深入探索,大量研究证实miRNA与胶质瘤的发展有紧密联系,扮演着原癌基因或抑癌基因的功能.miR-21是胶质瘤中最常见的具有原癌基因活性的高表达miRNA,已有研究[4]表明miR-21的表达异常可通过调控Spry2蛋白表达来阻断Ras/MAPK信号通路的负反馈调节,并以此影响胶质瘤的侵袭.Laura等[5]研究发现联合阿霉素和miR-21抑制剂治疗可使得胶质瘤耐药细胞(T98G)对蒽环类药物敏感,从而促进细胞凋亡.miR-23a[6]、miR-10b[7]、miR-372[8]、miR-381[9]等也能促进胶质瘤的发生与发展,而miR-34a具有抑癌基因的作用.Rathod等[10]研究发现miR-34a在高级别胶质瘤和胶质瘤干细胞系HNGC-2和NSG-K16中的表达明显下调,上调miR-34a后可明显抑制Rictor的表达从而抑制细胞的生长、增殖及侵袭能力,进一步证实上调Rictor可激活AKT和Wnt信号通路而加剧肿瘤的发展.此外,miR-106a[11]、miR-146a[12]、miR-137[13]等也能抑制胶质瘤的发生与发展,但关于miR-193b在胶质瘤上的研究相对较少.本研究通过分析miR-193b在人胶质瘤U251细胞迁移、侵袭中的作用机制,以期为临床提供新的胶质瘤诊断标志物和特异性治疗靶点.
1 材料和方法
2 结果与分析
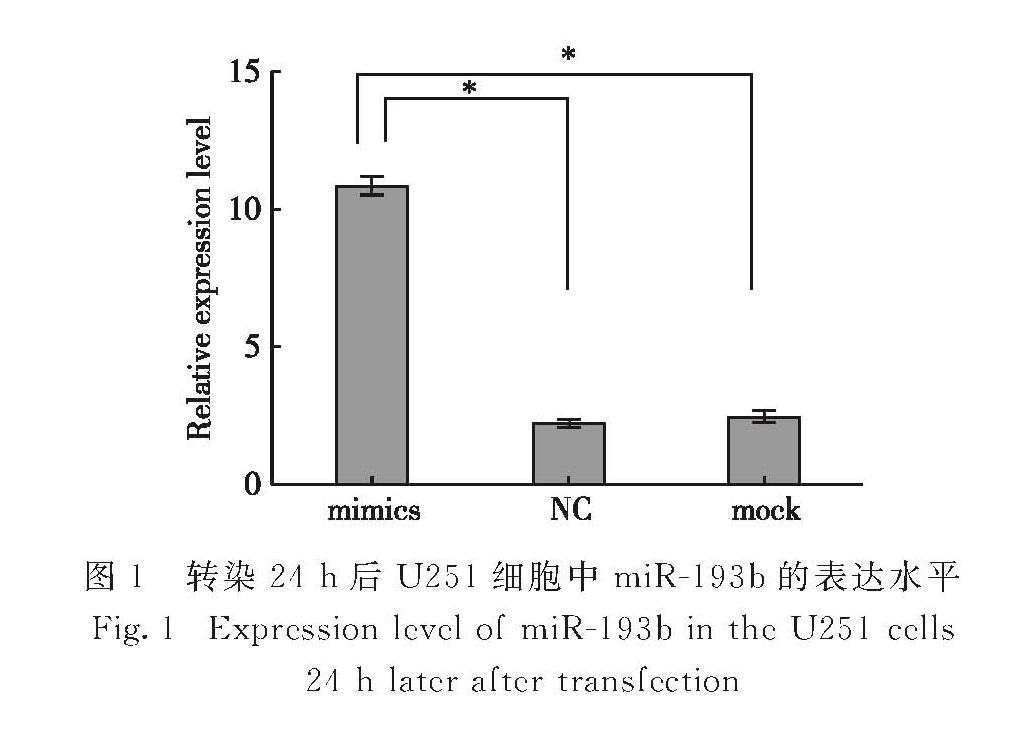
2.1 转染后miR-193b的表达qRT-PCR检测结果(图1)显示:mimics组中的miR-193b表达水平明显升高,与NC组和mock组相比差异显著(p<0.05); 而NC组与mock组之间无显著差异(p>0.05).这表明成功转染miR-193b mimics后可显著上调miR-193b的表达水平,由此计算得该浓度下的转染效率为77%.
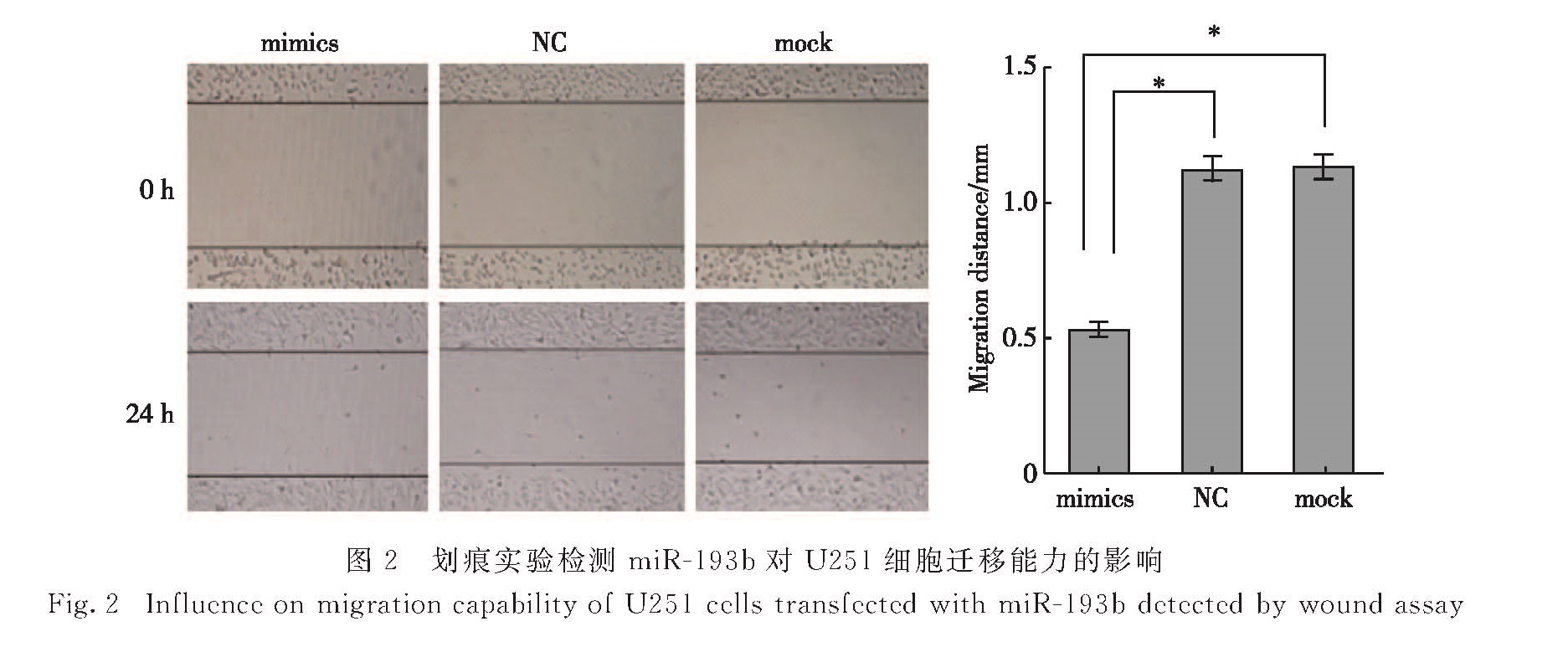
2.2 miR-193b对细胞迁移能力的影响划痕实验结果如图2所示,mimics组、NC组和mock组细胞的相对迁移距离分别为(0.55±0.05)mm,(1.13±0.07)mm,(1.14±0.06)mm.其中:mimics组细胞的相对迁移距离显著小于NC组及mock组(p<0.05); 而NC组与mock组之间无显著差异(p>0.05).这说明上调miR-193b的表达水平可以显著抑制U251细胞的迁移能力.
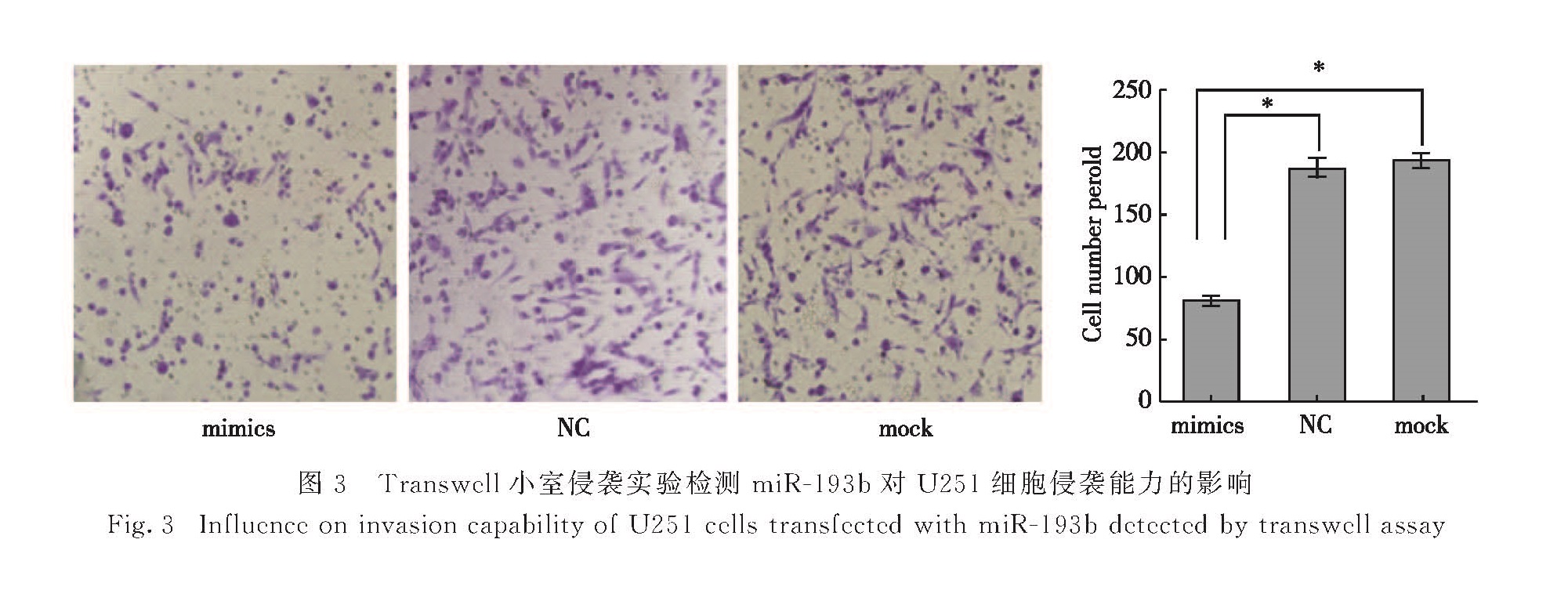
2.3 miR-193b对细胞侵袭能力的影响Transwell小室侵袭实验结果如图3所示,mimics组、NC组及mock组中穿过基底膜的细胞数分别为80±6,188±7,196±5.其中:mimics组与NC组及mock组相比,细胞侵袭能力显著下降(p<0.05); 而NC组与mock组之间无显著差异(p>0.05).这说明上调miR-193b的表达水平可以显著抑制U251细胞的侵袭能力.
2.4 miR-193b对靶基因MCT7表达的调控通过生物信息学软件分析检索,发现MCT7基因的3'非编码区域(3'-UTR)存在miR-193b的结合位点(图4),暗示MCT7可能是miR-193b的下游潜在靶基因.
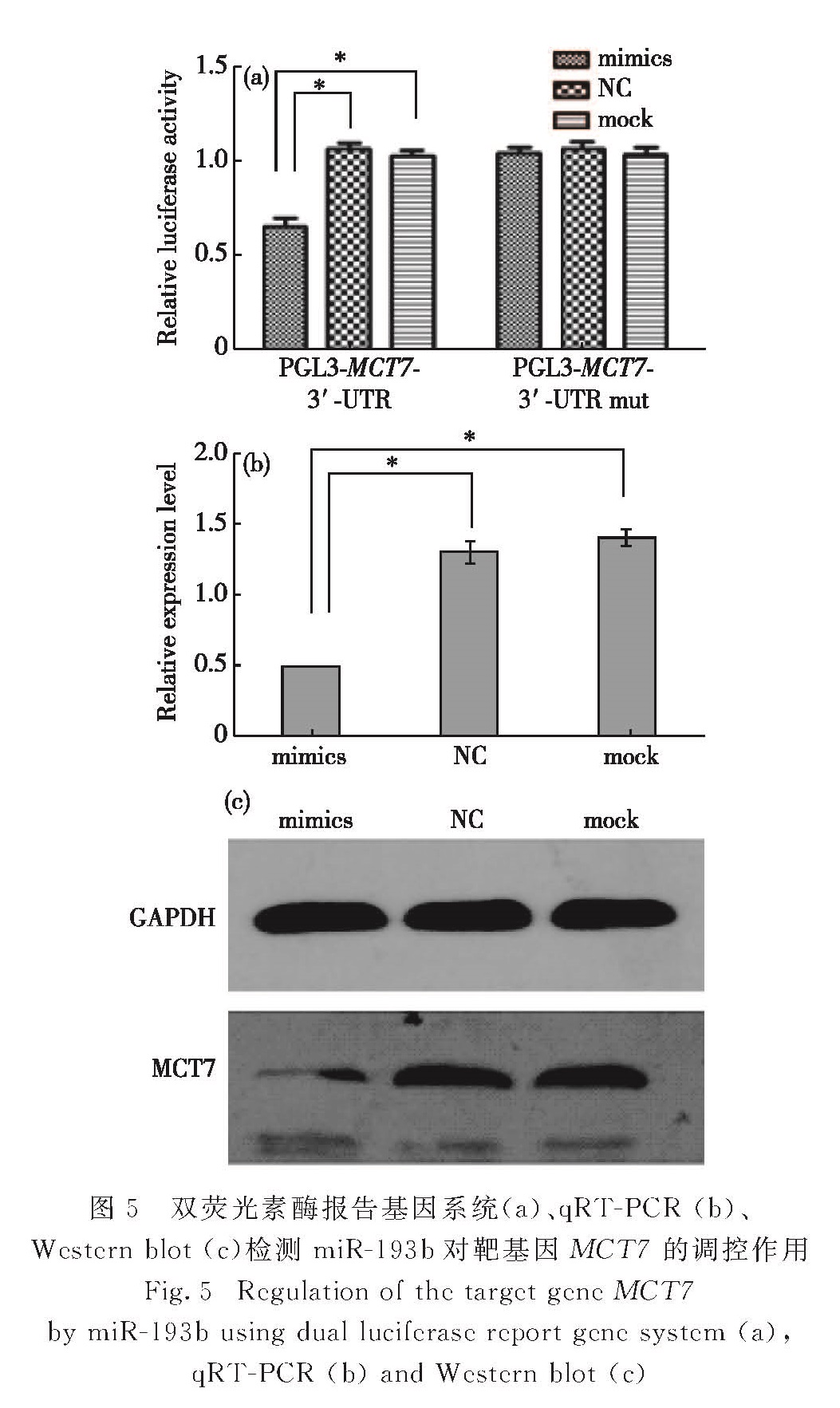
双荧光素酶报告基因系统检测结果如图5(a)所示:共转染PGL3-MCT7-3'-UTR时,mimics组可明显降低U251细胞中荧光素酶活性,与NC组和mock组相比差异显著(p<0.05); 而共转染PGL3-MCT7-3'-UTR mut时,荧光素酶活性与NC组及mock组相比无显著差异(p>0.05).由此证明MCT7是miR-193b调控的靶基因.qRT-PCR结果(图5(b))显示:mimics组的MCT7基因表达水平与NC组和mock组相比显著下降(p<0.05); 而NC组与mock组之间无显著差异(p>0.05).由此可知,上调miR-193b表达水平可显著抑制U251细胞中MCT7基因的表达.Western blot检测结果(图5(c))显示:转染后mimics组的MCT7蛋白表达水平明显下降,与NC组和mock组相比差异显著(p<0.05); NC组与mock组之间无显著差异(p>0.05).由此可知,上调miR-193b表达水平可显著抑制U251细胞中MCT7蛋白的表达.
3 讨 论
miR-193b异常表达与人类恶性肿瘤的进展息息相关,在不同肿瘤中发挥的功能有所不同,可起致癌基因的作用,也可发挥抑癌基因的作用.Wang等[14]通过qRT-PCR检测经低幅度激光照射处理后的骨间质干细胞,发现miR-193b表达异常升高,上调miR-193b可以抑制生长抑制剂家族成员5(ING5)的表达,从而激活细胞周期蛋白依赖性激酶2(CDK2)信号通路来促进细胞增殖.Li等[15]发现miR-193b可以靶向负调控尿激酶类血浆酶原激活子(uPA)的表达从而加剧乳腺癌的进展和侵袭.Xu等[16]发现与非肿瘤肝组织相比,miR-193b在肝癌组织中表达明显下调,miR-193b的异常表达可以显著抑制肝癌细胞的体外克隆能力以及肿瘤在裸鼠模型中的进展; 上调miR-193b可以通过靶向调节CCND1和ETS1基因的表达来阻滞细胞周期发展,抑制肝癌细胞的迁移和侵袭.Nyhan等[17]发现miR-193b可以通过负向调控Stathmin 1(STMN1)来影响食管癌细胞处理5-氟尿嘧啶的能力,诱导细胞自噬,并促进非凋亡性细胞死亡.本研究证实miR-193b可以抑制人胶质瘤U251细胞的迁移和侵袭能力.
MCT7是MCT家族成员之一,MCT又属于溶质运载蛋白家族(solute carrier family,SLC)的SLC16A 亚家族,是哺乳动物细胞膜上广泛分布的一类跨膜转运蛋白.目前,MCT家族已发现有14个成员,均由SLC16A基因家族编码,在种属间高度保守,其主要参与调控乳酸、短链脂肪酸、丙酮酸、丁酸等单羧酸类化合物的跨膜转运.Froberg等[18]研究了83例原发性中枢神经系统肿瘤和8例非中枢神经系统肿瘤,发现MCT1在室管膜瘤、血管母细胞瘤和多形性胶质母细胞瘤中均呈高表达,而在星形细胞瘤和少突胶质细胞瘤中呈阴性或低表达.Li等[19]发现在29例髓母细胞瘤样本中,90%都呈现编码MCT1的SLC16A1基因表达升高,进一步研究发现SLC16A1受到miR-124的负向调控,敲除SLC16A1基因后可以诱导髓母细胞瘤细胞死亡.Mathupala等[20]发现MCT1和MCT2主要表达于多形性胶质母细胞瘤组织中,MCT3主要表达于正常脑组织中,而在所有脑肿瘤组织中均未检测到MCT4的表达; 沉默MCT1和MCT2基因的表达可以诱导U87细胞的坏死和凋亡.Miranda-Goncalves等[21]发现与弥漫性星形细胞瘤和非肿瘤脑组织相比,胶质母细胞瘤组织的细胞膜上MCT1和MCT4均呈过量表达.此外,MCT7[22]和MCT14[23]的表达也主要存在于脑组织中,而MCT7在胶质瘤中的作用机制目前尚不明确.
本研究发现miR-193b存在与MCT7基因的3'-UTR特异性结合的位点,并对其表达进行负向调控,说明MCT7是miR-193b调控的靶基因.进一步研究发现miR-193b可以抑制人胶质瘤U251细胞的迁移和侵袭能力,这一作用机制很可能是通过负向调控MCT7基因的表达来实现的.因此,miR-193b有望为临床提供新的胶质瘤诊断标志物和特异性治疗靶点.
1.1 主要材料人胶质瘤U251细胞(世界卫生组织分级为Ⅳ级)为厦门大学附属第一医院中心实验室冻存.DMEM(Dulbecco's modified eagle medium)培养液和胎牛血清均购自美国Hyclone公司; miR-193b模拟物(mimics)和阴性对照(miR-negative control)由上海吉玛制药技术有限公司合成; miR-193b特异性引物购自北京天根生化科技有限公司(引物序列为5'-AACUGGCCCUCAAAGUCCCGCU-3'),靶基因单羧酸转运蛋白7(MCT7)基因的特异性引物(正向引物序列为5'-CCACAGTCCTGAGCAATCGT-3',反向引物序列为5'-CCCAGACCAGAGATGATGCC-3')以及内参基因U6的特异性扩增引物(正向引物序列为5'-CTCGCTTCGGCAGCACATA-3',反向引物序列为5'-CGAATTTGCGTGTCATCCT-3')和甘油醛-3-磷酸脱氢酶(GAPDH)基因的特异性扩增引物(正向引物序列为5'-GGAGCGAGATCCCTCCAAAAT-3',反向引物序列为5'-GGCTGTTGTCATACTTCTCATGG-3')均购自上海生工生物工程股份有限公司; HiPerFect 转染试剂、miRNeasy小量提取试剂盒、miScript Ⅱ反转录试剂盒、miScript SYBR Green PCR试剂盒均购自德国QIAGEN公司; Transwell小室购自美国BD公司; GAPDH、MCT7兔抗人单克隆抗体购自英国Abcam公司,羊抗兔二抗购自美国Santa Cruz公司; 双荧光素酶报告基因试剂盒(Dual-Luciferase Reporter Assay System)购自美国Promega公司.
1.2 方 法1.2.1 细胞培养和转染人胶质瘤U251细胞用含10%(体积分数,下同)胎牛血清、100 U/mL青霉素及100 μg/mL链霉素的DMEM培养液,置于37 ℃、5%(体积分数,下同)CO2的培养箱中培养,1~2 d更换一次培养液,常规消化传代.取处于对数生长期的细胞并计数,调整细胞密度为约2×105 mL-1后接种于6孔板中,更换为不含抗生素的DMEM培养液(含10%胎牛血清)继续培养24 h; 待细胞融合率达70%~80%时,按HiPerFect转染试剂说明书进行操作.实验分3组:1)实验组(mimics组),转入miR-193b mimics; 2)阴性对照组(NC组),转入miR-negative control; 3)空白对照组(mock组),正常培养,未转入任何miRNA.培养6~8 h后将培养液换成含10%胎牛血清的完全培养液,继续常规培养6~72 h后,根据实验的需要进行相关细胞功能学检测.
1.2.2 实时荧光定量PCR(qRT-PCR)检测收集转染24,48 h后的U251细胞,按miRNeasy小量提取试剂盒说明书的操作步骤提取miRNA; 根据miScript Ⅱ反转录试剂盒说明书的操作步骤合成cDNA; 并按miScript SYBR Green PCR试剂盒说明书配制PCR反应体系,在LightCycler480 PCR仪上进行目的片段的扩增检测.PCR反应条件为:95 ℃ 15 min预变性; 94 ℃ 15 s变性,55 ℃ 30 s退火,70 ℃ 30 s延伸,共40个循环.分别以GAPDH和U6为内参基因,以ddH2O作为空白对照,采用2-ΔΔCT相对定量法计算各组细胞中的miR-193b和MCT7的相对表达量,并以此计算miR-193b的转染效率,转染效率=(mimics组相对表达量-mock组相对表达量)/mimics组相对表达量.重复3次.
1.2.3 划痕实验取转染后24 h并处于对数生长期的各组细胞,接种于6孔板,每组设3个重复孔.待细胞融合率达80%~90%左右时,用200 μL吸头垂直于孔板背后的横线划痕,显微镜下记录划痕距离并拍照.用磷酸盐缓冲液(PBS)清洗细胞3次后,更换为无血清的DMEM培养液继续培养24 h.再次在显微镜下(放大倍数40×)记录划痕距离并拍照.重复3次.
1.2.4 Transwell小室侵袭实验转染24 h后的细胞,用胰酶消化,用无血清的DMEM 培养液制备细胞密度为2×105 mL-1的细胞悬液.取细胞悬液200 μL加入上室中,并在下室中加入500 μL含10%胎牛血清的DMEM培养液,每组设3个重复孔.置于37 ℃、5% CO2的细胞培养箱中培养24 h后,取出小室用95%(体积分数)乙醇固定10 min,结晶紫染色液染色20 min,再用无菌棉签擦去Matrigel基质胶和上室内的细胞,将小室置于倒置光学显微镜下(放大倍数200×),随机选取5个视野对穿膜细胞计数并拍照.重复3次.
1.2.5 双荧光素酶报告基因系统检测应用TargetScan、PicTar及microRNA等生物信息学软件网站预测得miR-193b的潜在下游靶基因MCT7,并构建包含miR-193b结合位点的野生型(PGL3-MCT7-3'UTR)和突变型(PGL3-MCT7-3'UTR mut)双荧光素酶报告质粒(购自上海吉凯基因化学技术有限公司),分别与miR-193b mimics、miR-negative control共转染U251细胞,并设计空白对照,转染24~48 h后,按Dual-LuciferaseReporter Assay System说明书进行操作:吸去24孔板中培养基,加入300 μL 1×Passive Lysis Buffer,放至4 ℃冰箱反应20 min待细胞充分裂解; 吸取40 μL细胞裂解液于Lockwell maxisorp检测板中,加入20 μL Luciferase Assay Reagent,震荡混匀后立即使用酶标仪检测萤火虫荧光酶(firefly luminescence)的荧光值; 检测后每孔中加入20 μL Stop&GloReagent,震荡混匀,静置3 min后使用酶标仪检测海肾荧光酶(renilla luminescence)的荧光值.
1.2.6 蛋白质免疫印迹(Western blot)检测取转染48 h后的各组细胞常规提取总蛋白,用BCA(bicinchoninic acid)法测定蛋白浓度.分别取30 μg蛋白进行电泳后转膜,用含5%(质量分数)脱脂奶粉的封闭液常温封闭1 h; 加入一抗(MCT7兔抗人单克隆抗体)4 ℃反应过夜,再用辣根过氧化物酶标记的羊抗兔二抗(稀释比例1:5 000)室温下反应1 h; 电化学发光法显影,定影.以GAPDH为内参,重复3次.
1.2.7 统计学分析应用SPSS 19.0软件进行统计学分析,数据以平均值±标准差表示,组间比较采用t-检验,p<0.05表示差异显著.
- [1] OHGAKI H,KLEIHUES P.Epidemiology and etiology of gliomas[J].Acta Neuropathologica,2005,109(1):93-108.
- [2] OKAMOTO Y,PATRE P L D,BURKHARD C,et al.Population-based study on incidence,survival rates,and genetic alterations of low-grade diffuse astrocytomas and oligodendrogliomas[J].Acta Neuropathologica,2004,108(1):49-56.
- [3] REARDON D A,RICH J N,FRIEDMAN H S,et al.Recent advances in the treatment of malignant astrocytoma[J].Journal of Clinical Oncology,2006,24(8):1253-1265.
- [4] KWAK H J,KIM Y J,CHUN K R,et al.Downregulation of Spry2 by miR-21 triggers malignancy in human gliomas[J].Oncogene,2011,30(21):2433-2442.
- [5] LAURA G,MARTINA D R,SERENA V,et al.Anti-miR21 oligonucleotide enhances chemosensitivity of T98G cell line to doxorubicin by inducing apoptosis[J].American Journal of Cancer Research,2015,5(1):231-242.
- [6] TAN X C,WANG S,ZHU L Y,et al.cAMP response element-binding protein promotes gliomagenesis by modulating the expression of oncogenic microRNA-23a[J].Proceedings of the National Academy of Sciences of the United States of America,2012,109(39):15805-15810.
- [7] SUN L,YAN W,WANG Y,et al.MicroRNA-10b induces glioma cell invasion by modulating MMP-14 and uPAR expression via HOXD10[J].Brain Research,2011,1389(7):9-18.
- [8] TANG H,LIU X,WANG Z,et al.Interaction of hsa-miR-381 and glioma suppressor LRRC4 is involved in glioma growth[J].Brain Research,2011,1390(20):21-32.
- [9] LI G,ZHANG Z,TU Y,et al.Correlation of microRNA-372 upregulation with poor prognosis in human glioma[J].Diagnostic Pathology,2013,8(1):1-6.
- [10] RATHOD S S,RANI S B,KHAN M,et al.Tumor suppressive miRNA-34a suppresses cell proliferation and tumor growth of glioma stem cells by targeting Akt and Wnt signaling pathways[J].Febs Open Bio,2013,4(1):485-495.
- [11] DAI D W,LU Q,WANG L X,et al.Decreased miR-106a inhibits glioma cell glucose uptake and proliferation by targeting SLC2A3 in GBM[J].BMC Cancer,2013,13(4):478.
- [12] LIU R,LI W,WU C.A functional polymorphism in the pre-miR-146a gene influences the prognosis of glioblastoma multiforme by interfering with the balance between Notch1 and Notch2[J].Molecular Medicine Reports,2015,12(4):5475-5481.
- [13] SILBER J,LIM D A,PETRITSCH C,et al.miR-124a and miR-137 inhibit proliferation of GBM cells and induce differentiation of tumor stem cells[J].BMC Me-dicine,2008,6(1):14.
- [14] WANG J,HUANG W C,WU Y H,et al.MicroRNA-193 pro-proliferation effects for bone mesenchymal stem cells after low-level laser irradiation treatment through inhibitor of growth family,member 5[J].Stem Cells & Development,2012,21(13):2508-2519.
- [15] LI X F,YAN P J,SHAO Z M.Downregulation of miR-193b contributes to enhance urokinase-type plasminogen activator(uPA)expression and tumor progression and invasion in human breast cancer[J].Oncogene,2009,28(44):3937-3948.
- [16] XU C,LIU S,FU H,et al.MicroRNA-193b regulates proliferation,migration and invasion in human hepatocellular carcinoma cells[J].European Journal of Cancer,2010,46(15):2828-2836.
- [17] NYHAN M J,O'DONOVAN T R,BOERSMA A W M,et al.MiR-193b promotes autophagy and non-apoptotic cell death in oesophageal cancer cells[J].BMC Cancer,2016,16(1):1-13.
- [18] FROBERG M K,GERHART D Z,ENERSON B E,et al.Expression of monocarboxylate transporter MCT1 in normal and neoplastic human CNS tissues[J].Neuroreport,2001,12(4):761-765.
- [19] LI K K W,PANG C S,CHING K K,et al.miR-124 is frequently down-regulated in medulloblastoma and is a negative regulator of SLC16A1[J].Human Pathology,2009,40(9):1234-1243.
- [20] MATHUPALA S P,PRAHLAD P,SLOAN A E.Silencing of monocarboxylate transporters via small interfering ribonucleic acid inhibits glycolysis and induces cell death in malignant glioma:an in vitro study[J].Neurosurgery,2004,55(6):1410-1419.
- [21] MIRANDA-GONÇALVES V,HONAVAR M,PINHEIRO C,et al.Monocarboxylate transporters(MCTs)in gliomas:expression and exploitation as therapeutic targets[J].Neuro-oncology,2013,15(2):172-188.
- [22] ENERSON B E,DREWES L R.Molecular features,regulation,and function of monocarboxylate transporters:implications for drug delivery[J].Journal of Pharmaceutical Sciences,2003,92(8):1531-1544.
- [23] HALESTRAP A P,MEREDITH D.The SLC16 gene family:from monocarboxylate transporters(MCTs)to aromatic amino acid transporters and beyond[J].Pflügers Archiv,2004,447(5):619-628.