摘要
全文
图/表
参考文献
引言
1 正文
在正常人体细胞中,葡萄糖主要经有氧代谢分解成水和CO2,并产生大量能量.早在20世纪20年代,Otto Warburg就发现即使在氧气充足的情况下,肿瘤细胞依然倾向于通过糖酵解分解葡萄糖为细胞提供能量,同时将丙酮酸转化成乳酸,并将该现象称为Warburg效应[1].大多数肿瘤在发生和发展过程中都会出现Warburg效应,且其发生与多种癌基因的激活和抑癌基因的失活有关[2].c-Src是首个在动物细胞中被发现的原癌基因,其编码的非受体酪氨酸激酶c-Src在促进多种癌症的发生和转移中起重要作用.但c-Src是否通过增强Warburg效应促进肿瘤的发生和发展尚不清楚,因此探究c-Src与葡萄糖代谢的关系对揭示其致癌机理有重要意义.
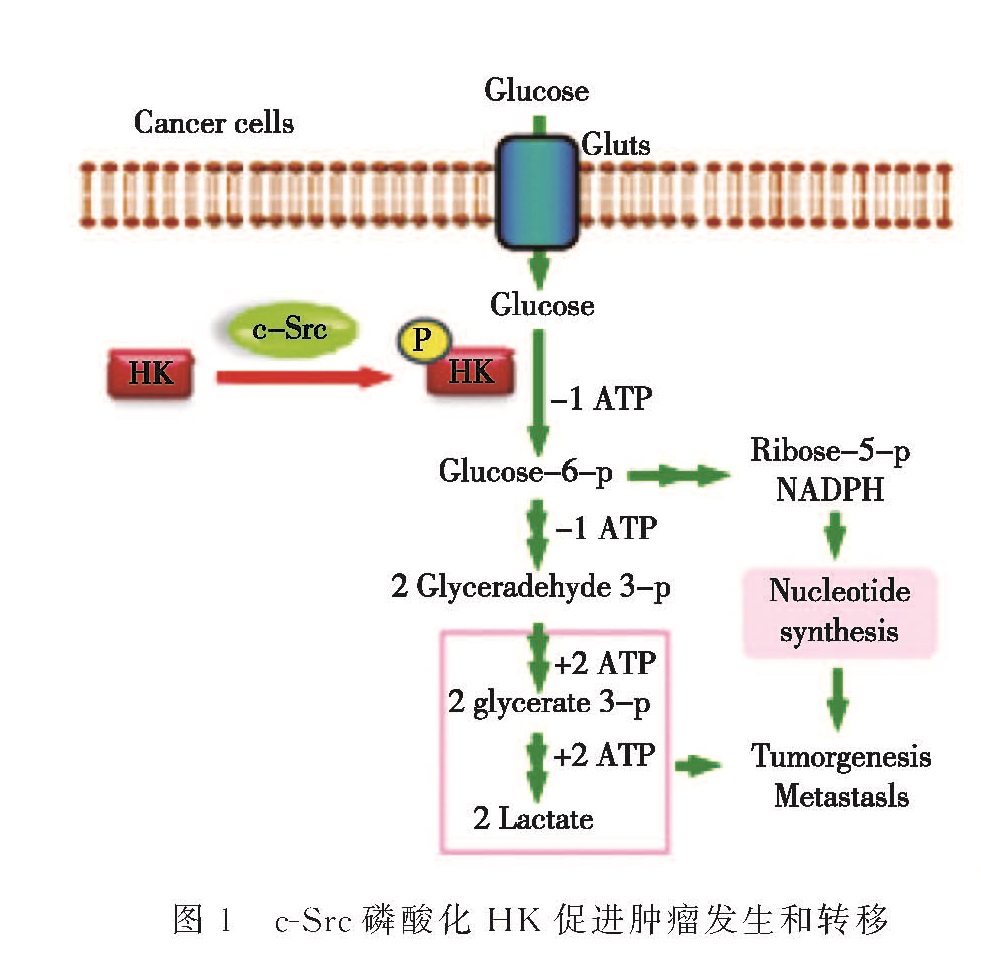
2017年1月5日,厦门大学生命科学学院李勤喜教授课题组在《Nature Communications》上在线发表研究论文[3],发现c-Src能和糖酵解途径中的限速酶己糖激酶(HK)相互作用并使之发生磷酸化,磷酸化位点分别为HK1的Y732和HK2的Y686,磷酸化强度与c-Src的活性呈正相关.这一磷酸化修饰使得HK1和HK2的酶活性大大增强,从而促进葡萄糖的摄入及糖酵解的速率.在机理上,Y732位点的磷酸化能引起HK1的构象变化,导致其寡聚体结构被破坏,增加其对葡萄糖的亲和力,从而增强其催化活性.另外,由于HK1对葡萄糖的米氏常数较小,在葡萄糖极度缺乏的情况下,HK1而不是HK2对肿瘤细胞的存活具有重要作用.总之,该项研究揭示了c-Src能通过磷酸化HK激活糖酵解、增强Warburg效应,进而促进肿瘤的发生和转移(图1).
目前,通过抑制糖酵解来治疗肿瘤这一思路被广泛的关注.基于该思路而研发并处于临床前试验的多种药物均以HK作为靶点[4],但是由于这些药物会阻断正常细胞对葡萄糖的利用,因此对人体内一些高度依赖于葡萄糖的细胞(如脑细胞)有很强的毒性,严重限制了其在临床上的应用.该项研究发现c-Src能与HK相互作用,为肿瘤的治疗提供了新的靶点,可以针对c-Src与HK的相互作用设计特异性的靶向药物破坏这种相互作用,这样既抑制了c-Src对HK的过度激活,又不影响HK的基本功能,因此与HK的其他抑制剂相比很有可能会降低毒副作用.另外,检测肿瘤样品中HK1的Y732磷酸化水平不仅能指示c-Src对糖酵解的激活程度,还与肿瘤转移密切相关.综上所述,该项研究不仅为今后开发新型抗肿瘤药物提供了新的思路,同时为肿瘤转移的预测提供了新的方法.
- [1] KOPPENOL W H,BOUNDS P L,DANG C V.Otto Warburg's contributions to current concepts of cancer metabolism[J].Nature Reviews Cancer,2011,11(5):325-337.
- [2] HAY N.Reprogramming glucose metabolism in cancer:can it be exploited for cancer therapy?[J].Nature Reviews Cancer,2016,16(10):635-649.
- [3] ZHANG J,WANG S,JIANG B,et al.c-Src phosphorylation and activation of hexokinase promotes tumorigenesis and metastasis[J].Nature Communications,2017,8:13732.
- [4] VANDER HEIDEN M G.Targeting cancer metabolism:a therapeutic window opens[J].Nature Reviews Drug Discovery,2011,10(9):671-684.