(1.厦门大学 分子疫苗学与分子诊断学国家重点实验室,国家传染病诊断试剂与疫苗工程技术研究中心,2.厦门大学生命科学学院,3.厦门大学公共卫生学院,福建 厦门 361102)
(1.State Key Laboratory of Molecular Vaccinology and Molecular Diagnostics,National Institute of Diagnostics and Vaccine Development in Infectious Diseases,Xiamen University,2.School of Life Sciences,Xiamen University,3.School of Public Health,Xiamen Univ
DOI: 10.6043/j.issn.0438-0479.201602011
备注
为建立血清中丙型肝炎病毒(HCV)中和抗体检测及评价手段,运用HCV核心区特异性抗体17H11及链霉亲和素-生物素放大系统,建立了基于酶联免疫斑点(ELISPOT)技术的HCV中和抗体检测平台.结果显示,该平台计数点清晰,可实现阴阳性分开,并能有效地检测并评价HCV 抗体阳性病人血清的中和作用,表明该平台可实现HCV中和抗体的检测,将有利于HCV疫苗研制中的免疫效果评价.
To establish the detection and evaluation methods of hepatitis C virus(HCV)neutralizing antibody in serum,an enzyme-linked immunospot assay(ELISPOT)based platform was established for detection of HCV neutralizing antibody using HCV core specific antibody 17H11 and streptavidin-biotin amplification system.This platform shows clearly counted foci and differentiable signals between positive and negative samples,which can also effectively detect and evaluate the neutralization effect in patients with the positive HCV antibody reaction.This platform is proved as an efficient HCV neutralizing antibody detection method and will benefit the evaluation of immunity effect in HCV vaccine development.
引言
丙型肝炎病毒(hepatitis C virus,HCV)是单股正链RNA病毒,属黄病毒科(Flaviviridae)嗜肝病毒属(Hepatovirus).HCV经过血液传播,感染人类可引发肝炎,并易发展为慢性肝炎、肝硬化甚至肝癌[1].据世界卫生组织(WHO)报告,全世界约有1.3亿~1.5亿人感染HCV病毒,每年新增300万~400万例病毒感染病例,约50万人死于HCV感染相关的肝病,HCV已成为严重危害人类健康的公共卫生问题.
治疗丙型肝炎的药物研究已取得了较大进展,美国食品药品监督管理局(FDA)最近批准的ledipasvir和sofosbuvir复合制剂Harvoni,对1型丙肝患者的有效治愈率可达到95%[2].然而鉴于Harvoni昂贵的治疗费用以及HCV患者不一定能及时发现等原因,研制疫苗控制HCV感染仍是目前主要的研究方向之一[3].现阶段实验室研制的疫苗包括重组蛋白、合成肽、病毒载体疫苗和DNA疫苗等,由于HCV基因组的高变异性,效果均不理想[4].除此之外,缺乏有效的体外中和抗体评价模型也是HCV疫苗快速研发的限制性因素之一.本研究拟运用HCV核心区特异性抗体17H11建立HCV中和抗体评价筛选的快速、高通量酶联免疫斑点(ELISPOT)检测平台,以实现备选疫苗免疫血清中和效果的评价.
1 材料与方法
1.1 细胞、病毒的培养人肝癌Huh7.5.1细胞使用添加了100 U/mL青霉素、100 mg/mL链霉素、10%(体积分数,下同)胎牛血清(FBS)、0.1 mmol/L非必需氨基酸的DMEM完全培养基[5],于37 ℃、5%(体积分数,下同)CO2的细胞培养箱中培养.HCV病毒株为使用Huh7.5.1细胞体外培养的HCV-JFH-1株,由厦门大学附属中山医院惠赠.
1.2 17H11单克隆抗体的来源及制备HCV核心区重组蛋白DPC173与弗氏佐剂(Sigma-Aldrich公司)混合免疫BALB/c小鼠3次后,检测小鼠血清抗体滴度达到106,取小鼠的脾细胞与骨髓瘤细胞融合,用添加了氨基蝶呤、次黄嘌呤、胸腺嘧啶的含10% FBS的RPMI1640培养基(Gibco公司)筛选,获得产生单克隆抗体的杂交瘤细胞.将杂交瘤细胞注入小鼠腹腔,一周左右收集小鼠腹水,使用蛋白A柱(GE公司)纯化得到针对HCV核心区的鼠源单抗17H11[6].
1.3 肽段的合成为确定17H11的具体作用表位,HCV核心区共合成18条多肽,每条多肽和相邻的多肽有10个左右重叠的氨基酸[7],分别是核心区氨基酸序列第1~19位、11~31位、21~40位、31~50位、41~60位、51~70位、61~80位、71~91位、81~100位、92~109位、101~120位、111~130位、121~138位、131~150位、139~160位、151~170位、161~180位、171~191位,由上海生工生物工程股份有限公司合成.
1.4 免疫斑点实验(DIBA)将用磷酸盐缓冲液(PBS)梯度稀释成1 000,100,10,1,0.1 ng/μL的HCV重组抗原DPC173、超声处理后的细胞培养的HCV病毒株(HCVcc)、未处理的HCVcc及PBS各取1 μL点渍于硝酸纤维素膜方格内,置于干燥间干燥2 h后,用封闭液(20 mmol/L pH 8.0 Tris-HCl,2%(质量分数,下同)牛血清白蛋白(BSA),0.5%(质量分数)酪蛋白,0.1%(体积分数,下同)Tween 20)37 ℃封闭1 h; 17H11单抗用PBS稀释成10 μg/mL加入10 mL于平皿中37 ℃孵育1 h,洗涤3次后,加入用稀释液1(20%(体积分数)山羊血清,400 mmol/L pH 7.4 PBS,40%(质量分数)蔗糖,10%(质量分数)酪蛋白)按1:5 000稀释的辣根过氧化物酶标记的羊抗鼠(GAM-HRP,购自美国Sigma公司)二抗,37 ℃反应50 min; 洗涤3次后,用四甲基联苯胺(TMB)显色[8].
1.5 间接酶联免疫吸附试验(ELISA)鉴定抗体表位
合成的各区段多肽用PBS稀释成1 mg/mL,用20 mmol/L pH 9.6的碳酸盐缓冲液稀释成0.5 μg/mL,每孔100 μL加至96孔板,37 ℃放置2 h; 洗板1次后甩干,每孔加200 μL封闭液(20 mmol/L pH 8.0 Tris-HCl,2%BSA,0.5% 酪蛋白,0.1% Tween 20),37 ℃放置2 h后甩干; 17H11单抗用PBS稀释成10 μg/mL,每孔100 μL与各区段包被的ELISA板37 ℃反应40 min; 洗板5次后,加入用稀释液1按1:5 000稀释的GAM-HRP二抗,37 ℃反应30 min; 洗板5次,显色,读取450 nm下的吸光度(OD450)值[7].
1.6 17H11单抗标记生物素取1 mg生物素溶解于1 mL PBS,抗体与生物素(购自美国Sigma公司)按摩尔比1:20的比例混合,室温下放置1 h后转移至透析袋中,于4 ℃ PBS中透析6 h,中间换液3次,取出透析袋,将标记好的17H11抗体分装至EP管中,-20 ℃保存.
1.7 ELISPOT平台检测HCVcc病毒观察100 mm细胞培养盘中Huh7.5.1细胞生长到95%汇合率时,使用1 mL胰酶消化细胞,按每孔1×105个铺至96孔细胞培养板,于37 ℃、5% CO2的细胞培养箱培养12 h.将初始感染性滴度7×104 PFU(空斑形成单位)/mL的HCVcc病毒按照1:10梯度稀释后感染96孔板中的Huh7.5.1细胞,感染后36 h,吸掉培养基及病毒,PBS洗板1次后每孔加入50 μL -20 ℃冰浴的100%甲醇,-20 ℃放置15 min对细胞进行固定及通透.PBS洗板2次,每孔加入100 μL封闭液(1%BSA,0.25 mmol/L乙二胺四乙酸(EDTA))后置于37 ℃培养箱中封闭1 h; 洗板1次,每孔加入17H11或生物素标记的17H11 100 μL,37 ℃孵育1 h; 洗板5次后,加入GAM-HRP或辣根过氧化物酶标记的链霉亲和素(购自美国Sigma公司)100 μL,37 ℃孵育40 min; 洗板5次后,显色,读板[9].
1.8 ELISPOT平台与比色法自动计数平台评价HCV病人血清中和作用
100 mm细胞培养盘中细胞生长到95%汇合率后,用胰酶消化,按每孔1×105个细胞铺至96孔细胞培养板,放置于5% CO2的细胞培养箱培养.待细胞生长到90%汇合率后,将按2倍梯度稀释好的人血清(血清稀释倍数为0~211)与HCVcc病毒混匀后于37 ℃孵育1 h; 将孵育后的病毒感染Huh7.5.1细胞,感染后36 h使用ELISPOT平台检测细胞内的HCVcc复制情况.比色法自动计数平台(colorimetric focus-forming assay)细胞培养、血清稀释、病毒感染、固定、封闭、读板及分析与本平台相同,但比色法用针对HCV核心区鼠源IgG1抗体(购自Thermo公司)1:1 000稀释作为一抗,以碱性磷酸酶标记的羊抗鼠IgG(GAM-AP)为二抗,用5-溴-4-氯-3-吲哚基-磷酸盐/四唑硝基蓝(BCIP/NBT)显色[9].
2 结果与分析
2.1 DIBA验证17H11反应特异性为确定17H11与丙肝核心抗原的反应特应性,运用DIBA分别验证17H11与梯度稀释的HCV核心区重组蛋白DPC173及处理前后HCVcc的反应性,同时设置PBS作为阴性对照.如图1所示:HCV核心区重组抗原在DPC173蛋白质量浓度为1 000,100,10 ng/μL时与17H11有明显反应,1 ng/μL时有微弱反应,与PBS无反应.HCVcc在未处理的情况下与17H11无反应,究其原因,HCV病毒颗粒外有包膜蛋白包裹,未经处理的HCVcc核心区不能暴露; 而经过超声处理后核心区暴露,便可与17H11有明显抗原抗体反应.由此可知,17H11与重组抗原反应质量浓度下限约为10 ng/μL,可与HCVcc核心区有特异反应.
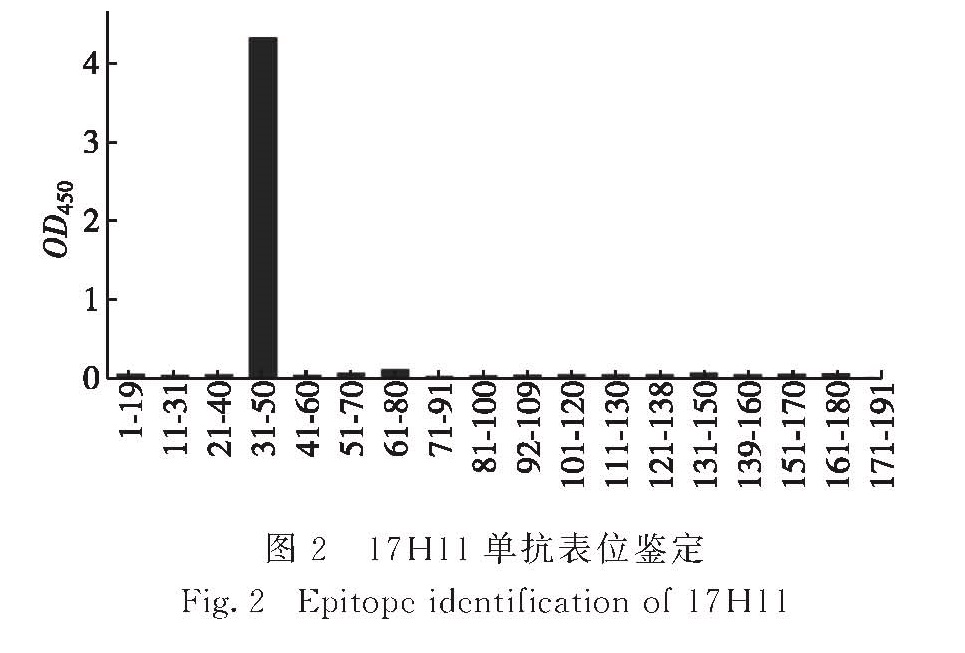
2.2 17H11表位鉴定如图2所示,通过ELISA间接法,将17H11分别与HCV核心抗原不同区段的肽段反应,17H11只与31~50区段多肽有强反应,可推测17H11作用的表位在HCV核心抗原的第31~50位氨基酸内.
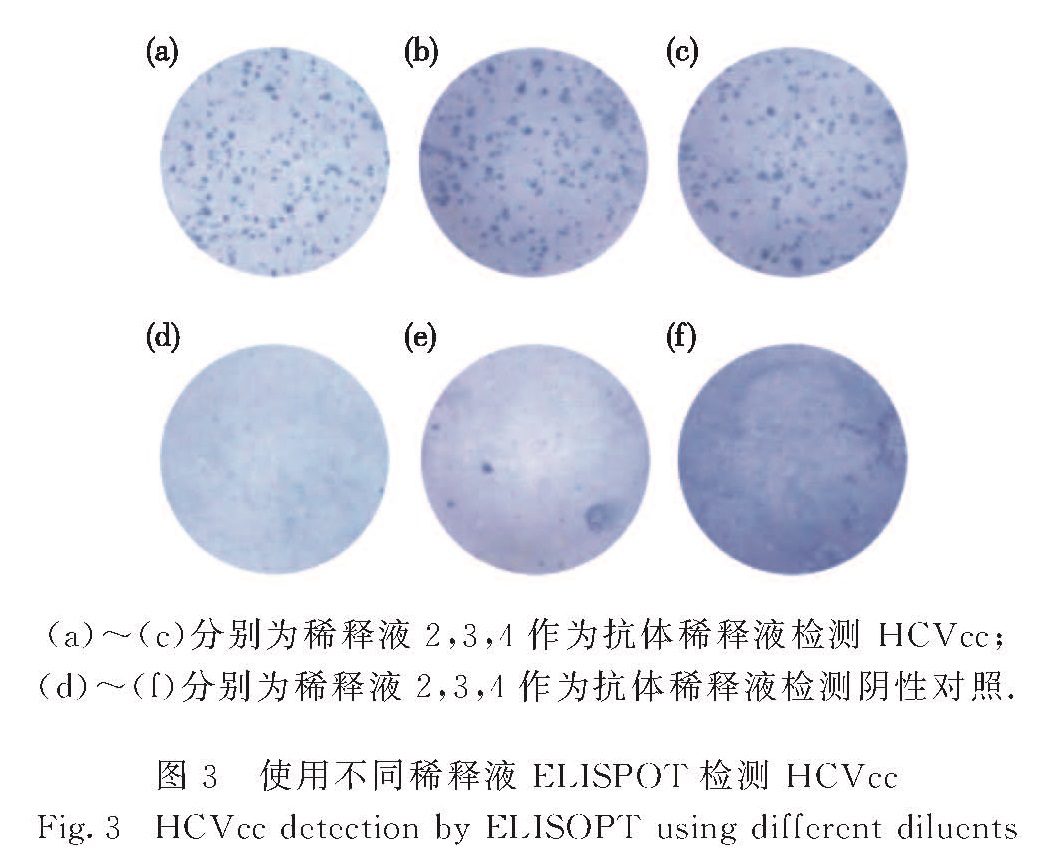
2.3 基于ELISPOT技术检测HCVcc平台的建立首先以17H11(0.5 μg/mL)为一抗,用GAM-HRP按1:5 000稀释为二抗,确定最佳的抗体稀释液.本研究共选择3种稀释液进行测试,分别是稀释液2(20 mmol/L pH 8.0 Tris-HCl,20% FBS,1%酪蛋白,10%蔗糖)、稀释液3(20 mmol/L pH 8.0 Tris-HCl,150 mmol/L NaCl,0.05% Tween 20,30% FBS,5 mmol/L CaCl2)和稀释液4(1 mol/L pH 7.85 Tris-HCl,20% FBS,10%酪蛋白,10%蔗糖).由图3可知:使用稀释液2作为抗体稀释液时,HCVcc病毒感染的孔中形成的斑点清晰(图3(a)),而无病毒感染的阴性对照孔中没有斑点形成且背景比较干净(图3(d)); 使用稀释液3和4进行ELISPOT检测时,HCVcc感染可检测到清晰斑点,但背景稍高(图3(b)和(c)),无病毒感染的阴性对照孔也能检测到斑点(图3(e)和(f)),存在背景本底过高的问题; 而稀释液2中的蔗糖可以有效地保持抗原的活性,FBS及酪蛋白可以起到降低非特异性反应的作用,又在一个较好的pH环境下有效地避免了稀释液3和4的问题.因此,最终确定使用稀释液2作为后续实验的抗体稀释液.
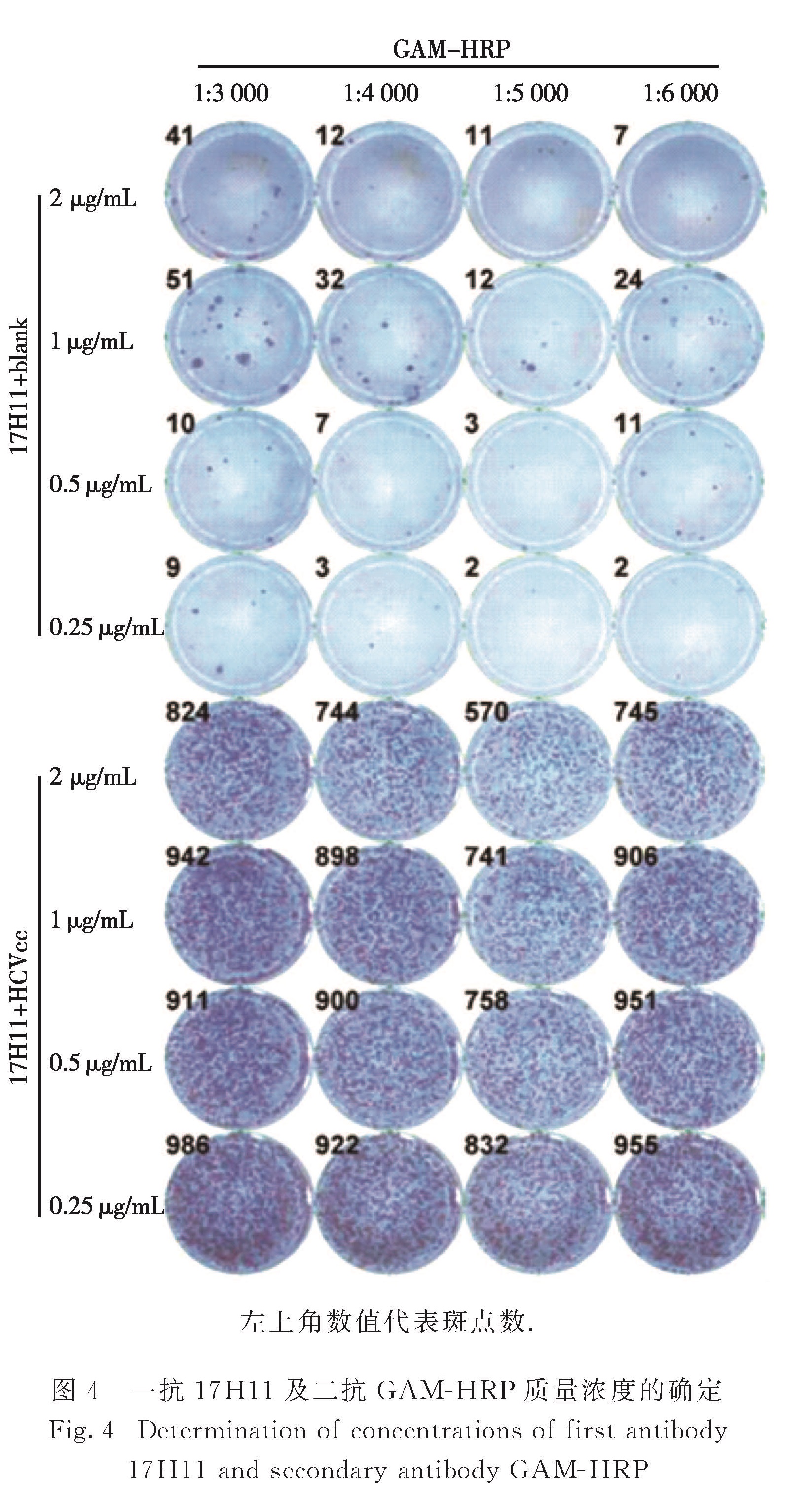
为了进一步确定ELISPOT使用的最佳抗体浓度,分别使用不同质量浓度的一抗17H11(0.25,0.5,1,2 μg/mL)和不同稀释倍数的GAM-HRP(1:3 000,1:4 000,1:5 000,1:6 000)为条件进行ELISPOT实验,结果如图4所示:当17H11质量浓度为0.25 μg/mL,二抗稀释倍数为1:5 000时,HCVcc感染的孔中形成的斑点清晰,且无病毒感染的阴性对照孔没有假阳性的斑点形成,背景干净.因此,确定了一抗17H11质量浓度0.25 μg/mL、二抗稀释倍数1:5 000为反应条件,可实现ELISPOT对HCVcc的检测.
左上角数值代表斑点数.
2.4 基于ELISPOT技术检测HCV中和抗体平台的建立小鼠是疫苗免疫最常用的动物,上述平台由于使用GAM-HRP作为二抗,不能用于小鼠血清中和抗体的检测.对此曾尝试17H11直接标记HRP,通过一步法检测HCVcc,但是存在很严重的非特异性反应(实验结果未展示).因此尝试将17H11标记生物素,使用GAM-HRP标记的链霉素作为二抗,通过链霉亲合素-生物素放大系统,实现HCVcc的检测.按照上述相同的方法,经过对稀释液、一抗及二抗浓度的摸索,最终确定检测条件如下:一抗使用标记生物素的17H11(1 mg/mL),稀释液1稀释4万倍使用; 二抗为SA-HRP(1 mg/mL),稀释液2稀释1万倍使用.由图5可以看出,经过调试后的中和抗体检测平台可实现阴阳性分开,并以此条件作为ELISPOT检测HCV中和抗体的反应条件.
2.5 ELISPOT中和抗体检测平台和比色法自动计数平台对HCV病人抗体阳性血
清中和效果评价
为了验证建立的平台是否能够检测HCV中和抗体,选取6份不同型别HCV病人的血清标本及2份正常人血清标本,病人血清编号及HCV型别为M256(2a)、M412(2a)、M107(1b)、M389(1b)、M115(3a)、M029(6a),正常人血清编号为N126和N124.经HCV抗体诊断试剂盒(酶联免疫法)检测,6份病人血清抗体呈阳性且检测值分别为3.845,2.046,3.546,1.178,2.227和1.463,2份正常人血清检测值为0.012和0.010.将血清梯度稀释后与病毒混合,感染Huh7.5.1细胞36 h后,分别用比色法自动计数平台及本研究建立的平台进行ELISPOT检测,每份血清样本做4组重复.如图6所示,对2种方法的计数点进行对比,r2值为0.930 6,p<0.000 1,说明本平台与已报道的方法得出结果有显著相关性,所得数据可靠.
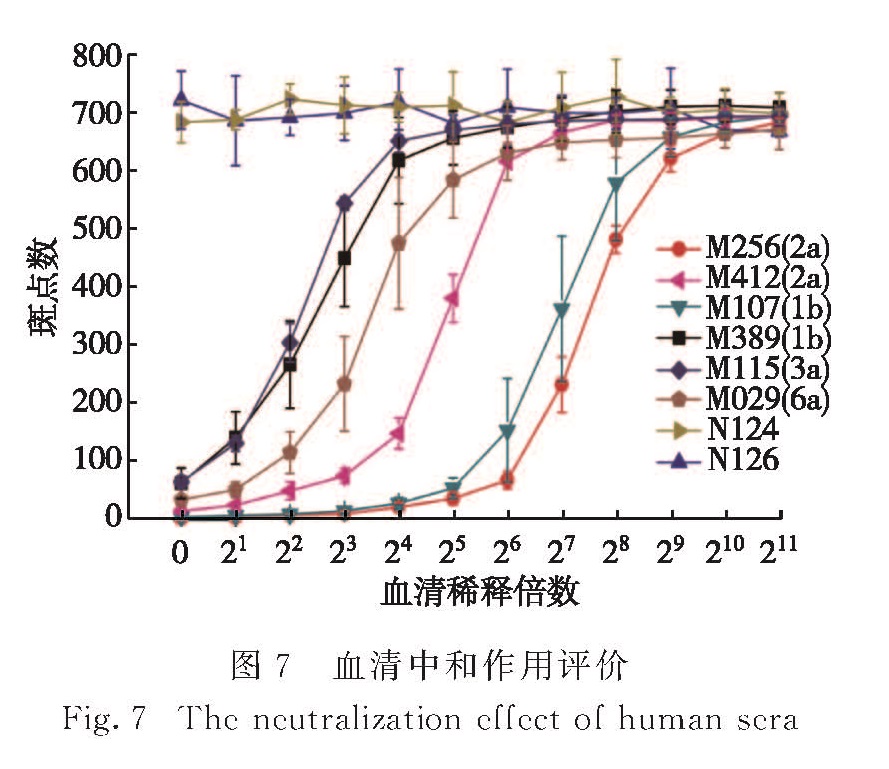
对本平台得出的中和效果进行评价,由图7可知:计数点随6份HCV病人血清的稀释倍数(0~211倍)增加而增加,而正常人血清不同的稀释倍数下计数点没有明显的变化,说明此6份HCV病人血清均具有对JFH-1(2a)病毒的中和作用; 而对2a型外的M107(1b)、M389(1b)、M115(3a)、M029(6a)标本同样有一定的中和作用,说明不同型别的HCV病人血清中存在广谱抗体; 此外,抗体水平最高的M256(2a)和M107(1b)中和效果最强.由于现阶段不同型别的HCV病人血清标本较少,抗体水平、型别与中和作用的关系仍需进一步验证.上述实验结果说明,本研究建立的中和抗体检测平台,可广泛应用于疫苗的评价和HCV病毒的入胞机制等基础研究.
3 讨 论
2005年,Wakita等从日本肝炎病人身上分离到一株JFH1病毒,将其全基因组转染至Huh7细胞,实现了HCV病毒的体外细胞培养[10].在此之前,有效的HCV体外感染性细胞模型及动物感染模型都严重缺乏,HCV现在可感染的动物模型有大猩猩、树枸等,但是黑猩猩在成本以及伦理上有很大的限制[11-12].现在普遍运用细胞感染模型进行HCV的相关研究.为了获得对HCV病毒高容许的细胞,不断对细胞进行改造,如Huh7.5、Huh7.5.1[13]等.本研究使用Huh7.5.1细胞培养HCVcc,收集含HCV病毒的上清,可继续感染Huh7.5.1细胞,获得第二代病毒,并可通过ELISPOT病毒检测平台测定感染复数(MOI),确定二代感染所用病毒量,以获得最大滴度的HCVcc.相比另一种细胞感染模型假性HCV颗粒(HCV pseudeo-particle,HCVpp),HCVcc是真正的病毒颗粒,不局限于HCV早期感染,可以真实地模拟HCV体外感染及中和的情况.
其他的HCV中和抗体检测评价方法有免疫荧光法(immunofluorescence assay)、荧光素酶检测法(luciferase assay)、反转录PCR[14]等,前2种方法过程繁琐,且不方便进行大规模的检测工作,反转录PCR容易污染,耗费时间久.本研究建立的平台借助自动化的ELISPOT仪器进行斑点计数和分析,可以有效地避免人为原因造成的误差,同时可以节省时间和人力,适合进行大规模的检测实验.且ELISPOT平台检测中和抗体在病毒疫苗相关研究中已得到了很好的应用[15].
本研究新建立的ELISPOT法主要依靠针对 HCV核心区特异性的抗体反应,并运用链霉亲合素-生物素放大的方法,相比Kang等[9]建立的基于核心区鼠抗及GAM-HRP反应的HCVcc比色法自动计数的检测平台,本研究建立的检测平台斑点更清晰,背景更干净,不但能区别感染和未感染的细胞,具有较高的特异性和灵敏度,在实现HCVcc检测的同时,还能完成鼠源中和抗体的筛选或者效价的确定; 此外,通过对HCV不同型别血清中和作用的评价,可发现不同型别中有广谱中和抗体的存在,与前人的报道相符[16],因此本平台可以实现不同亚型中和抗体的筛选,将有利于疫苗免疫效果的评价和优势表位的筛选等领域的研究.
综上所述,本研究建立的HCV中和抗体评价筛选的快速高通量ELISPOT检测平台,具有特异性好、操作简便、省时省力等优势,为今后HCV疫苗的评价提供了很好的技术支持.
- [1] 曾文婷,卢雪梅,汪洁,等.丙型肝炎病毒入胞抑制剂的研究进展[J].病毒学报,2015,31(1):97-105.
- [2] RAEDLER L A.Once-a-day Harvoni(ledipasvir plus sofosbuvir),a new oral combination for the treatment of patients with genotype 1 chronic hepatitis C infection[J].American Health & Drug Benefits,2015,8(Spec Feature):54-58.
- [3] 李婷婷,殷森,黎诚耀.丙型肝炎疫苗最新研究进展:挑战与希望并存[J],现代免疫学,2015,35(1):81-87.
- [4] GUMMOW J,LI Y,YU W,et al.A multiantigenic DNA vaccine that induces broad hepatitis C virus-specific T-cell responses in mice [J].Journal of Virology,2015,89(15):7991-8002.
- [5] YANAGI M,PURCELL R H,EMERSON S U,et a1.Hepatitis C virus:an infectious molecular clone of a second major genotype(2a)and lack of viability of intertypic 1a and 2a chimeras[J].Virology,1999,262(1):250-263.
- [6] KIMURA T,ROKUHARA A S,SAKAMOTO Y,et al.Sensitive enzyme immunoassay for hepatitis B virus core-related antigens and their correlation to virus load[J].Journal of Clinical Microbiology,2002,40(2):439-445.
- [7] KASHIWAKUMA T,HASEGAWA A,KAJITA T,et al.Detection of hepatitis C virus specific core protein in serum of patients by a sensitive fluorescence enzyme immunoassay(FEIA)[J].Journal of Immunological Methods,1996,190(1):79-89.
- [8] VIJAYANANDRAJ S,YOGITA M,AMRITA D,et al.Highly efficient immunodiagnosis of large cardamom chirke virus using the polyclonal antiserum against Esche-richia coli expressed recombinant coat protein[J].Indian Journal of Virology,2014,24(2):227-234.
- [9] KANG W,SHIN E C.Colorimetric focus-forming assay with automated focus counting by image analysis for quantification of infectious hepatitis C virions[J].PLoS One,2012,7(8):e43960.
- [10] WAKITA T,PIETSCHMANN T,KATO T,et al.Production of infectious hepatitis C virus in tissue culture from a cloned viral genome[J].Nature Medicine,2005,11(7):791-796.
- [11] SHIMIZU Y K,WEINER A J,ROSENBLATT J,et al.Early events in hepatitis C virus infection of chimpanzees[J].Proceedings of the National Academy of Sciences of the United States of America,1990,87(16):6441-6444.
- [12] WALTER E,KEIST R,NIEDEROST B,et al.Hepatitis B virus infection of tupaia hepatocytes in vitro and in vivo[J].Hepatology,1996,24(1):1-5.
- [13] ZHONG J,GASTAMINZA P,CHENG G,et al.Robust hepatitis C virus infection in vitro[J].Proceedings of the National Academy of Sciences of the United States of America,2005,102(26):9294-9299.
- [14] LIU L P,YE L,WANG X,et al.Cyclosporina inhibits hepatitis C virus replication and restores interferon-alpha expression in hepatocytes[J].NIH Public Access,2011,13(1):24-32.
- [15] LI T D,LIN H J,YU L Q,et al.Development of an enzyme-linked immune spot assay for determination of rotavirus infectivity[J].Journal of Virological Methods,2014,209:7-14.
- [16] RACHAEL E S,VANESSA M C.Broad anti-HCV antibody responses are associated with improved clinical di-sease parameters inchronic HCV infection [J].Journal of Virology,2016.doi :10.1128/JVI.02669-15.